Clear Sky Science · pt
Desenvolvimento de ligantes derivados da capsaicina para Prohibitin visando modular a interação Aurora quinase A/PHB2 e a mitofagia em células cancerosas
Por que um composto da pimenta importa para o câncer
As pimentas devem sua ardência à capsaicina, uma pequena molécula que se liga a proteínas em nossas células. Este estudo explora uma reviravolta surpreendente desse conhecido tempero: pesquisadores redesenharam a capsaicina para criar novas moléculas com características de fármaco que se direcionam às “usinas” das células cancerosas — as mitocôndrias — e atenuam um processo que essas células usam para manter suas fábricas de energia em bom funcionamento. Como células tumorais dependem fortemente de mitocôndrias eficientes para alimentar o crescimento desenfreado, ser capaz de interromper seletivamente esse sistema de suporte pode abrir um novo caminho para terapias anticâncer.
Usinas celulares e sua equipe interna de limpeza
As mitocôndrias equilibram constantemente a construção de novas unidades com a reciclagem das danificadas. O lado da reciclagem, chamado mitofagia, atua como um sistema de controle de qualidade: mitocôndrias desgastadas são marcadas e degradadas, enquanto as mais saudáveis permanecem. Muitas células cancerosas se apropriam desse equilíbrio, usando a mitofagia para eliminar mitocôndrias fracas e enriquecer “super-desempenhadoras” que produzem grandes quantidades de ATP, a moeda energética da célula. Uma proteína chamada Aurora quinase A (AURKA), frequentemente superexpressa em tumores, foi recentemente encontrada dentro das mitocôndrias onde se combina com outra proteína, Prohibitin‑2 (PHB2), e com o adaptador de autofagia LC3. Juntas, formam um complexo que promove a mitofagia e sustenta a alta produção de energia em células cancerosas.
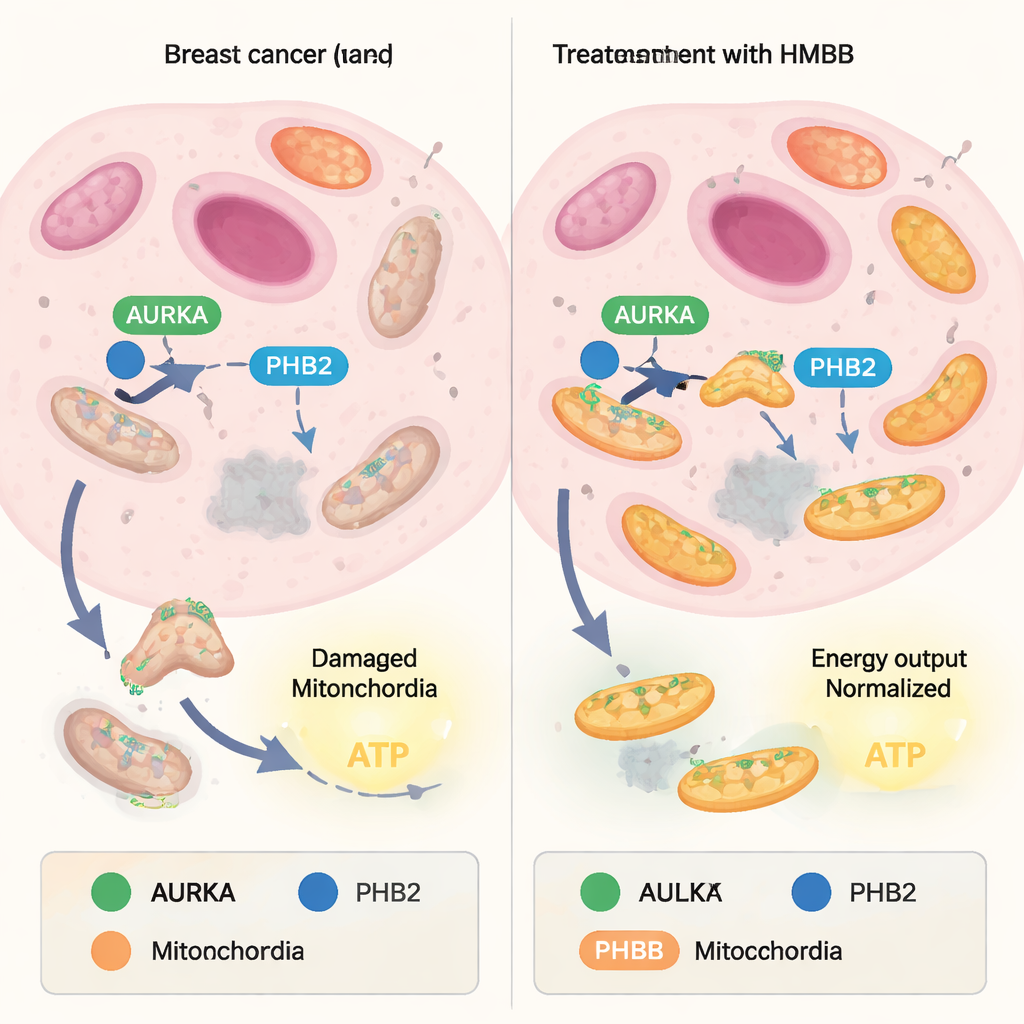
Da capsaicina picante a ferramentas moleculares sob medida
Trabalhos anteriores mostraram que um composto natural chamado xantumol pode se ligar à PHB2 e interromper o complexo AURKA–PHB2–LC3, bloqueando a mitofagia e reduzindo a produção mitocondrial de ATP. No entanto, a estrutura química do xantumol não é ideal para desenvolvimento de fármacos. Neste estudo, os autores voltaram-se para a capsaicina, outro ligante natural da PHB, e investigaram se ela poderia ser remodelada em ferramentas mais práticas. Primeiro confirmaram que a capsaicina enfraquece ligeiramente a interação entre AURKA e PHB2 em células de câncer de mama vivas, usando uma técnica de imagem (FRET/FLIM) que mede o quão próximas duas proteínas marcadas estão entre si. Em seguida, sintetizaram 16 moléculas inspiradas na capsaicina modificando a “cauda” e a “cabeça” aromática da estrutura original e testaram sistematicamente como cada versão afetava a parceria AURKA–PHB2 dentro das mitocôndrias.
Descobrindo uma “cola” molecular que prende proteínas juntas
As moléculas modificadas tiveram efeitos marcadamente diferentes. Algumas, como a própria capsaicina ou um derivado chamado composto 5, facilitaram a separação de AURKA e PHB2. Outras quase não tiveram efeito. Um subconjunto, no entanto — especialmente uma molécula chamada composto 13, depois denominada HMBB — teve o efeito oposto e apertou significativamente a ligação entre AURKA e PHB2. Simulações de acoplamento por computador ajudaram a explicar esse comportamento. Capsaicina e o composto 5 tendiam a se acomodar no sítio ativo de AURKA de formas que criavam colisões físicas com a PHB2, empurrando as duas proteínas para longe. Em contraste, os compostos 12 e 13 encaixaram-se no sítio ativo de AURKA e simultaneamente contataram um bolso inibitório conhecido na PHB2 sem causar uma colisão. Em vez disso, suas formas permitiram que agissem como uma “cola molecular”, fazendo a ponte entre AURKA e PHB2 e estabilizando o complexo.
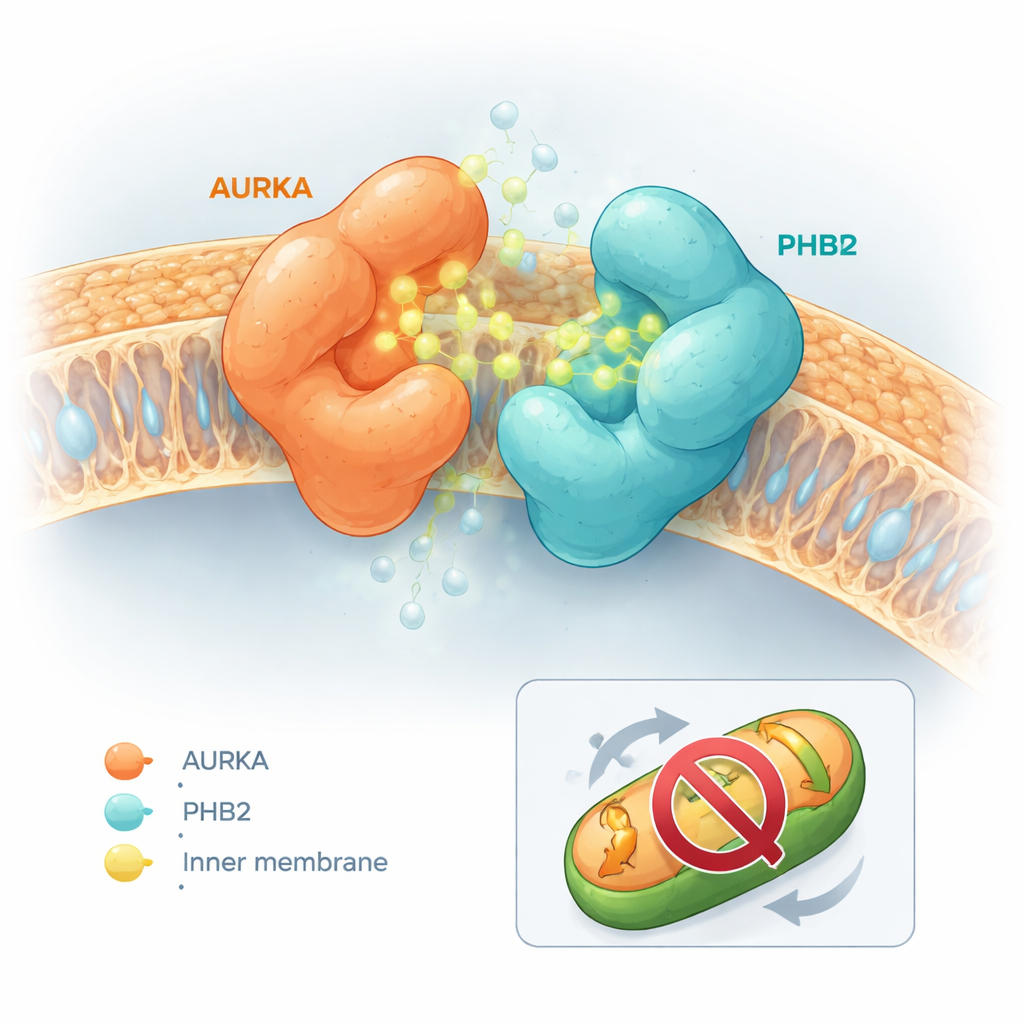
Bloqueando a limpeza mitocondrial sem desligar o centro de controle da célula
Uma questão crucial era saber se esse comportamento de cola molecular simplesmente desativava a AURKA em toda a célula, o que acarretaria risco de efeitos colaterais amplos, ou se agia de forma mais seletiva. Usando um biossensor fluorescente separado que indica a ativação de AURKA nos centríolos — as estruturas que organizam a maquinaria de divisão celular — a equipe observou que o HMBB não reduziu a atividade de AURKA nesses locais. Entretanto, em ensaios mitocondriais, o HMBB reverteu a perda de massa mitocondrial normalmente causada pela superexpressão de AURKA em células de câncer de mama. Em células que naturalmente produzem altos níveis de AURKA, o HMBB aumentou o conteúdo mitocondrial, indicando que a mitofagia induzida por AURKA foi bloqueada. Em células com baixos níveis de AURKA, o HMBB teve pouco impacto, ressaltando sua dependência da via AURKA–PHB2.
O que isso pode significar para tratamentos futuros do câncer
Em conjunto, os achados mostram que derivados de capsaicina cuidadosamente desenhados podem afinar a interação entre AURKA e PHB2 nas mitocôndrias. Ao agir como cola molecular, HMBB e compostos relacionados prendem AURKA e PHB2 em uma configuração que impede o prosseguimento do programa usual de mitofagia, sem desativar os papéis essenciais de AURKA em outras partes da célula. Para um leitor leigo, a ideia principal é que os autores criaram moléculas protótipo que interferem seletivamente em como as células cancerosas mantêm suas usinas de energia em bom estado, potencialmente enfraquecendo seu suprimento energético enquanto preservam funções celulares normais. Embora esses compostos ainda estejam em estágio inicial, em laboratório, eles ilustram uma estratégia promissora: usar pequenas moléculas com propriedades farmacológicas para direcionar parcerias proteicas específicas dentro das mitocôndrias e, assim, minar as vantagens metabólicas das quais muitos tumores dependem.
Citação: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Palavras-chave: mitocôndrias, mitofagia, Aurora quinase A, derivados da capsaicina, metabolismo do câncer