Clear Sky Science · pt
Remodelação funcional de células iNKT por células NKT tipo II reativas a sulfátide reprograma macrófagos alveolares para aliviar lesão por isquemia-reperfusão pulmonar
Por que proteger pulmões doadores importa
Quando cirurgiões transplantam um pulmão ou restauram o fluxo sanguíneo após uma obstrução, o retorno súbito de oxigênio pode paradoxalmente lesar o tecido. Esse problema, chamado lesão por isquemia–reperfusão pulmonar, é uma causa principal de falha precoce após transplante pulmonar e outros procedimentos críticos. O estudo resumido aqui investiga como um conjunto raro de células imunes pode ser “reprogramado” para acalmar a inflamação, oferecendo uma possível nova forma de proteger pulmões frágeis quando eles mais são necessários.
Células imunes que podem curar ou prejudicar
Nossos pulmões são patrulhados por macrófagos alveolares, células do sistema imune que ficam nos alvéolos e respondem rapidamente ao perigo. Essas células podem alternar entre dois modos principais. Em um modo “de combate” (frequentemente chamado de M1), elas liberam substâncias inflamatórias que ajudam a matar germes, mas também podem danificar o tecido. Em um modo “de reparo” (frequentemente chamado de M2), liberam moléculas que acalmam, limitam a inflamação e auxiliam na cura. Na lesão por isquemia–reperfusão pulmonar, o equilíbrio se inclina para o modo de combate prejudicial. Os pesquisadores supuseram que, se pudessem empurrar os macrófagos com delicadeza para o modo de reparo no momento certo, poderiam atenuar o impacto dessa lesão.
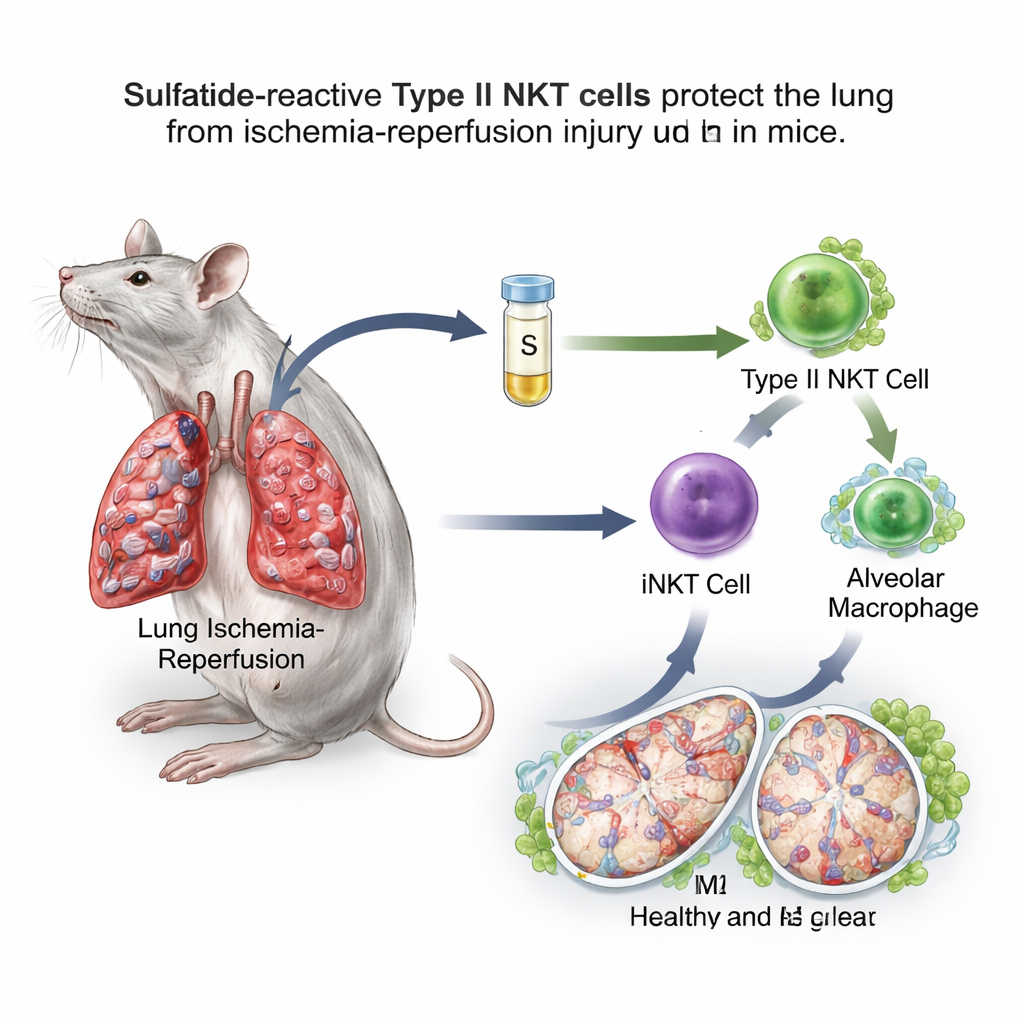
Uma molécula açúcar–gordura inverte um interruptor imune
A equipe focou nas células T natural killer (NKT), células imunes incomuns que ficam entre as defesas inatas de ação rápida e respostas mais lentas e específicas. As células NKT existem em dois tipos principais. O tipo I, também chamado de NKT invariante (iNKT), é conhecido por agravar a isquemia–reperfusão pulmonar em camundongos. As células NKT do tipo II, no entanto, podem conter reações imunes em outros órgãos. Uma molécula gordurosa chamada sulfátide é reconhecida especificamente pelas células NKT tipo II. Em um modelo de camundongo em que o fluxo sanguíneo para um pulmão foi clamped por uma hora e depois restaurado, os pesquisadores administraram sulfátide várias horas antes do insulto. Eles descobriram que camundongos tratados com sulfátide apresentaram menos inchaço pulmonar, menos vasos sanguíneos permeáveis, menor estresse oxidativo, melhores níveis de oxigenação e redução de substâncias inflamatórias no líquido de lavagem pulmonar em comparação com animais não tratados.
Reprogramando macrófagos por meio de um revezamento de sinais
Exames mais detalhados mostraram que a sulfátide deslocou os macrófagos alveolares para o estado M2 orientado ao reparo. Esses macrófagos exibiram mais marcadores de superfície e genes ligados à cicatrização e foram melhores em atenuar a inflamação quando transferidos para outros camundongos. Quando os cientistas removeram seletivamente os macrófagos alveolares, a lesão pulmonar piorou e a sulfátide perdeu em grande parte seu efeito protetor, mostrando que essas células são um ponto crucial na via. Importante, o benefício da sulfátide desapareceu em camundongos sem células NKT tipo II ou sem células iNKT tipo I, e pôde ser restaurado pela transferência de volta de iNKT pré-expostas à sulfátide. Juntos, esses experimentos revelaram um revezamento: a sulfátide ativa células NKT tipo II, que por sua vez remodelam o comportamento das iNKT, e estas reprogramam os macrófagos alveolares.
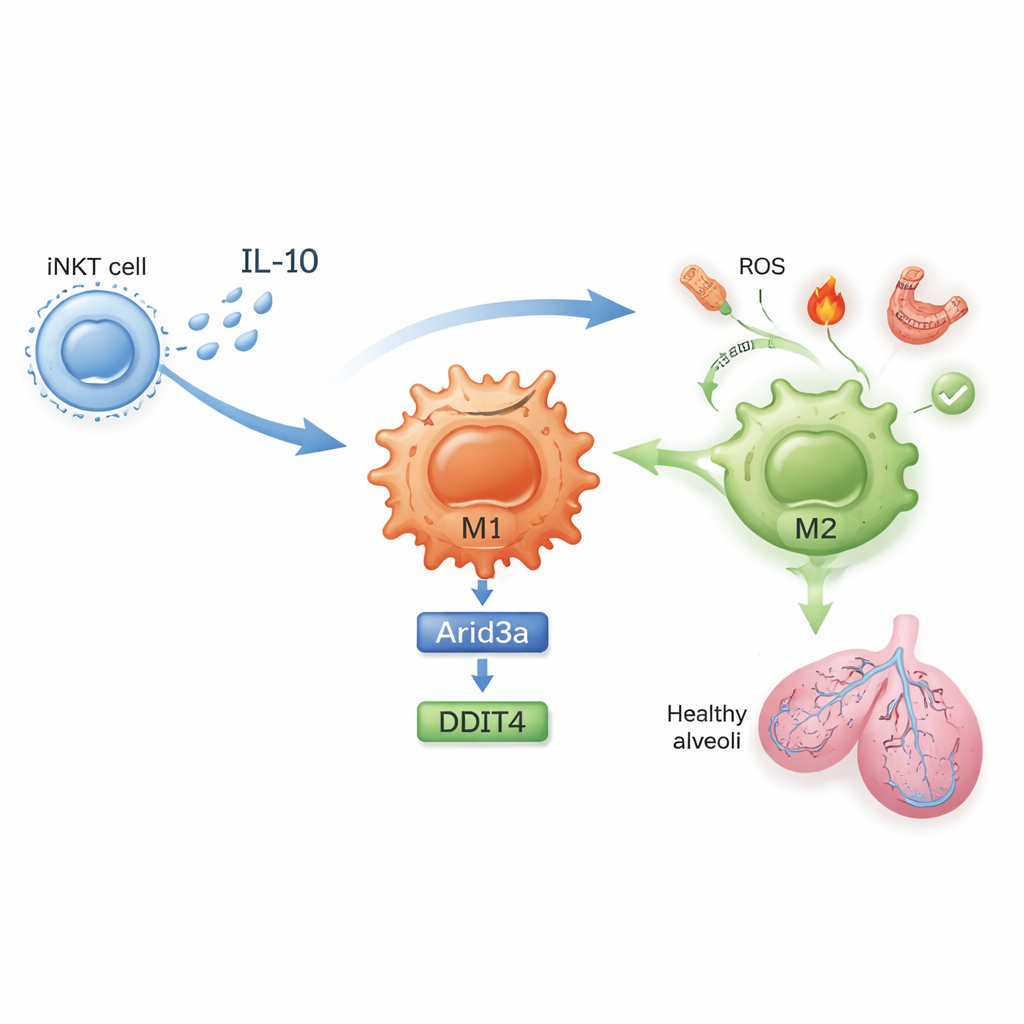
Uma cadeia molecular que acalma a inflamação
O que exatamente muda dentro dessas células? Em camundongos não tratados, as iNKT pulmonares proliferaram durante a isquemia–reperfusão e produziram altos níveis de interferon-gama, um potente sinal inflamatório. Após a exposição à sulfátide, as iNKT passaram a produzir mais interleucina‑10 (IL‑10), uma molécula anti-inflamatória poderosa, e menos interferon-gama. O estudo mostra que a IL‑10 das iNKT age diretamente sobre os macrófagos para impulsionar sua polarização para M2. Usando perfilamento de expressão gênica e experimentos cuidadosamente desenhados em cultura celular, os autores descobriram uma cadeia molecular dentro dos macrófagos: a IL‑10 aumenta um fator de transcrição chamado Arid3a, que por sua vez aumenta a expressão de um gene de resposta ao estresse chamado DDIT4. Esse eixo Arid3a–DDIT4 ajuda a desligar uma via de controle de crescimento que, de outro modo, manteria os macrófagos em um estado inflamatório, empurrando-os para o programa protetor M2.
Dos pulmões de camundongos às terapias futuras
Para testar quão central essa cadeia molecular é, os pesquisadores usaram pequenos RNAs interferentes para silenciar Arid3a ou DDIT4 nos macrófagos antes de transferi-los para camundongos. Quando qualquer um dos genes foi silenciado, a sulfátide deixou de empurrar completamente os macrófagos para o modo de reparo, e a proteção pulmonar foi enfraquecida. Análises adicionais sugerem que uma proteína de sinalização chamada YES1 ajuda as células NKT tipo II ativadas por sulfátide a reprogramar as iNKT para a produção de IL‑10. Embora essas descobertas venham de modelos em camundongos e de células manipuladas em laboratório, elas descrevem uma história clara: ao ativar brevemente um subconjunto específico de células NKT com sulfátide, pode ser possível converter respostas imunes potencialmente danosas em respostas que protejam pulmões transplantados ou lesionados. No futuro, fármacos que imitem essa via poderiam ajudar mais pacientes a sobreviver e se recuperar após procedimentos pulmonares que salvam vidas.
Citação: Li, Q., Yin, J., Lin, Q. et al. Functional remodeling of iNKT cells by sulfatide-reactive type II NKT cells reprograms alveolar macrophages to alleviate lung ischemia-reperfusion injury. Commun Biol 9, 289 (2026). https://doi.org/10.1038/s42003-026-09572-4
Palavras-chave: lesão por isquemia-reperfusão pulmonar, macrófagos alveolares, células T N natural killers, interleucina-10, modulação imune