Clear Sky Science · pt
Reavaliando a especificidade entre proteínas Gα e elementos de resposta no sinalização por GPCR
Por que pequenos interruptores celulares importam para a medicina
Muitos dos medicamentos atuais funcionam acionando “interruptores” moleculares na superfície de nossas células chamados receptores acoplados à proteína G, ou GPCRs. Esses interruptores transmitem mensagens para o interior da célula por meio de proteínas auxiliares conhecidas como proteínas G e, em última instância, ligam ou desligam genes. Durante décadas, os pesquisadores têm confiado em testes simples que produzem luz para ver quais proteínas G um determinado fármaco ou receptor está usando. Este estudo coloca uma pergunta básica, porém crítica: esses testes realmente nos dizem o que pensamos que dizem — e podemos ainda confiar neles ao projetar a próxima geração de medicamentos de precisão?
Como os cientistas normalmente interpretam os sinais de GPCR
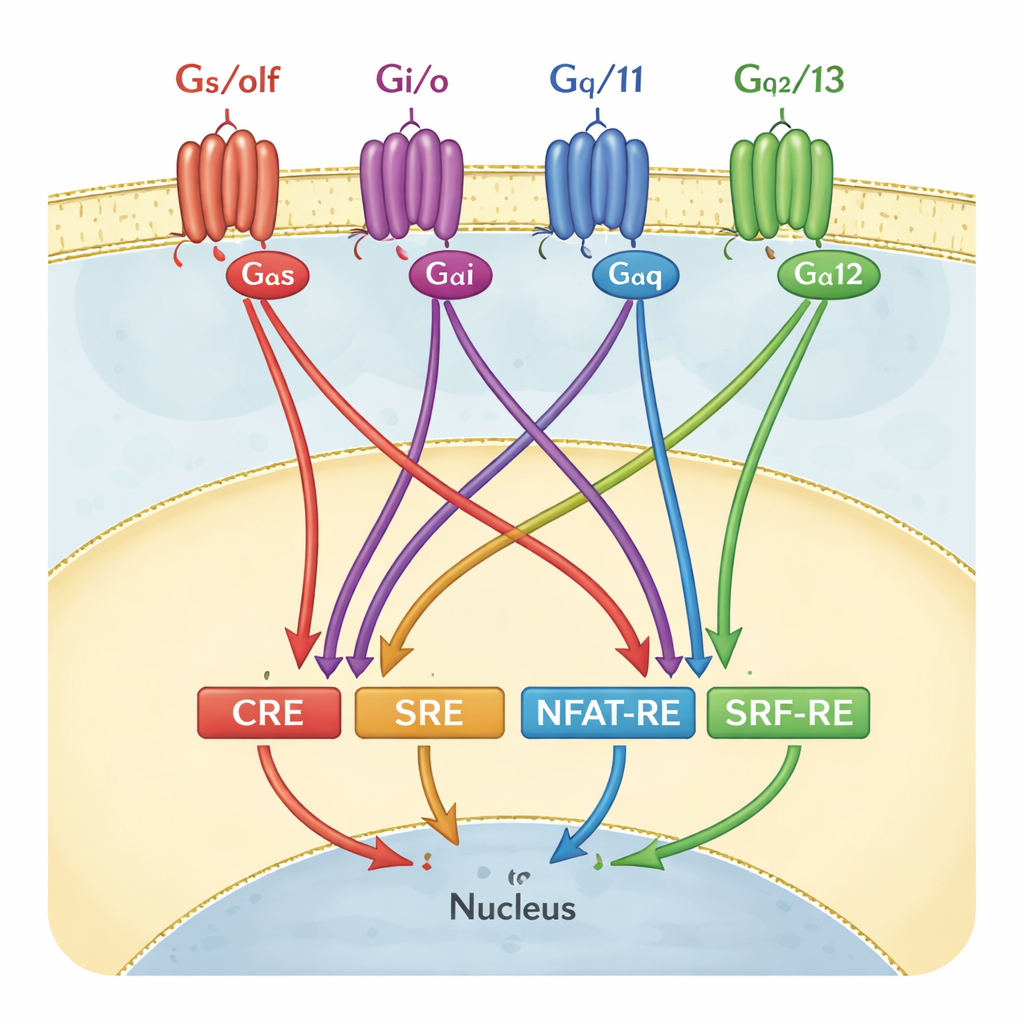
Para rastrear a atividade dos GPCRs, muitos laboratórios usam ensaios de genes repórteres. Nesses testes, as células são modificadas de modo que, quando um determinado “elemento de resposta” ou interruptor gênico é ativado, as células brilham. Quatro desses interruptores são especialmente populares: CRE, SRE, NFAT‑RE e SRF‑RE. Cada um tem sido considerado há muito tempo como representante de um ramo da sinalização por proteínas G — por exemplo, CRE para a família Gαs/olf, ou SRF‑RE para Gα12/13. Em livros e pipelines de triagem, esses pareamentos frequentemente aparecem quase como diagramas de fiação um‑a‑um: ative uma proteína G específica e apenas um repórter se acende.
Testando o antigo diagrama de fiação
Os autores desafiaram sistematicamente essa imagem usando células HEK293 humanas nas quais famílias específicas de proteínas G — ou até todas as proteínas G — foram removidas por edição genômica. Em seguida, reintroduziram tipos individuais de proteínas G, uma a uma. Nessas células expressaram nove GPCRs diferentes, escolhidos para representar receptores que sinalizam de forma muito seletiva ou por muitos parceiros de proteínas G. Medindo o brilho de cada um dos quatro repórteres em várias concentrações de fármaco, puderam ver quais proteínas G eram realmente necessárias para cada elemento de resposta e quais podiam ajudar indiretamente.
Caminhos sobrepostos em vez de canais limpos
Os resultados derrubam o modelo limpo de um receptor‑um‑repórter. Embora o CRE ainda dependesse principalmente das proteínas Gαs/olf — a via clássica que eleva o cAMP — outras famílias de proteínas G puderam influenciar notavelmente a atividade do CRE, porém apenas quando Gαs/olf estava presente. Para os outros três repórteres, SRE, NFAT‑RE e SRF‑RE, a família Gαq/11 surgiu como a grande condutora, embora SRE e SRF‑RE tenham sido tradicionalmente vinculados a outros ramos de proteínas G. SRE e SRF‑RE se comportaram de maneira especialmente semelhante, sugerindo que acessam maquinarias downstream compartilhadas em vez de rotas distintas e isoladas. Em muitos casos, proteínas G adicionais, como Gα12/13 e Gαi/o, forneceram impulso extra ou atividade de base, destacando uma teia de entrelaçamento em vez de canais separados.
Por que a rede celular borrra nossas leituras
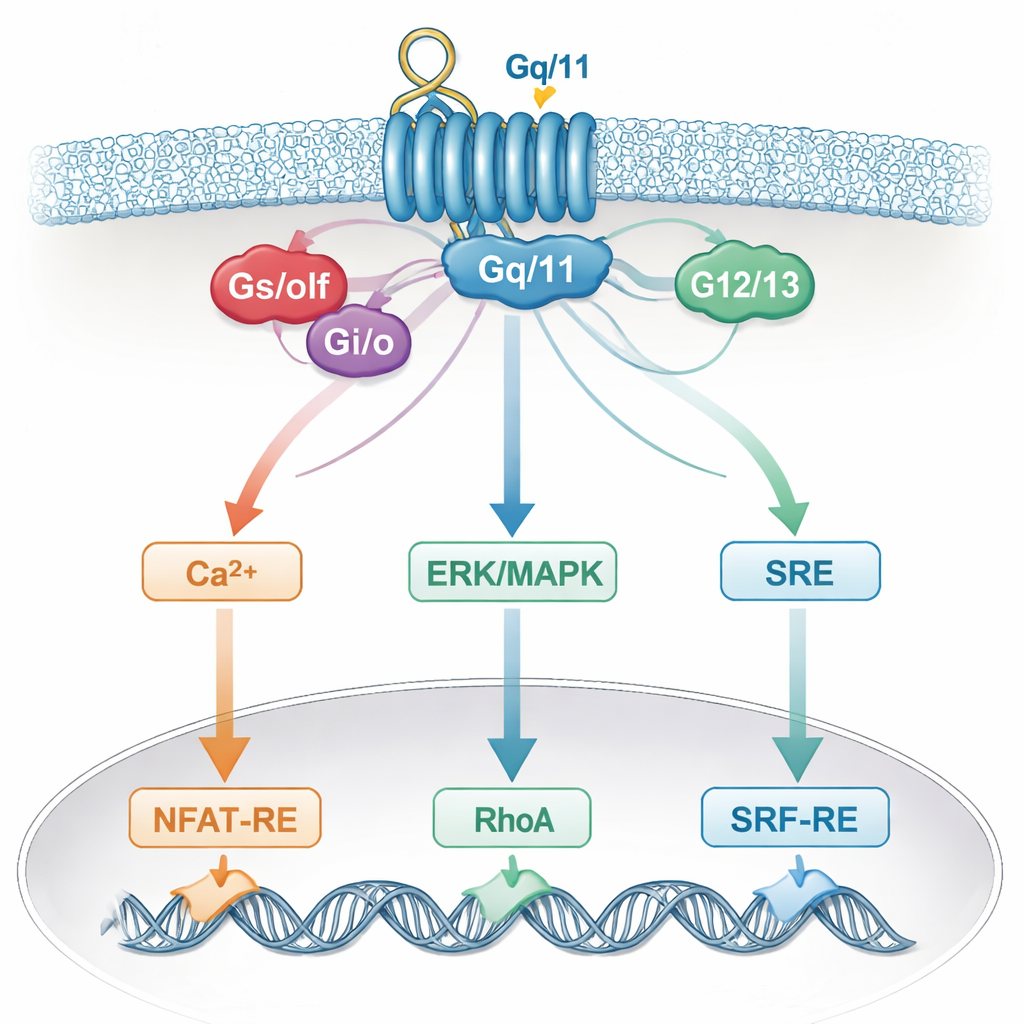
Essa especificidade borrada provavelmente reflete como células reais integram sinais. Um único receptor pode ativar múltiplas proteínas G, que então convergem em mensageiros comuns como cálcio, ERK/MAPK, RhoA ou cAMP, e em auxiliares compartilhados como subunidades Gβγ. Essas vias compartilhadas, por sua vez, alimentam os mesmos interruptores gênicos no núcleo. Como resultado, um repórter que se pensava responder a uma família de proteínas G na verdade “ouve” várias. Fatores específicos do tipo celular e o conjunto exato de receptores presentes acrescentam ainda mais complexidade, o que significa que conclusões tiradas de um sistema celular podem não valer em outro.
O que isso significa para a descoberta de fármacos
Para não especialistas, a conclusão principal é que muitos ensaios baseados em brilho amplamente usados para GPCRs são menos específicos do que seus rótulos sugerem. Eles ainda podem indicar que um receptor está ativo e, de modo aproximado, quais vias amplas estão envolvidas, mas não são prova confiável de que uma família particular de proteínas G — e apenas essa família — esteja envolvida. Os autores argumentam que pesquisadores e desenvolvedores de fármacos devem tratar esses repórteres como indicadores grosseiros e associá‑los a métodos mais diretos que observem proteínas interagindo em tempo real. Fazer isso dará uma imagem mais fiel de como potenciais medicamentos orientam a sinalização celular e ajudará a evitar atalhos enganadores na busca por terapias mais seguras e mais direcionadas.
Citação: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
Palavras-chave: Sinalização por GPCR, Proteínas G, ensaios repórter, redes de sinalização celular, descoberta de fármacos