Clear Sky Science · pt
Ensaios celulares e isoformes-seletivos de quinases acopladas a proteínas G para avaliação abrangente de inibidores
Por que reduzir os “botões de volume” celulares importa
Muitos dos nossos medicamentos atuam ajustando para cima ou para baixo a atividade de receptores na superfície celular que detectam hormônios, neurotransmissores e fármacos. Esses receptores precisam ser cuidadosamente desligados novamente para que as células não fiquem superestimuladas — um processo controlado em parte por enzimas chamadas GRKs. Quando as GRKs estão hiperativas, como observado na insuficiência cardíaca e em alguns cânceres, a sinalização se desregula. Este estudo desenvolve testes celulares práticos para medir quão bem moléculas experimentais conseguem bloquear GRKs específicas, ajudando cientistas a projetarem fármacos mais inteligentes que afinam esses cruciais botões de volume celulares.
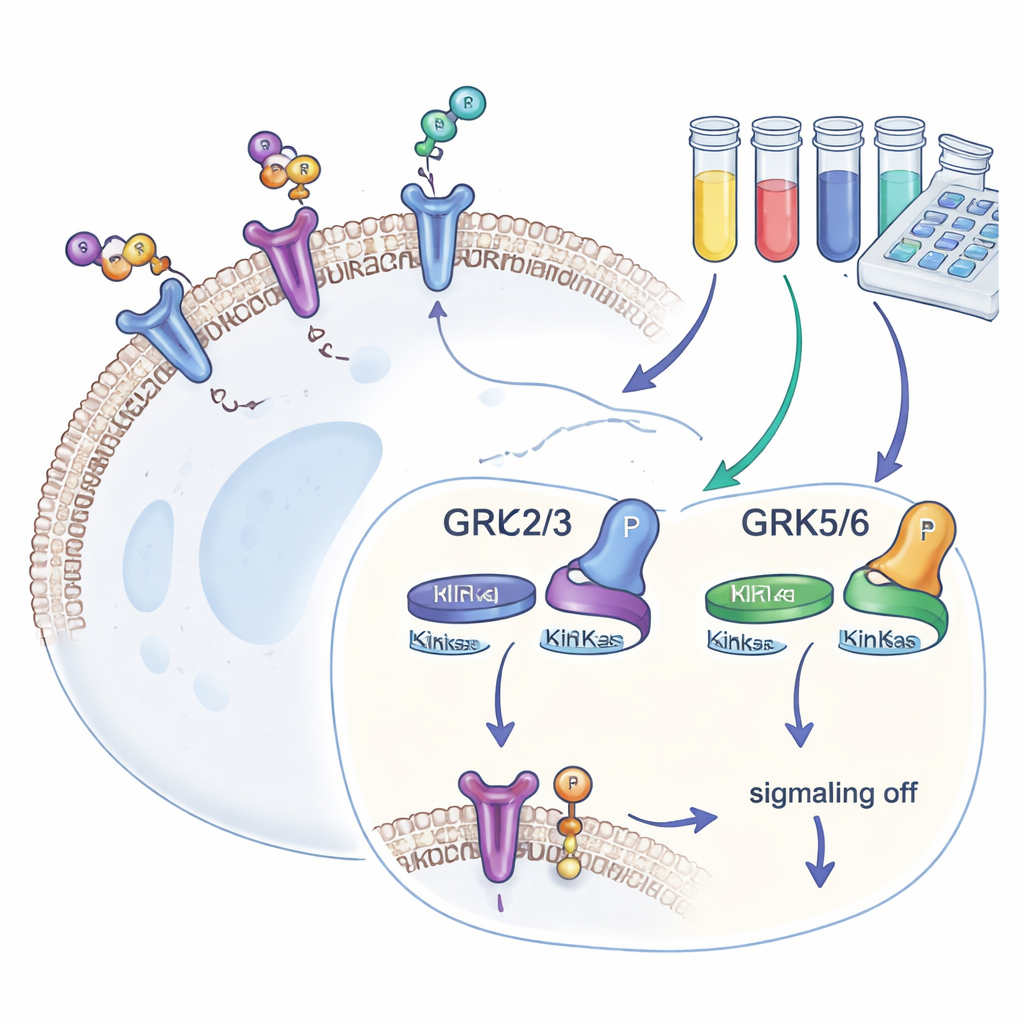
Cerqueiros na superfície celular
Nossas células exibem centenas de tipos de receptores acoplados à proteína G (GPCRs), que detectam sinais externos e os traduzem em respostas internas. Depois que um GPCR é ativado, as GRKs adicionam pequenas “bandeiras” de fosfato à sua cauda. Essas bandeiras atraem outra proteína, a beta-arrestina, que interrompe a sinalização e frequentemente internaliza o receptor. Quatro variantes de GRK — GRK2, GRK3, GRK5 e GRK6 — são encontradas em muitos tecidos. Como elas moldam a intensidade da resposta dos GPCRs e têm níveis alterados em doenças como insuficiência cardíaca, câncer e dependência, desenvolvedores de fármacos buscam bloqueadores de GRK que sejam ao mesmo tempo potentes e seletivos.
Construindo um campo de testes limpo dentro das células
A maior parte dos estudos anteriores sobre GRK baseou-se em modelagem computacional ou química em tubo de ensaio, que mostram quão bem um inibidor se liga, mas não como ele atua no interior congestionado de uma célula viva. Para preencher essa lacuna, os autores engenheiraram células humanas HEK293 que não possuem as quatro GRKs comuns e então reintroduziram apenas uma isoforma de GRK por vez. Cada linha celular também expressava um receptor bem estudado, o receptor beta-2 adrenérgico, marcado de modo que sua fosforilação em um sítio específico da cauda (chamado T360/S364) pudesse ser detectada por um ensaio sensível baseado em anticorpos. Como esse sítio é modificado apenas por GRKs, a quantidade de fosfato presente serve como uma medida direta e quantitativa da atividade de cada isoforma de GRK dentro de células vivas.
Separando os bons, os fracos e os não específicos
Com esse conjunto de ferramentas, a equipe testou um painel de inibidores de GRK comercialmente disponíveis. Primeiro agruparam compostos que miram principalmente GRK2 e GRK3, e outro conjunto direcionado a GRK5 e GRK6. Ao comparar quanto cada molécula reduzia a fosforilação do receptor em células que expressavam apenas um subtipo de GRK, puderam mapear a seletividade no contexto celular real. Um composto, chamado 8h, destacou-se como o bloqueador mais potente de GRK2/3, enquanto o composto 18 se sobressaiu por inibir seletivamente GRK5/6. Algumas moléculas amplamente usadas mostraram pouco efeito nas doses testadas, provavelmente porque não penetraram bem nas células, e um inibidor covalente muito potente prejudicou a saúde celular, tornando-o inadequado para experimentos de imageamento.
De impressões químicas ao comportamento do receptor
Para demonstrar que esses inibidores afetam não apenas um receptor-teste, mas a biologia dos GPCRs de forma mais ampla, os autores examinaram vários receptores de importância médica, incluindo o receptor mu-opioide e o receptor de vasopressina V2. Mediram tanto a fosforilação quanto a internalização dos receptores por microscopia. O composto 8h ou 18 isoladamente reduziu parcialmente a fosforilação e o movimento interno dos receptores em muitos alvos, mas a combinação de 8h e 18 quase completamente previniu essas alterações e manteve os receptores na superfície celular. Experimentos adicionais acompanhando o recrutamento de beta-arrestina confirmaram que os mesmos compostos podem modular a sinalização em outros receptores regulados por conjuntos sobrepostos de GRKs.
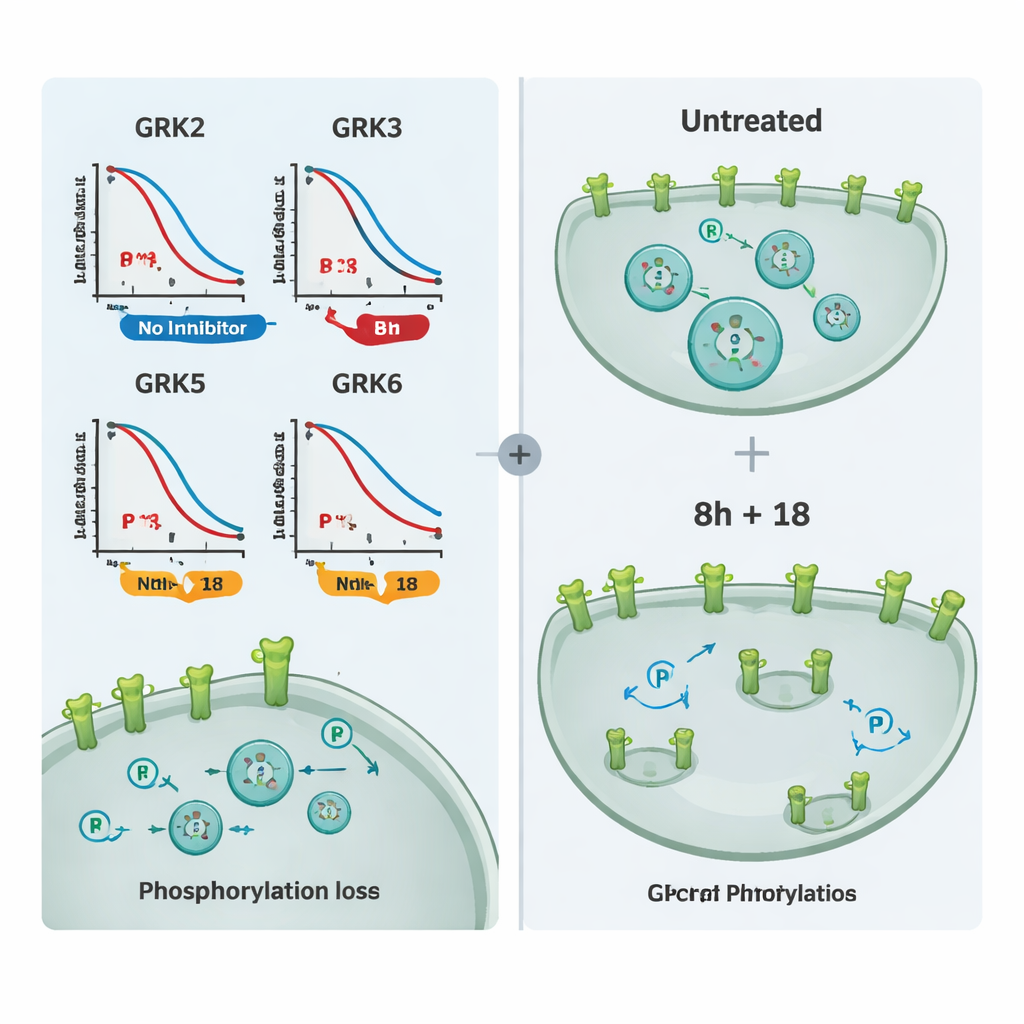
O que isso significa para futuros medicamentos
Para não especialistas, a mensagem principal é que o estudo entrega um conjunto confiável de ensaios celulares — e dois compostos-ferramenta especialmente úteis, 8h e 18 — que permitem aos pesquisadores ver, em células vivas, exatamente como diferentes isoformas de GRK são atenuadas. Em vez de inferir a partir de dados simplificados de tubo de ensaio, os cientistas podem agora comparar candidatos lado a lado e decidir se eles afetam principalmente GRK2/3, GRK5/6 ou as quatro simultaneamente. Essa clareza deve acelerar o desenvolvimento de fármacos que modulam com mais precisão a sinalização por GPCR, com benefícios potenciais no tratamento de doenças cardíacas, câncer, distúrbios de dor e outras condições em que o equilíbrio da sinalização foi comprometido.
Citação: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
Palavras-chave: Sinalização GPCR, Inibidores de GRK, Receptor beta-adrenérgico, ensaio celular, descoberta de fármacos