Clear Sky Science · pt
HBP1 potencializa a atividade do receptor de progesterona e a expressão de IGFBP1 promovendo a decidualização endometrial
Por que isso importa para a fertilidade
Quando uma gravidez começa, o embrião só pode se alojar no útero se o revestimento uterino passar por uma transformação crucial chamada decidualização. Muitos casos de infertilidade e falhas repetidas na transferência de embriões permanecem sem explicação, e evidências crescentes sugerem que o problema está nessa transformação, e não no embrião em si. Este estudo revela um “interruptor” molecular antes subestimado — um fator de transcrição chamado HBP1 — que ajuda a preparar o revestimento uterino para a implantação e pode oferecer novas maneiras de diagnosticar e tratar problemas de implantação.
Um interruptor escondido no revestimento uterino
O revestimento interno do útero, o endométrio, muda ritmicamente a cada ciclo menstrual. Sob a influência do estrogênio ele cresce, e sob a progesterona ele amadurece em um leito receptivo para o embrião. Neste trabalho, os pesquisadores focaram nas células estromais endometriais humanas, as células estruturais que se transformam em células deciduais maiores e mais secretoras no momento da implantação. Ao minerar dados existentes de atividade gênica e realizar novos experimentos, eles descobriram que os níveis de HBP1 aumentam fortemente quando essas células estromais começam a decidualizar, sugerindo que HBP1 faz parte do sistema de tempo incorporado que prepara o útero.
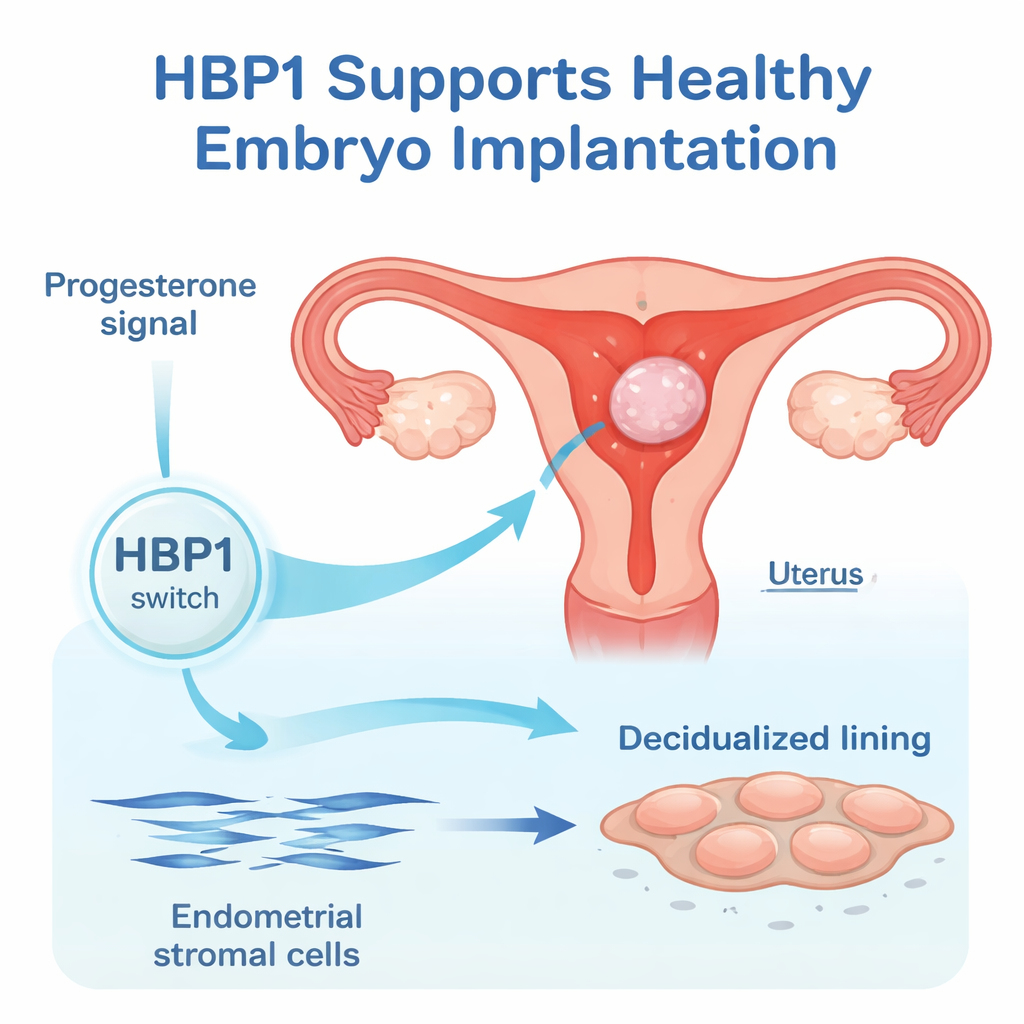
Auxiliando as células a mudar de forma e desacelerar
Para testar se HBP1 está apenas presente ou realmente necessário, a equipe modulou seus níveis para cima e para baixo em células estromais endometriais humanas em cultura. Quando HBP1 foi reduzido, marcadores clássicos de decidualização como IGFBP1, FOXO1 e prolactina diminuíram tanto no RNA quanto no nível proteico. As células também não passaram pela mudança típica de forma — de células delgadas e fusiformes para formas mais largas e poligonais — e, em vez disso, continuaram proliferando. Quando HBP1 foi aumentado, os níveis de IGFBP1 subiram e a divisão celular diminuiu. Juntos, esses achados mostram que HBP1 ajuda as células a sair do modo de crescimento e entrar no estado decidual especializado que sustenta a gravidez inicial.
Ajustando finamente os sinais hormonais dentro da célula
A progesterona e seu receptor são centrais para preparar o útero, mas nem todos os tecidos respondem igualmente ao hormônio. Os pesquisadores descobriram que a sinalização da progesterona por si só aumenta os níveis de HBP1, criando um circuito de feedback positivo. Surpreendentemente, reduzir HBP1 não alterou quanto receptor de progesterona as células produziam, mas atenuou a atividade de genes importantes responsivos à progesterona, incluindo FKBP4, FKBP5, FOSL2 e o coativador SRC1. Usando abordagens genômicas amplas, eles mostraram que HBP1 se liga próximo a muitos desses genes e está associado a um aumento de uma marca específica de histona, H3K4me3, que sinaliza DNA ativo. Em essência, HBP1 não liga ou desliga o receptor; ele facilita a leitura dos genes-alvo do receptor.
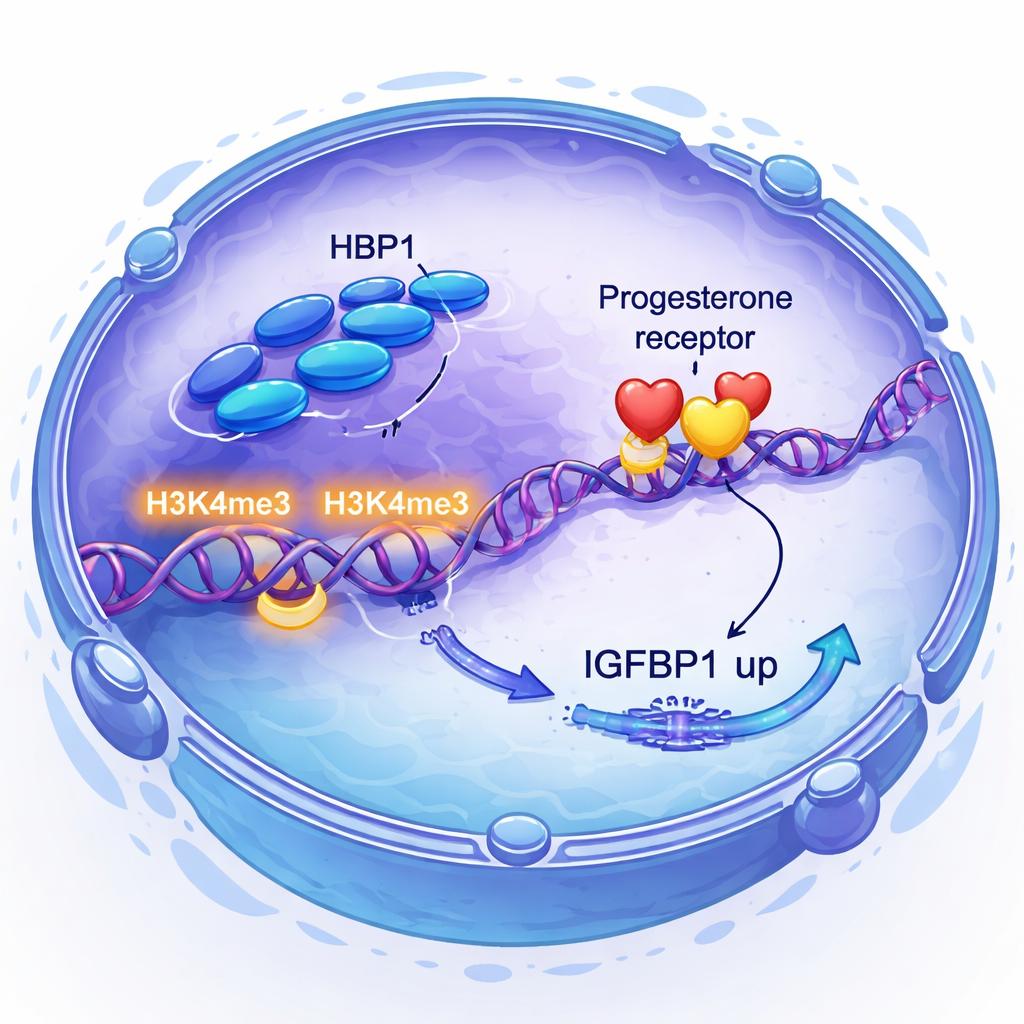
Controle direto de um sinal-chave de implantação
A equipe então investigou como HBP1 se conecta ao IGFBP1, uma proteína há muito usada como marcador de decidualização saudável e conhecida por influenciar a comunicação embrião–útero. Ao combinar sequenciamento de RNA com sequenciamento de imunoprecipitação da cromatina, eles mostraram que HBP1 se posiciona diretamente na região promotora de IGFBP1 e aumenta H3K4me3 ali, impulsionando maior produção de IGFBP1. Também descobriram que reduzir HBP1 ativava a via PI3K–AKT, um sinal relacionado ao crescimento que, quando hiperativo, suprimia IGFBP1. Bloquear essa via resgatou os níveis de IGFBP1. Assim, HBP1 sustenta a decidualização de duas maneiras: ativando diretamente IGFBP1 e atenuando um sinal de crescimento que, de outra forma, impediria a expressão dos genes deciduais.
Ligando um defeito molecular à falha de implantação
Por fim, os pesquisadores analisaram amostras endometriais de mulheres com falha recorrente de implantação e as compararam com tecidos de controles férteis durante a fase secretora média, pronta para implantação. Mulheres com falhas repetidas apresentaram níveis notavelmente mais baixos de HBP1 e de seus parceiros a jusante IGFBP1, FKBP5 e FOSL2, embora os níveis do receptor de progesterona fossem semelhantes entre os grupos. Esse padrão se encaixa na ideia de “resistência à progesterona” — o hormônio está presente, mas o tecido não consegue montar uma resposta completa porque fatores de suporte chave como HBP1 estão ausentes.
O que isso significa para pacientes
De forma acessível, este estudo sugere que HBP1 age como uma configuração mestre no painel de controle do revestimento uterino. Quando ajustado corretamente, ele ajuda as sinalizações de progesterona a serem ouvidas, incentiva as células a parar de se dividir e a se especializar, e aumenta a produção de moléculas favoráveis à implantação, como IGFBP1. Quando HBP1 está baixo demais, o revestimento pode parecer normal ao microscópio, mas funcionar mal, levando a embriões que simplesmente não conseguem se firmar. Entender e medir HBP1 e sua rede pode, no futuro, ajudar médicos a identificar mulheres em risco de problemas de implantação e inspirar novos tratamentos que restaurem a receptividade do útero.
Citação: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
Palavras-chave: decidualização endometrial, implantação do embrião, sinalização de progesterona, infertilidade, HBP1