Clear Sky Science · pt
Dinamicamente distintas da GABA entre redes funcionais do cérebro no autismo
Por que este estudo cerebral é importante
Muitas pessoas no espectro autista descrevem o mundo como avassalador, com sons, luzes e emoções parecendo excessivamente intensos ou estranhamente amortecidos. Cientistas suspeitam que parte da razão reside em como as células cerebrais equilibram sinais de “avançar” e “frear”. Este estudo examina um químico chave de “freio”, a GABA, e faz uma pergunta prática: como o cérebro autista responde quando mexemos nesse sistema com um medicamento? A resposta pode ajudar a explicar por que alguns fármacos funcionam de forma imprevisível no autismo e por que acertar a dose é tão desafiador.
Sinais que mantêm o equilíbrio da atividade cerebral
Nossos cérebros funcionam numa constante disputa entre excitação (neurônios disparando) e inibição (neurônios acalmando a atividade). A GABA é o principal químico que fornece essa função de freio. No autismo, anos de pesquisa sugerem que esse equilíbrio está alterado, especialmente em sistemas cerebrais que processam informação sensorial como visão, audição e tato. Mas a maior parte dos trabalhos anteriores foi estática: medir química ou estrutura cerebral em repouso e comparar pessoas autistas e não autistas. O que faltava era um teste dinâmico de como o sistema GABA realmente responde quando é desafiado por um medicamento, especialmente através das redes em larga escala que sustentam sensação, movimento, atenção e emoção.
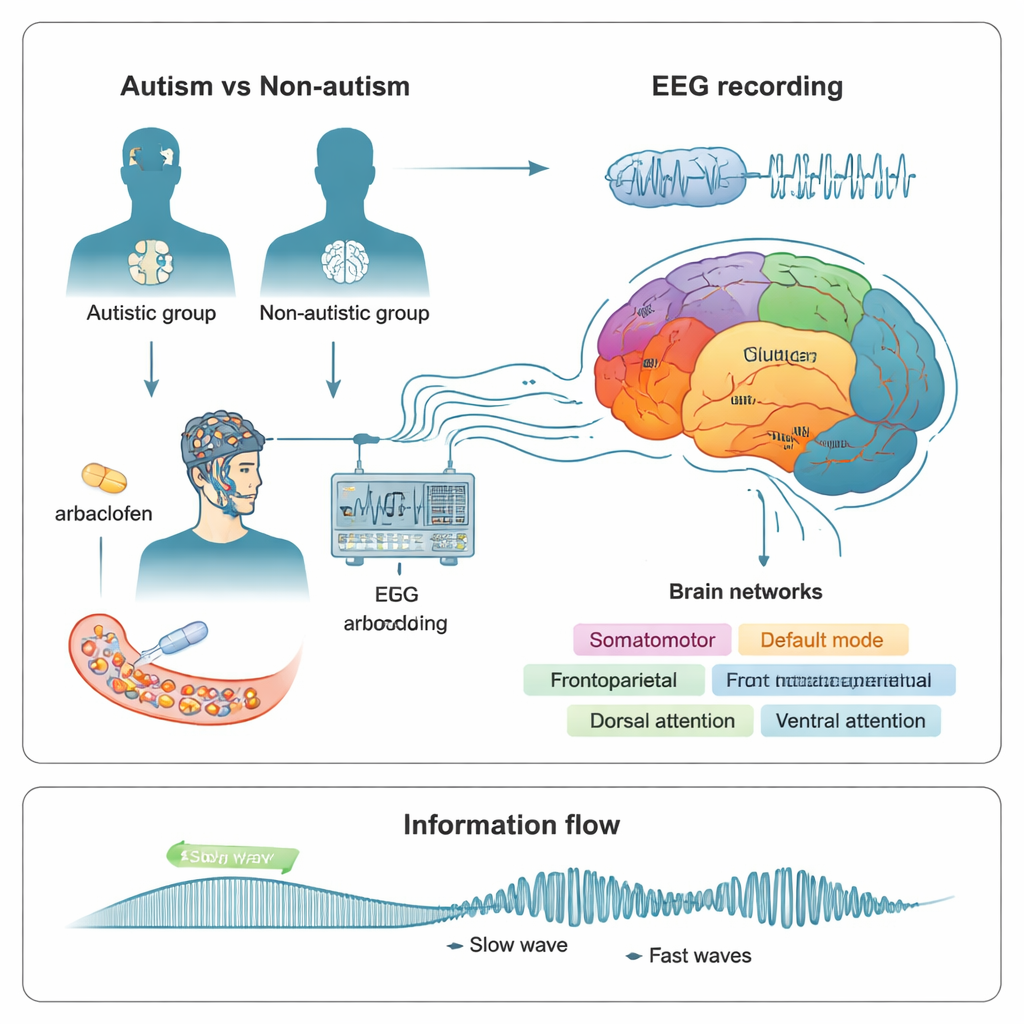
Ouvindo os ritmos cerebrais
Para investigar isso, os pesquisadores registraram a atividade cerebral em repouso usando EEG, que mede sinais elétricos minúsculos no couro cabeludo. Estudaram 24 adultos não autistas e 15 adultos autistas ao longo de várias visitas. A cada vez, os participantes ingeriam um placebo ou uma de duas doses (15 mg ou 30 mg) de arbaclofen, um medicamento que ativa um tipo específico de receptor GABA chamado GABAB. Cerca de três horas depois, quando o fármaco estava ativo, a equipe registrou EEG com olhos abertos e fechados e usou modelos computacionais para rastrear os sinais até 400 locais no córtex. Esses locais foram então agrupados em sete grandes redes funcionais, incluindo visual, somatomotora (movimento e tato), límbica (emoção e memória) e várias redes de ordem superior envolvidas em pensamento e atenção.
Como ondas lentas e rápidas conversam
Em vez de olhar apenas para a força de certas ondas cerebrais, a equipe concentrou-se em como diferentes frequências interagem. Em cérebros saudáveis, ondas lentas que abrangem grandes regiões frequentemente ajudam a coordenar explosões de atividade mais rápidas e locais. Essa interação, chamada acoplamento fase–amplitude, pode ser vista como um ritmo lento abrindo e fechando “janelas” nas quais a atividade rápida é mais provável. Os autores mediram quão fortemente ritmos lentos em faixas como teta e alfa estavam sincronizados com atividade mais rápida em beta e gama, tanto dentro quanto entre as sete redes. Um acoplamento mais forte pode ser útil em certos contextos, mas se ficar excessivamente rígido ou inflexível pode indicar um desequilíbrio na forma como a informação flui pelo cérebro.
Cérebros autistas exibem acoplamento mais forte em repouso
Sob placebo, os participantes autistas apresentaram consistentemente acoplamento mais alto entre ritmos teta e beta através da maioria das redes cerebrais quando os olhos estavam fechados, em comparação com os voluntários não autistas. O sistema límbico se destacou: ali, todas as quatro medidas de acoplamento examinadas pela equipe estavam elevadas, sugerindo ligações incomumente fortes entre ritmos lentos e amplos e atividade rápida local em regiões envolvidas em emoção e memória. A rede somatomotora também mostrou aumento no acoplamento entre teta e gama. Esses padrões reforçam a ideia de que o equilíbrio excitação–inibição está alterado ao nível dos ritmos cerebrais dinâmicos no autismo, especialmente em redes sensoriais e emocionais.
A dose importa — e diferentes redes se comportam de modos distintos
Quando os pesquisadores administraram arbaclofen, o quadro tornou-se mais complexo e dependente da dose. Nos participantes autistas, a dose mais alta de 30 mg deslocou o acoplamento elevado teta–beta nas redes visual e somatomotora em direção à faixa observada nos não autistas, sugerindo um padrão mais típico de fluxo de informação sensorial. No entanto, redes de ordem superior que sustentam planejamento, pensamento autorreferencial e atenção mudaram muito pouco. O sistema límbico comportou-se de forma diferente novamente: uma dose baixa de 15 mg aproximou seu acoplamento exagerado — tanto dentro da rede quanto em suas conexões com outras redes — dos níveis de controle. Mas com 30 mg, muitas dessas anomalias reapareceram, e conexões límbicas atípicas com outras redes, como a somatomotora, ressurgiram. Em outras palavras, alguns circuitos emocionais pareciam responder melhor a uma dose menor e poderiam ser excessivamente estimulados em doses mais altas.
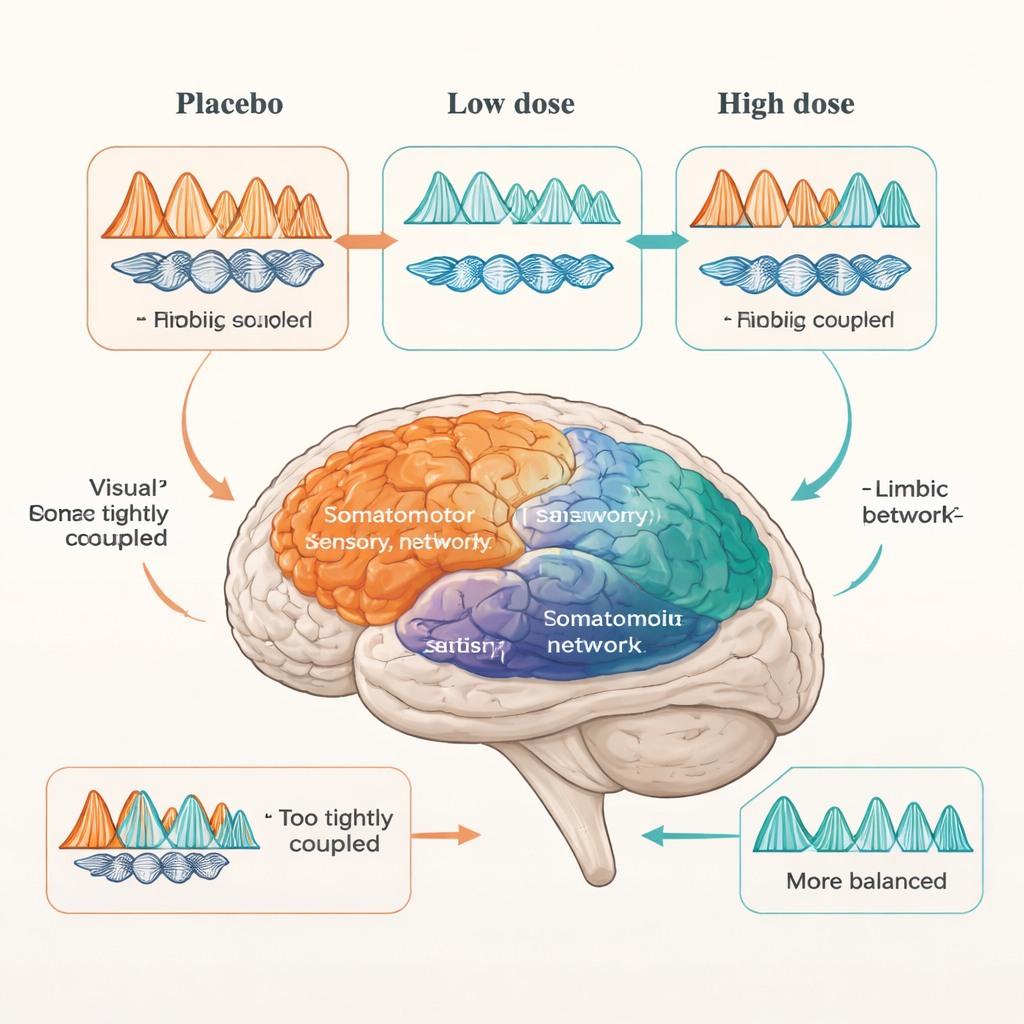
O que isso significa para tratamentos no mundo real
Para um público leigo, a mensagem principal é que o cérebro autista não responde a drogas que agem na GABA de maneira simples e uniforme. Diferentes redes cerebrais — sensoriais, emocionais e de ordem superior — exibem padrões distintos de sensibilidade, e alguns circuitos são especialmente sensíveis à dose. Isso ajuda a explicar por que medicamentos que miram a inibição podem às vezes ter efeitos paradoxais ou mistos no autismo, ajudando em um domínio enquanto atrapalham outro. Embora este estudo não avalie se o arbaclofen melhora sintomas do dia a dia, ele mostra que doses escolhidas com cuidado podem ajustar certas redes cerebrais autistas rumo a um equilíbrio de atividade mais típico. Trabalhos futuros podem usar esse tipo de “teste de estresse” baseado no cérebro para personalizar tratamentos, com o objetivo de restaurar uma comunicação mais flexível e melhor ajustada entre as redes cerebrais.
Citação: Huang, Q., Chen, D., Pereira, A.C. et al. Differential GABA dynamics across brain functional networks in autism. Commun Biol 9, 283 (2026). https://doi.org/10.1038/s42003-026-09563-5
Palavras-chave: autismo, GABA, redes cerebrais, EEG, arbaclofen