Clear Sky Science · pt
O metabólito intestinal ácido indol‑3‑acético agrava o lúpus neuropsiquiátrico via a via AHR/STAT3 em micróglias
Como germes intestinais podem afetar a mente
Pessoas com lúpus, uma doença autoimune, às vezes desenvolvem problemas sérios de pensamento, humor e memória — uma condição chamada lúpus neuropsiquiátrico. Esses sintomas cerebrais podem ser incapacitantes, mas os médicos ainda têm dificuldade em explicar exatamente por que ocorrem ou como tratá‑los. Este estudo explora um culpado inesperado: certas bactérias intestinais e os compostos que produzem, que podem viajar do intestino ao cérebro e alimentar a inflamação lá.
Dos micróbios intestinais ao comportamento perturbado
Os pesquisadores começaram perguntando se os micróbios intestinais de pacientes com lúpus neuropsiquiátrico diferem em seus efeitos daqueles de pacientes com lúpus sem sintomas cerebrais. Eles transferiram bactérias fecais de cada grupo de pacientes para camundongos saudáveis que, previamente, tiveram seus próprios micróbios intestinais eliminados. Camundongos que receberam micróbios de pacientes com lúpus neuropsiquiátrico desenvolveram mais comportamentos semelhantes à ansiedade, sinais de depressão e problemas de aprendizagem e memória do que camundongos que receberam micróbios de outros pacientes com lúpus. Seus cérebros mostraram maior ativação das micróglias — as células imunes do cérebro — e níveis mais altos de moléculas inflamatórias. O selo protetor ao redor do cérebro, conhecido como barreira hematoencefálica, também estava mais permeável nesses animais, sugerindo que algo na microbiota transplantada estava danificando essa barreira crítica.
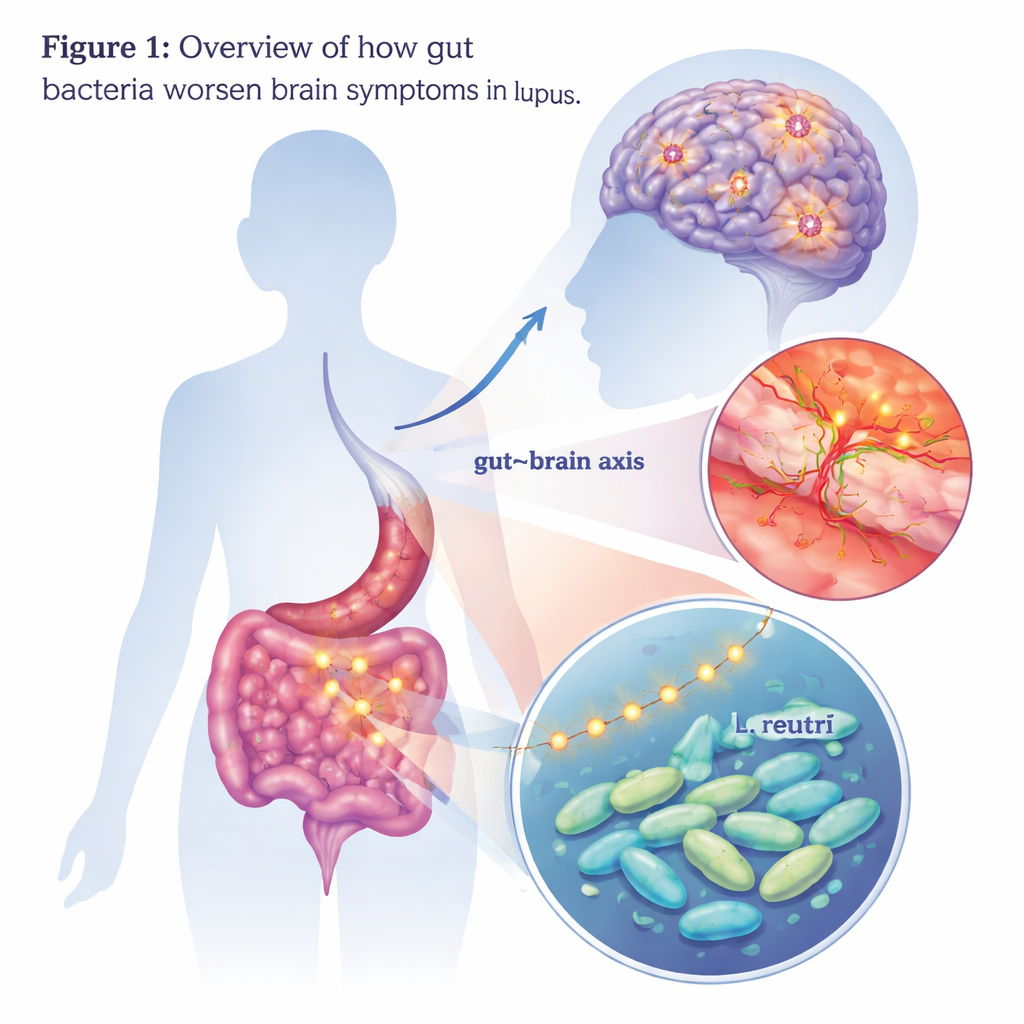
Focalizando em uma única bactéria
Para identificar quais micróbios poderiam ser responsáveis, a equipe comparou as comunidades bacterianas intestinais de pacientes e camundongos. Um grupo se destacou: Lactobacillus, e em especial uma espécie chamada Lactobacillus reuteri, estava mais abundante em pacientes com lúpus neuropsiquiátrico e em camundongos que apresentaram alterações cerebrais. Quando os cientistas alimentaram apenas L. reuteri em camundongos predispostos ao lúpus, os animais desenvolveram comportamentos mais intensos de ansiedade e depressão e foram piores em testes de memória. Seus cérebros exibiram micróglias mais ativadas, maior perda de neurônios e maior comprometimento da barreira hematoencefálica. Esses achados sugerem que, ao menos no contexto do lúpus, essa bactéria normalmente associada a efeitos probióticos pode assumir um papel mais prejudicial.
Uma pequena molécula com grandes efeitos
L. reuteri é conhecida por produzir um composto chamado ácido indol‑3‑acético (IAA) a partir do triptofano dietético. Usando testes químicos sensíveis, a equipe encontrou níveis mais altos de IAA nas fezes de pacientes com lúpus neuropsiquiátrico do que em outros pacientes com lúpus, e confirmaram que culturas de L. reuteri produzem muito mais IAA do que bactérias intestinais comuns, como Escherichia coli. Em pacientes com lúpus neuropsiquiátrico, os níveis de IAA no líquido que envolve o cérebro e a medula espinhal correlacionaram‑se com níveis mais elevados de citocinas inflamatórias, sugerindo que essa molécula pode alcançar o sistema nervoso central e provocar inflamação. Em camundongos predispostos ao lúpus, alimentar com L. reuteri aumentou os níveis de IAA no intestino, no sangue e no cérebro. Administrar apenas IAA a esses camundongos reproduziu muitas das mesmas alterações: comportamentos anormais, ativação microglial, sinais inflamatórios mais altos e enfraquecimento da barreira hematoencefálica e da barreira intestinal.
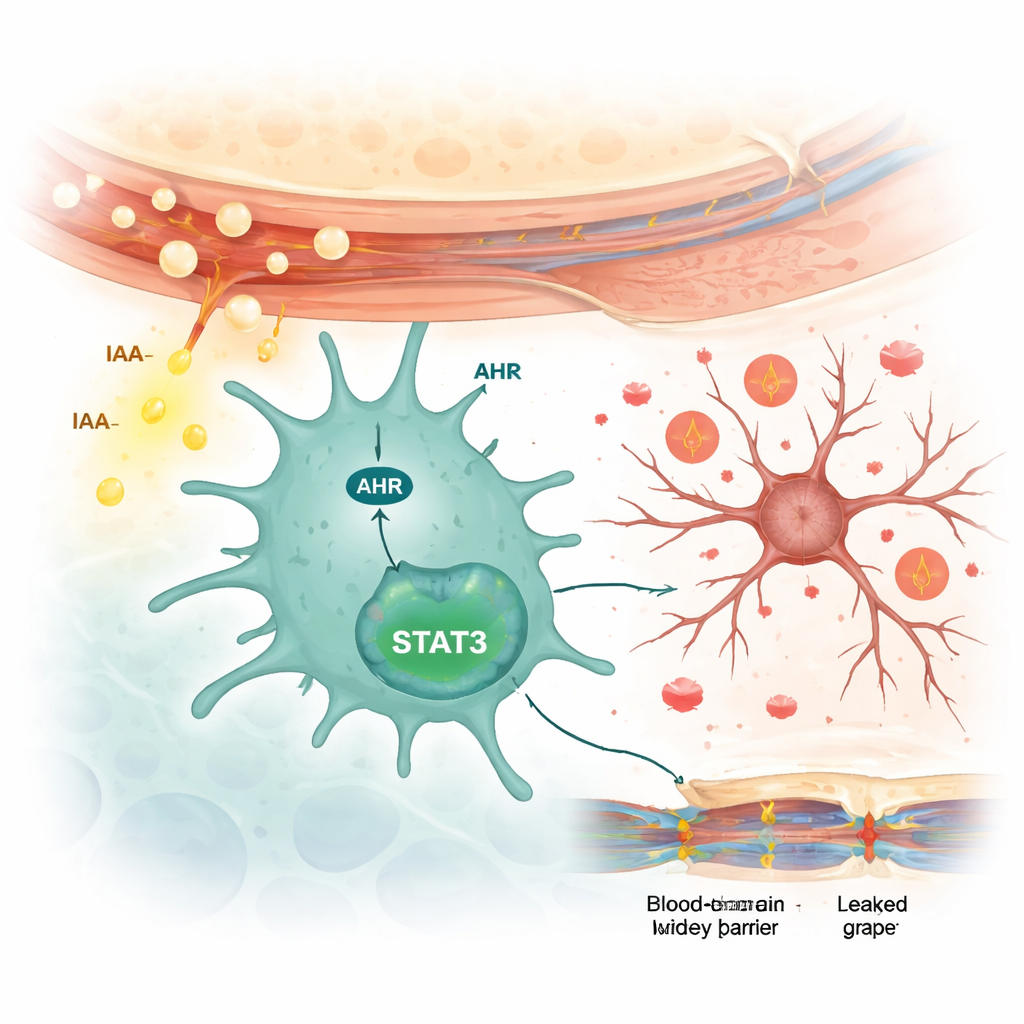
Como as células imunes do cérebro são ativadas
Os cientistas então examinaram como o IAA se comunica com as células cerebrais. Eles descobriram que o IAA aumentou a atividade de uma proteína sensora chamada receptor de hidrocarboneto arílico (AHR) especificamente nas micróglias, não nos neurônios nem nas células estreladas de suporte chamadas astrócitos. Em micróglias em cultura, o IAA elevou os níveis de AHR e ativou uma proteína de sinalização a jusante chamada STAT3, que por sua vez impulsionou a produção de citocinas inflamatórias. Bloquear o AHR com um fármaco impediu a ativação da STAT3 e reduziu a liberação desses sinais inflamatórios. Quando camundongos predispostos ao lúpus foram tratados com o fármaco bloqueador de AHR, seus comportamentos de ansiedade e depressão melhoraram, a ativação microglial diminuiu, as moléculas inflamatórias caíram e a barreira hematoencefálica ficou menos permeável.
O que isso significa para os pacientes
No conjunto, o estudo descreve uma cadeia de eventos que liga o intestino ao cérebro no lúpus neuropsiquiátrico. Uma superabundância de L. reuteri no intestino produz IAA em excesso, que enfraquece a barreira intestinal e entra na corrente sanguínea. O IAA então alcança o cérebro, onde ativa o AHR e a sinalização STAT3 nas micróglias, desencadeando inflamação que danifica neurônios e afrouxa a barreira hematoencefálica. Para os pacientes, esses achados sugerem que alterar as bactérias intestinais, reduzir metabólitos nocivos como o IAA ou bloquear a via AHR/STAT3 em micróglias pode, um dia, ajudar a proteger o cérebro dos efeitos devastadores do lúpus neuropsiquiátrico.
Citação: Feng, Y., Zheng, L., Tang, W. et al. Gut metabolite indole-3-acetic acid aggravates neuropsychiatric lupus via the AHR/STAT3 pathway in microglia. Commun Biol 9, 281 (2026). https://doi.org/10.1038/s42003-026-09561-7
Palavras-chave: lúpus neuropsiquiátrico, microbiota intestinal, Lactobacillus reuteri, inflamação microglial