Clear Sky Science · pt
Terapia dinâmica estimulada por radionuclídeos induz necroptose imunogênica e apoptose complementares como vias de morte de células cancerosas
Virando as astúcias do câncer contra ele mesmo
O câncer é notório por escapar dos nossos melhores tratamentos, especialmente em tumores agressivos de mama que se espalham pelo corpo. Este estudo explora uma abordagem inventiva chamada terapia dinâmica estimulada por radionuclídeos (RaST), que usa traçadores de imagem médicos e nanopartículas ativadas por luz para matar células cancerosas de maneiras que também despertam o sistema imunológico. Para os leitores, este trabalho é importante porque sugere como ferramentas de imagem existentes e materiais inteligentes podem ser reaproveitados para gerar um controle do câncer mais duradouro e impulsionado pela imunidade, em vez de apenas uma redução temporária do tumor.
Uma nova maneira de iluminar tumores de dentro
Os tratamentos convencionais baseados em luz funcionam apenas onde um feixe externo pode alcançar, como na pele ou em tumores superficiais. A RaST contorna essa limitação usando um açúcar radioativo, semelhante ao traçador já usado em PET, que se acumula naturalmente em células cancerosas de rápido crescimento. À medida que esse traçador percorre o tumor, ele emite um brilho azulado fraco conhecido como radiação de Cerenkov. Os pesquisadores projetaram pequenas nanopartículas de dióxido de titânio revestidas com uma proteína que direciona o câncer, para que elas também se acumulem no tumor. Quando o traçador e as nanopartículas se encontram, a luz interna acende as partículas, que por sua vez geram rajadas de espécies reativas de oxigênio — moléculas altamente reativas que danificam as células cancerosas de dentro.
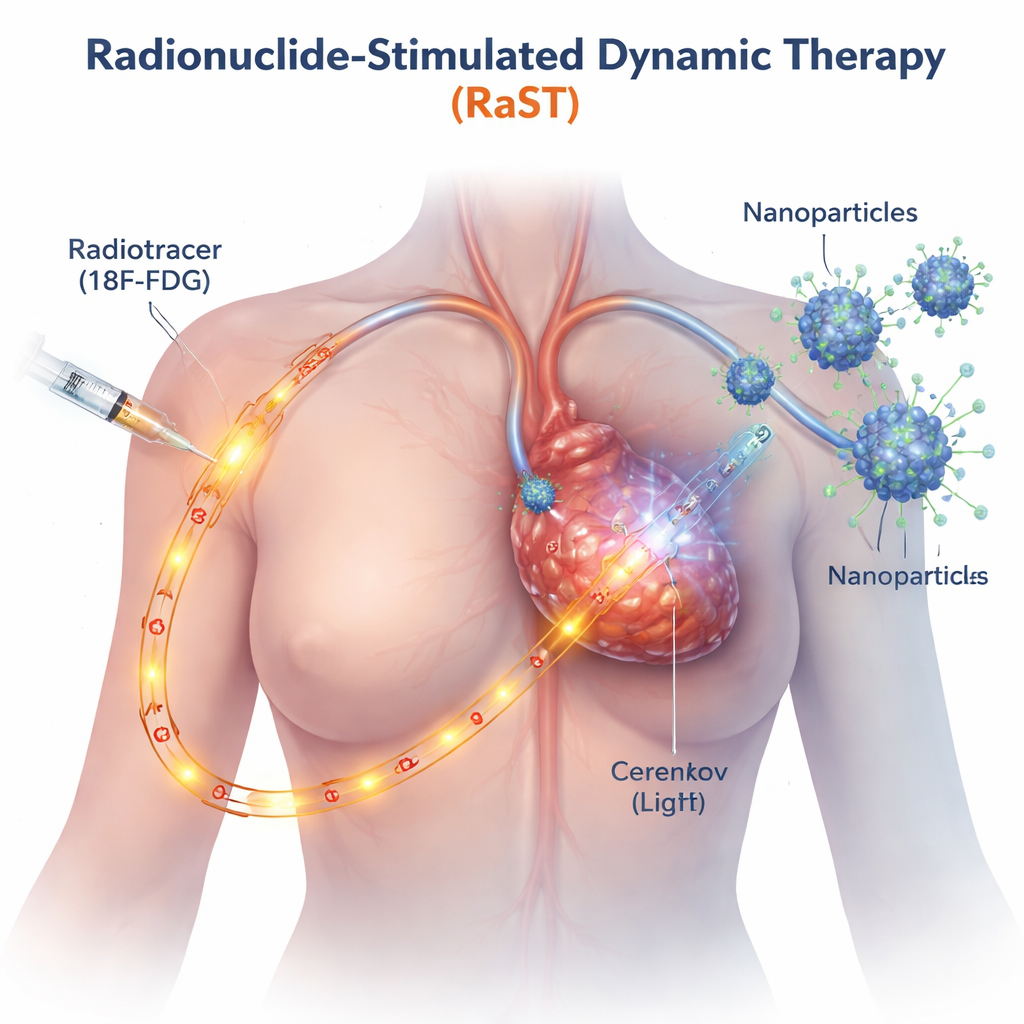
Disparando duas vias distintas de morte celular
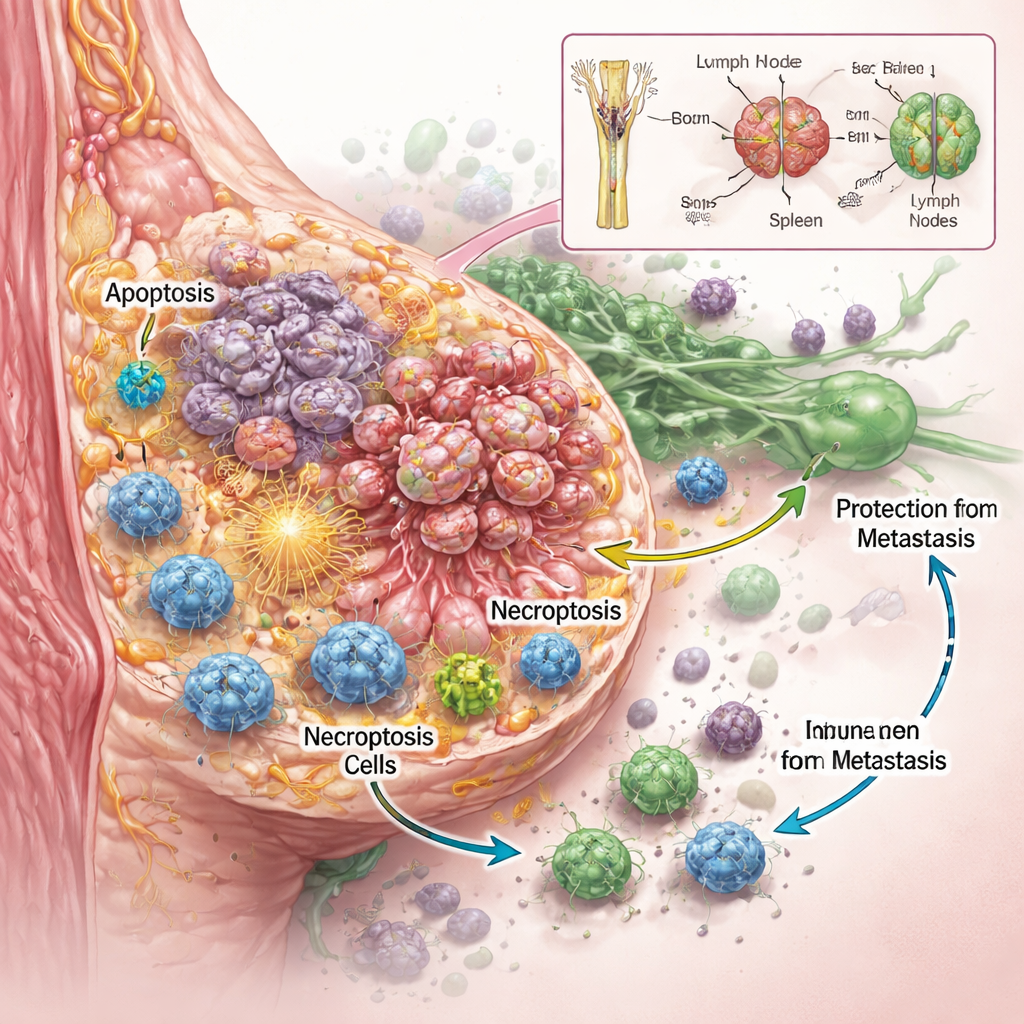
A equipe quis saber não apenas se a RaST matava as células cancerosas, mas como isso ocorria. Usando várias linhagens agressivas de câncer de mama em laboratório, eles descobriram que doses cuidadosamente ajustadas do traçador radioativo e das nanopartículas agiam em conjunto para danificar as células tumorais de forma mais eficaz do que cada componente isoladamente, inclusive em tipos conhecidos por resistir à quimioterapia padrão. Imagens detalhadas e medições de proteínas revelaram que a RaST ativou dois programas regulados de morte celular ao mesmo tempo. Um foi a apoptose, frequentemente descrita como “suicídio” celular, em que as células se desmontam de maneira ordenada. O outro foi a necroptose, uma forma mais explosiva de morte em que as células incham, rompem-se e liberam sinais moleculares de aflição para o ambiente. Esses sinais, conhecidos como moléculas associadas a danos e citocinas inflamatórias, podem funcionar como sinalizadores que atraem e ativam células do sistema imune.
Convocando o sistema imunológico para um controle duradouro
Para verificar se esse estilo inflamatório de eliminação tumoral fazia diferença em organismos vivos, os pesquisadores testaram a RaST em modelos murinos de câncer de mama. Em camundongos sem defesas imunes-chave, a RaST pouco fez para deter o crescimento tumoral ou a disseminação para os pulmões, apesar de gerar abundante morte celular local. Mas em camundongos com sistema imune intacto, o mesmo tratamento produziu respostas tumorais parciais e completas e preveniu metástase para os pulmões. Tumores expostos à RaST ficaram repletos de células imunes — especialmente células mieloides como macrófagos e células dendríticas — que são hábeis em engolfar material morto e apresentar fragmentos tumorais às células T. Testes sanguíneos mostraram ondas de sinais que estimulam e regulam o sistema imune ao longo do tempo, sugerindo que a RaST inicialmente desencadeia um ataque ao câncer e depois evolui para um estado mais equilibrado conforme os tumores encolhem ou se estabilizam.
Caçando remanescentes ocultos e protegendo contra recaída
Mesmo em camundongos onde os tumores pareceram completamente curados pela RaST, um corante de imagem altamente sensível revelou posteriormente pequenos bolsões de células cancerosas residuais escondidos em gânglios linfáticos. Notavelmente, esses animais ainda não desenvolveram novos tumores ou metástases distantes ao longo de muitos meses. Análises químicas mostraram que as nanopartículas de dióxido de titânio, inicialmente abundantes em ossos e fígado, foram gradualmente redistribuídas para o baço e os gânglios linfáticos — precisamente os centros onde as células imunes patrulham. Essa migração lenta provavelmente mantém uma fonte local de oxigênio reativo disponível para as células imunes, ajudando-as a reconhecer e controlar esses remanescentes ocultos antes que possam crescer ou se espalhar.
O que isso pode significar para o cuidado oncológico futuro
Em termos simples, este trabalho mostra que a RaST é mais do que apenas outra forma de envenenar células tumorais. Ao combinar traçadores radioativos, nanopartículas sensíveis à luz e as próprias defesas do corpo, ela empurra as células cancerosas para duas formas de morte programada que alertam de maneira clara o sistema imunológico. Em animais imunocompetentes, isso conduz a um controle duradouro de tumores agressivos de mama e bloqueia a metástase, mesmo quando algumas células cancerosas permanecem em gânglios linfáticos. Embora muito ainda precise ser feito antes que essa abordagem possa ser testada amplamente em humanos, o estudo aponta para tratamentos futuros que não visam apenas reduzir tumores, mas remodelar a relação entre câncer, morte celular e imunidade para que o próprio corpo ajude a manter a doença controlada a longo prazo.
Citação: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Palavras-chave: câncer de mama, nanopartículas, imunoterapia, terapia com radionuclídeos, necroptose