Clear Sky Science · pt
A glicofagia é uma via bilatéria antiga que suporta adaptação metabólica por meio da evolução estrutural do STBD1
Como ostras revelam truques energéticos ocultos
Os animais sobrevivem a tempos difíceis acessando combustíveis armazenados, mas nem todos dependem do mesmo tipo de “bateria”. Este estudo examina as ostras-do-Pacífico e mostra que, ao contrário de muitos outros animais que recorrem principalmente à gordura, as ostras dependem fortemente de açúcar armazenado, na forma de glicogênio. O trabalho revela uma via celular pouco conhecida — chamada glicofagia — que ajuda as ostras a drenar e reabastecer rapidamente suas reservas de açúcar, e traça como esse sistema evoluiu ao longo do reino animal.
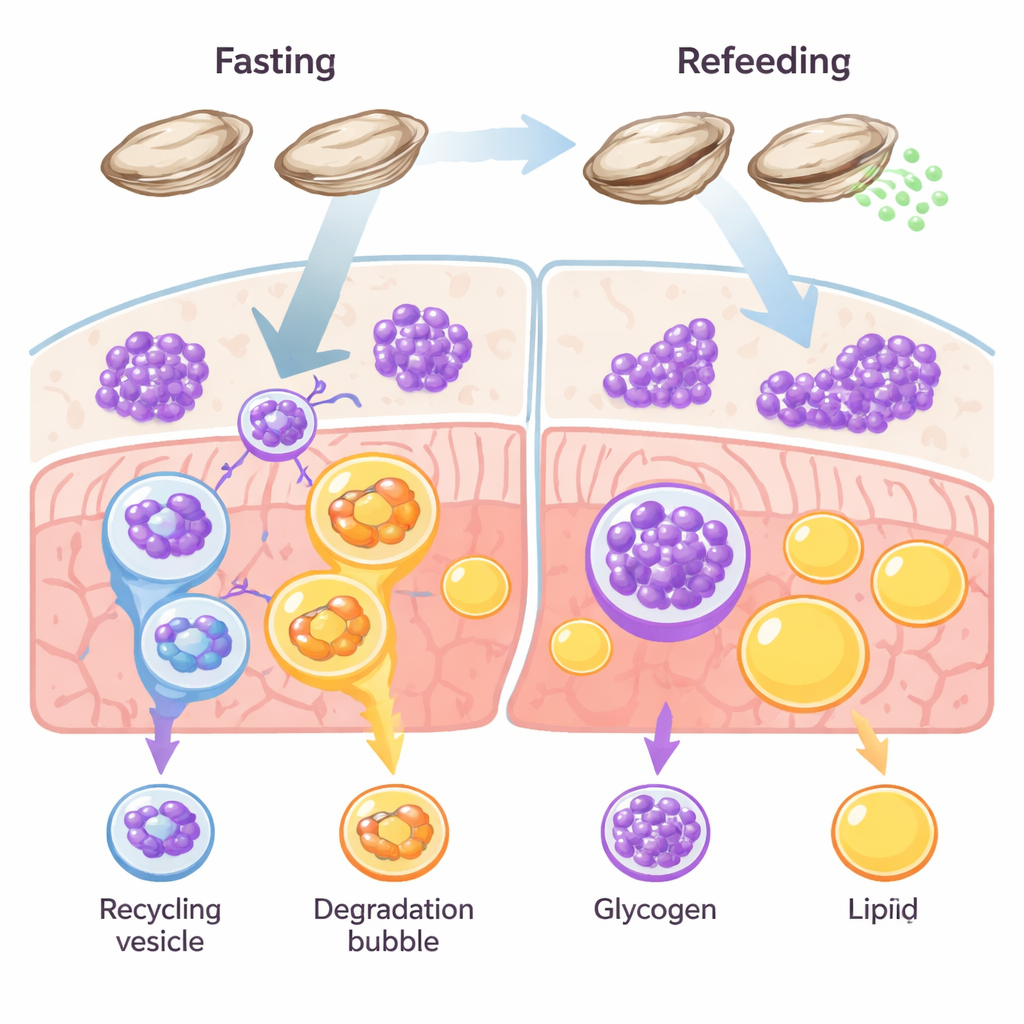
Uma estratégia de sobrevivência centrada no açúcar
A maioria dos animais gerencia várias reservas de energia, principalmente gordura e glicogênio. Em vertebrados como peixes e mamíferos, a gordura normalmente domina como reserva de longo prazo. As ostras quebram essa regra. Seus tecidos estão repletos de glicogênio, e pesquisas anteriores sugeriram que esses moluscos consomem açúcar, em vez de gordura, quando o alimento é escasso ou durante a gametogênese. Os autores procuraram testar se a glicofagia — a degradação dirigida do glicogênio dentro das células — atua como uma via de sobrevivência primária nas ostras durante o jejum e a recuperação.
Observando as células mudarem do armazenamento ao gasto
A equipe sujeitou ostras-do-Pacífico a duas semanas de jejum e depois as reabasteceu, acompanhando como seus tecidos respondiam ao longo do tempo. Durante o jejum, colorações microscópicas mostraram um aumento nos marcadores de autofagia — sinais de “limpeza” celular — exatamente onde o glicogênio era armazenado, enquanto o próprio glicogênio diminuía. As reservas de gordura, em contraste, praticamente não mudaram. Quando as ostras foram alimentadas novamente, o glicogênio retornou rapidamente e os sinais de autofagia caíram. Ao mesmo tempo, os níveis de uma proteína receptora chave chamada STBD1, que conecta especificamente o glicogênio à maquinaria de autofagia, subiram e desceram em sincronia com o uso do glicogênio. Outro receptor ligado à reciclagem de gordura, p62, permaneceu em grande parte estável. Juntos, esses padrões apontam para uma via de reciclagem dedicada e centrada no açúcar: a glicofagia, não a lipofagia (que consome gordura), é a principal responsável pelo balanço energético nas ostras.
O gancho molecular que captura o glicogênio
A glicofagia depende do STBD1 atuando como um gancho molecular: ele se liga ao glicogênio e o entrega a pequenas proteínas adaptadoras que montam vesículas de reciclagem. Nas ostras, o STBD1 mostrou-se configurado de maneira diferente do homólogo em vertebrados. A proteína da ostra carrega sua região captadora de glicogênio, conhecida como domínio CBM20, na extremidade dianteira (N-terminus), enquanto o STBD1 de vertebrados coloca esse mesmo módulo na extremidade traseira (C-terminus) e inclui uma cauda adicional hidrofóbica que o ancora às membranas celulares. Modelos computacionais e simulações sugeriram que o arranjo N-terminal da ostra confere ao CBM20 uma aderência mais forte e versátil às cadeias de açúcar ramificadas. Experimentos de laboratório confirmaram isso: o STBD1 purificado da ostra ligou-se ao glicogênio com mais afinidade do que o STBD1 de peixe ou de camundongo, e quando todas as versões foram expressas em células humanas, a proteína da ostra provocou uma queda mais acentuada no glicogênio durante a autofagia induzida.
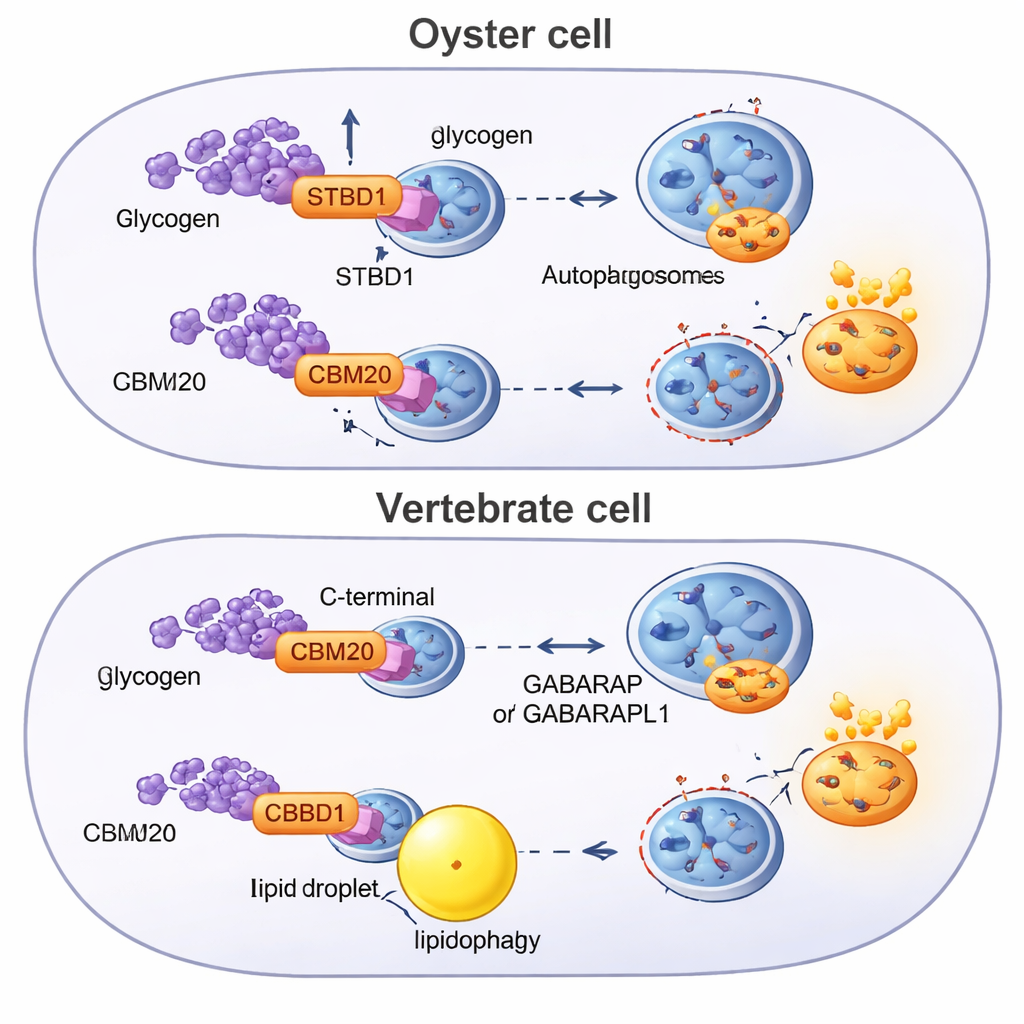
Reconfigurando uma via antiga ao longo dos animais
Para entender de onde veio esse sistema, os pesquisadores escanearam genomas de dezenas de animais em busca de proteínas portadoras de CBM20 e construíram árvores evolutivas. Eles descobriram que o STBD1 é uma invenção dos bilatérios — aparecendo no ancestral comum dos animais com planos corporais bilaterais —, mas sua estrutura foi reordenada em diferentes linhagens. Ostras e outros lophotrochozoários tendem a manter o desenho ancestral com o CBM20 N-terminal, às vezes até duplicando o módulo de ligação ao açúcar. Cordados, o grupo que inclui os vertebrados, mostram uma versão distinta em que o CBM20 foi movido para a cauda da proteína. Esse rearranjo correlaciona-se com uma ligação ao glicogênio mais fraca e com uma estratégia metabólica que confia mais na quebra de gordura por lipofagia, apoiada por outros receptores e proteínas adaptadoras de autofagia que as ostras não possuem.
O que isso significa para as escolhas energéticas da vida
Para não especialistas, a mensagem principal é que os animais evoluíram mais de uma maneira de enfrentar a escassez de energia. As ostras demonstram uma estratégia antiga centrada no açúcar: uma versão de alta afinidade do STBD1 captura glicogênio rapidamente e o alimenta em unidades de reciclagem celular, tornando a glicofagia uma fonte de energia principal durante o estresse. Os vertebrados, em contraste, parecem ter trocado parte dessa forte aderência ao açúcar por uma abordagem mais equilibrada ou inclinada à gordura, apoiada por parceiros protéicos e arranjos de domínios diferentes. Ao ligar a estrutura detalhada de proteínas às escolhas de combustível em todo o organismo, este estudo ilustra como pequenas “reconfigurações” moleculares podem ajudar ramos distintos da árvore animal a se adaptarem aos seus próprios ambientes e estilos de vida.
Citação: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
Palavras-chave: glicofagia, metabolismo do glicogênio, biologia do ostréa, autofagia, evolução do metabolismo