Clear Sky Science · pt
Reprogramação epigenética e metabólica em feocromocitomas e paragangliomas metastáticos impulsionada por mutações em SDHB
Por que esses tumores raros importam
Feocromocitomas e paragangliomas são tumores raros que crescem a partir de células nervosas produtoras de hormônios, frequentemente próximos às glândulas adrenais. A maioria cresce lentamente e pode ser curada com cirurgia, mas cerca de um em cada cinco acaba se espalhando para outros órgãos, tornando‑se potencialmente fatal. Este estudo faz uma pergunta simples, porém crucial: o que faz com que alguns desses tumores se tornem perigosos? Ao investigar em profundidade como esses cânceres ligam e desligam seus genes e como se alimentam, os pesquisadores revelam uma vulnerabilidade oculta que pode, no futuro, ser alvo de novos tratamentos.
Do crescimento silencioso à disseminação letal
A equipe concentrou‑se em tumores que carregam alterações em um gene chamado SDHB. SDHB ajuda as mitocôndrias — as usinas de energia da célula — a executar parte do ciclo de Krebs, uma via central de produção de energia. Quando o SDHB é comprometido, uma molécula chamada succinato se acumula, e as células passam a comportar‑se como se vivessem em baixo teor de oxigênio, mesmo quando não é o caso. Os pesquisadores estudaram tecidos de 34 pacientes, comparando tumores que permaneceram localizados com aqueles que já haviam metastizado. Usando um mapa de metilação do DNA de alta resolução, que mostra como marcas químicas regulam a atividade gênica, eles descobriram que tumores metastáticos apresentavam um padrão mais intenso de silenciamento gênico do que os benignos, especialmente quando havia mutação em SDHB.
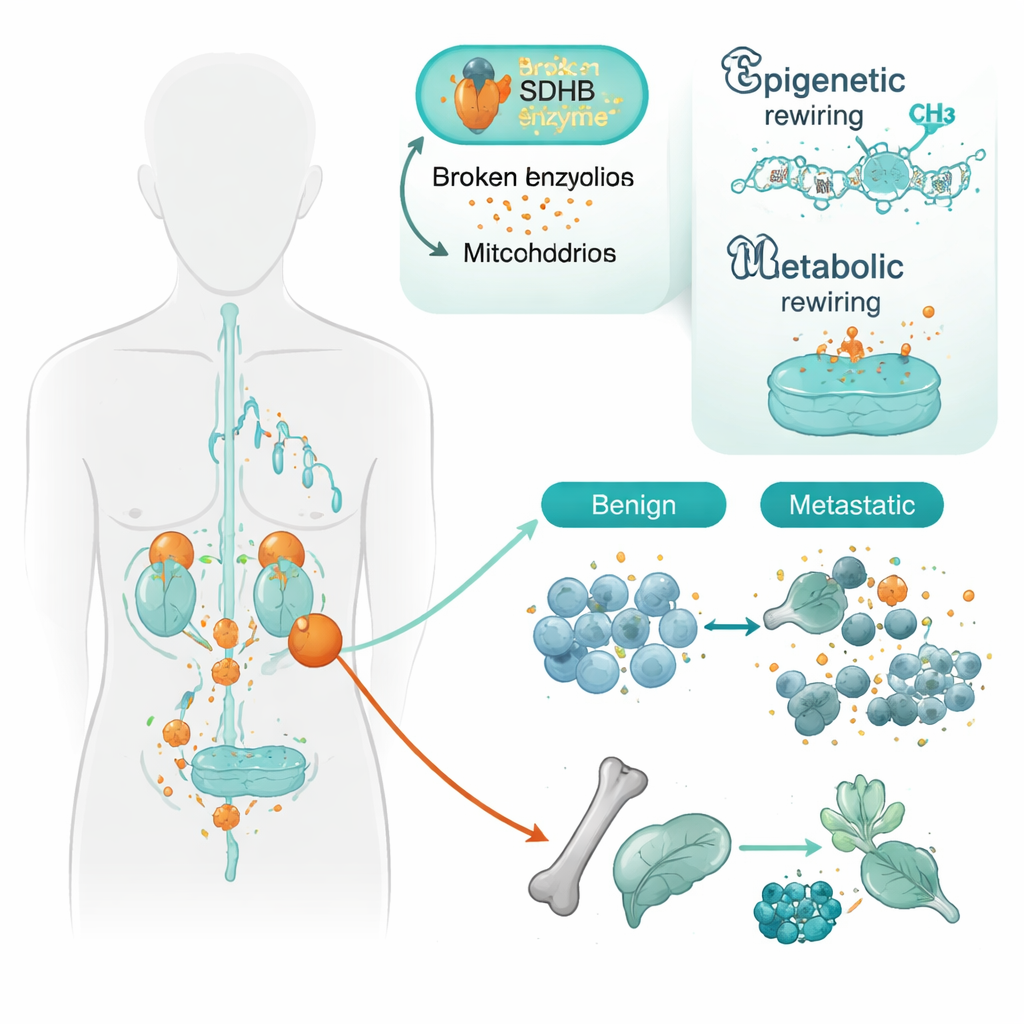
Reprogramando a identidade celular
Muitos dos genes silenciados em tumores agressivos eram aqueles que ajudam células de tipo nervoso a amadurecer e manter sua identidade especializada. Entre eles estão famílias de genes que orientam como as células se aderem umas às outras, organizam seu DNA e decidem que tipo celular se tornam. Um exemplo de destaque foi um gene de adesão celular chamado PCDHGC3. Mesmo em tumores SDHB-mutantes não metastáticos, a região regulatória desse gene já estava parcialmente desligada; nos tumores metastáticos o silenciamento era ainda mais intenso. Outro gene, SATB2, envolvido na organização de grandes trechos de DNA, foi silenciado apenas em tumores metastáticos, independentemente do status de SDHB. Em conjunto, esses padrões sugerem que a perda de SDHB “prepara” as células para um estado menos maduro e mais móvel, e alterações epigenéticas adicionais então as ajudam a se desprender e a metastizar.
Reconfigurando como os tumores consomem açúcar
Surpreendentemente, nem todas as alterações envolveram o silenciamento gênico. Um conjunto menor de genes ficou menos metilado e mais ativo, e esses estavam fortemente envolvidos na entrada de açúcares nas células. Entre eles, destacou‑se o gene transportador de frutose SLC2A5. Seu produto, conhecido como GLUT5, transporta frutose — um açúcar comum em frutas e em muitos alimentos processados — para dentro das células. Em modelos laboratoriais de células com características tumorais expostas a baixo oxigênio, SLC2A5 foi progressivamente ativado, enquanto outros transportadores de açúcar responderam de forma menos consistente. Os autores então criaram culturas de células derivadas de pacientes com tumores PPGL e mostraram que, quando a glicose era escassa, a adição de frutose ajudava essas células a continuar se dividindo, especialmente em condições de baixo oxigênio que imitam o microambiente tumoral.
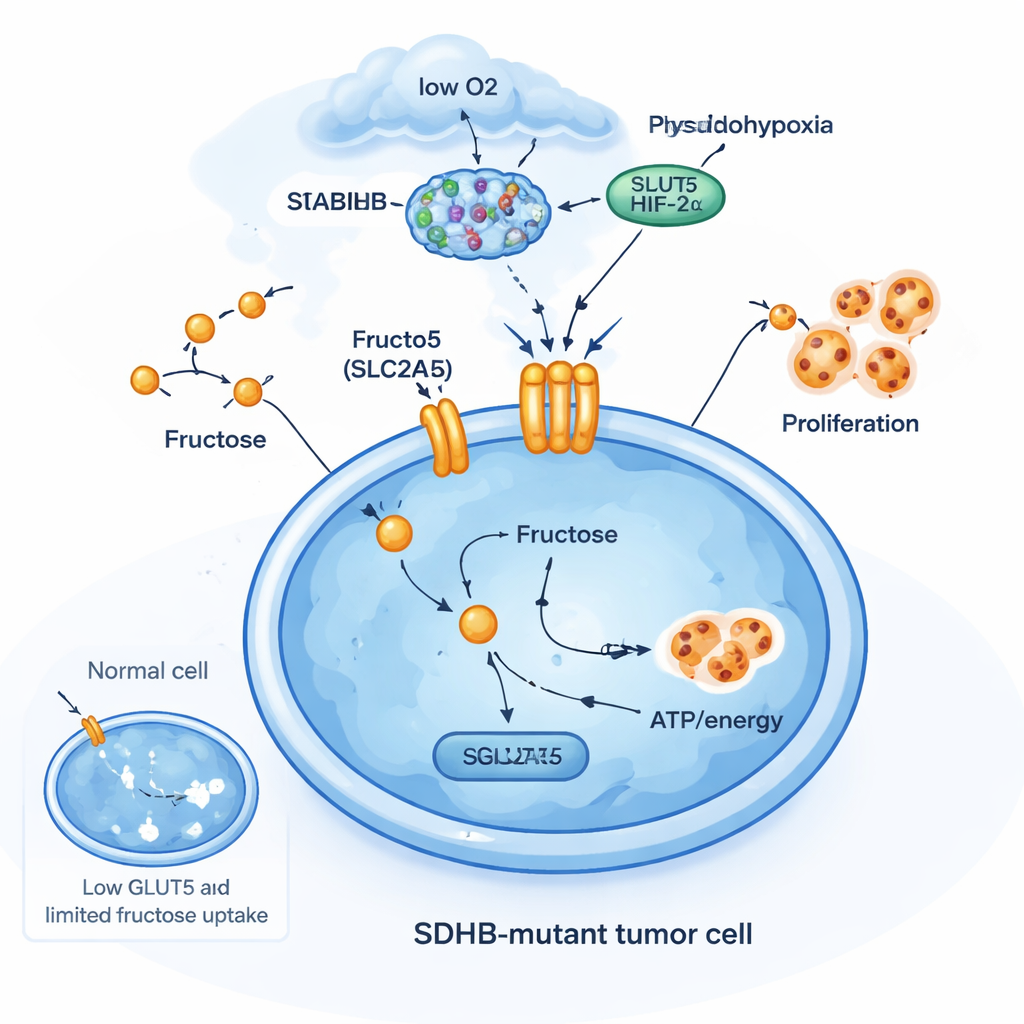
Um truque de sobrevivência movido a frutose
Para entender por que as mutações em SDHB são relevantes aqui, a equipe editou vários tipos celulares para remover SDHB. Em células do tipo cromafim da glândula adrenal e em uma linha de câncer renal com ativação constante do fator sensor de oxigênio HIF2α, a perda de SDHB aumentou os níveis de SLC2A5. Mas em linhas celulares de câncer mais comuns que não apresentavam essas características neuroendócrinas ou de HIF2α, o mesmo knockout de SDHB não ativou SLC2A5. Isso mostra que o transportador de frutose não faz parte de uma resposta ao estresse genérica; é uma adaptação altamente específica em certos tipos celulares que já vivem em um estado de “pseudo‑hipóxia”. Nessas células, perda de SDHB, acúmulo de succinato e atividade de HIF2α cooperam para abrir uma nova via metabólica: a captação de frutose para sustentar o crescimento quando oxigênio e glicose são limitados.
O que isso significa para os pacientes
Em termos simples, o estudo revela uma dupla mudança em PPGLs metastáticos com mutação em SDHB. Primeiro, seu sistema de controle do DNA é reconfigurado para empurrar as células a um estado menos especializado e mais plástico, propenso à invasão. Segundo, seu sistema energético é reprogramado para recorrer à frutose como combustível alternativo em nichos adversos, com pouco oxigênio e pouca glicose. Ao identificar o transportador de frutose SLC2A5/GLUT5 como um ator-chave nesse processo, o trabalho aponta para um possível calcanhar de Aquiles: bloquear a captação ou o metabolismo da frutose poderia, teoricamente, privar seletivamente esses tumores de energia, poupando a maioria dos tecidos normais. Embora tais terapias ainda não estejam disponíveis, mapear esse panorama epigenético e metabólico é um passo crítico rumo a tratamentos mais precisos e focados no metabolismo para pacientes com PPGLs de alto risco e mutação em SDHB.
Citação: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Palavras-chave: feocromocitoma, paraganglioma, mutação SDHB, epigenética, metabolismo da frutose