Clear Sky Science · pt
Análise multiómica das redes de sinalização humana de PHACTR1
Por que esse gene dos vasos sanguíneos importa para você
Infartos, derrames e hipertensão têm todas origem na saúde dos nossos vasos sanguíneos. Um único gene chamado PHACTR1 surgiu repetidamente em grandes estudos genéticos dessas condições, mas os cientistas ainda não compreendiam o porquê. Este estudo usou uma abordagem abrangente, “em todos os níveis”, dentro de células humanas para mapear o que o PHACTR1 realmente faz, revelando como ele pode influenciar o crescimento celular, o uso de energia e o manejo do ferro — processos que, em última análise, moldam a saúde das artérias.
Uma varredura de grande escala dentro das células
Em vez de focar em uma molécula por vez, os pesquisadores usaram uma estratégia chamada multi-ômica — medindo simultaneamente milhares de RNAs, proteínas, pequenos metabólitos e lipídios nas células. Eles engenheiraram células humanas para produzir PHACTR1 em excesso ou para reduzir sua expressão, imitando diferenças genéticas naturais observadas em pessoas. Ao comparar essas células alteradas com controles normais em quatro camadas moleculares e depois alimentar os dados em softwares sofisticados de viações, construíram um mapa global de como a variação em PHACTR1 reverbera na maquinaria interna da célula. 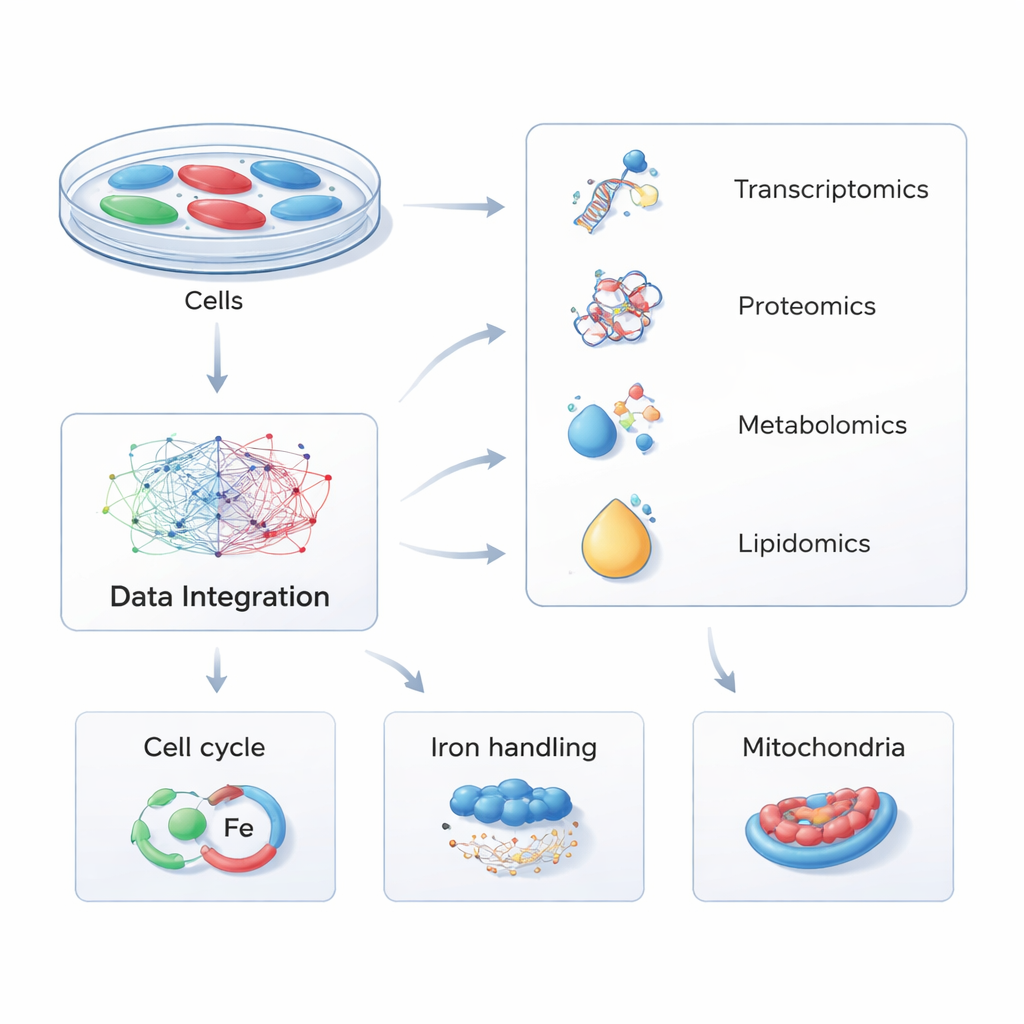
Além do esqueleto celular: controlando os ciclos de crescimento
O PHACTR1 era conhecido principalmente por ajudar a organizar o arcabouço interno de fibras de actina da célula. Os novos dados mostraram que ele também tem um papel importante no controle do ciclo celular — a coreografia pela qual as células copiam seu DNA e se dividem. Células com excesso de PHACTR1 saíram da fase de repouso G1 e se acumularam nas fases de cópia de DNA e pré-divisão, com menos células entrando com sucesso na mitose completa. Reguladores-chave como Ciclin B1, Cdt1 e outras proteínas do ciclo celular foram alterados. Quando a equipe repetiu os experimentos em células endoteliais humanas primárias — as células que revestem os vasos sanguíneos — observaram novamente mudanças em reguladores centrais do ciclo celular. Isso sugere que o PHACTR1 ajuda a decidir quando as células vasculares descansam, se dividem ou emperram, um equilíbrio crucial tanto na reparação das paredes vasculares quanto na formação de crescimentos teciduais perigosos.
Gerenciando o ferro e protegendo contra danos
A integração multi-ômica também indicou vias relacionadas ao ferro e a uma forma especializada de morte celular dependente de ferro chamada ferroptose. Embora as células não estivessem morrendo ativamente por ferroptose, o aumento de PHACTR1 reduziu os níveis de proteínas chave no manejo do ferro, incluindo a cadeia pesada da ferritina (a principal “concha” de armazenamento de ferro) e a heme oxigenase 1 (que recicla ferro a partir do heme). Em células endoteliais primárias, o PHACTR1 alterou de forma semelhante essas proteínas e defensores essenciais contra danos oxidativos. Como o ferro mal gerido pode alimentar inflamação, estresse oxidativo e placas arteriais instáveis, esses resultados sugerem que o PHACTR1 pode ajustar como as células vasculares armazenam e desintoxicam o ferro, potencialmente afetando quem é mais vulnerável a certas doenças dos vasos.
Mitocôndrias, energia e saúde arterial
Outra surpresa foi o papel do PHACTR1 nas mitocôndrias, as usinas de força da célula. A equipe encontrou proteína PHACTR1 dentro de mitocôndrias isoladas e observou que alterar seus níveis remodelava a rede mitocondrial. Quando o PHACTR1 estava alto, as mitocôndrias eram mais alongadas, e uma proteína chamada Drp1 sofreu modificação química em um sítio que reduz o fracionamento mitocondrial. Os níveis de uma proteína scaffolding, AKAP1, que ajuda a organizar a sinalização na superfície mitocondrial, subiam e caiam em sintonia com o PHACTR1. Essas mudanças estruturais corresponderam a alterações na produção de energia das células: PHACTR1 elevado reduziu a produção mitocondrial de ATP e foi associado ao acúmulo de certos metabólitos derivados de ácidos graxos que sinalizam queima lenta de gordura, enquanto PHACTR1 baixo levou as células a dependerem mais da glicólise (queima de açúcar). Análises de amostras de artérias humanas mostraram que PHACTR1 e AKAP1 tendem a ser ativados juntos, ligando esse circuito de controle mitocondrial diretamente a vasos sanguíneos reais. 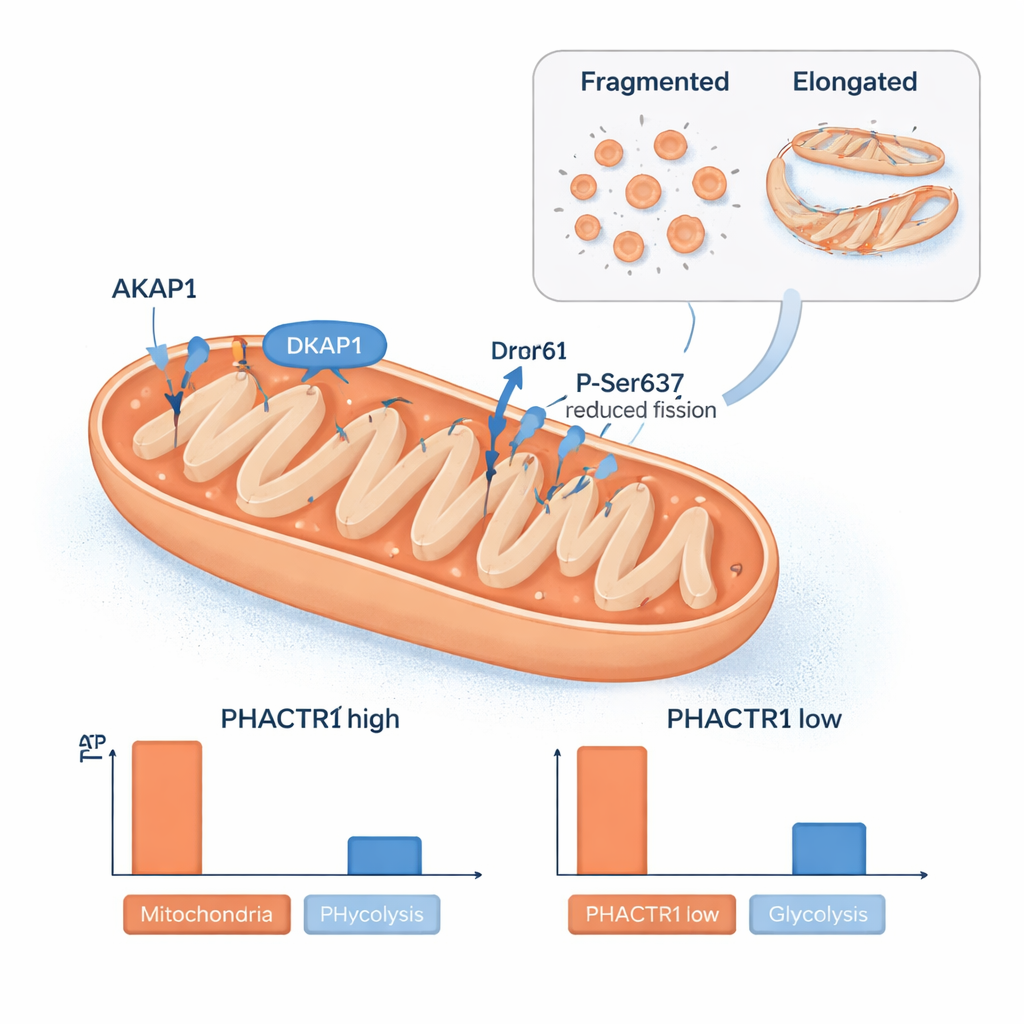
O que tudo isso significa para os vasos sanguíneos
Em conjunto, este trabalho mostra que o PHACTR1 não é um gene de função única, mas um coordenador mestre que influencia como as células vasculares se dividem, armazenam ferro e se energizam. Ao mapear essas conexões através de milhares de moléculas, o estudo ajuda a explicar por que diferenças naturais em PHACTR1 estão ligadas a uma gama tão ampla de doenças vasculares — desde doença arterial coronariana até rompimentos espontâneos de artérias e enxaqueca. Para leigos, a mensagem é que um gene identificado pela genética humana agora está sendo ligado a comportamentos celulares concretos que influenciam o crescimento de placas, a estabilidade dos vasos e o balanço energético. A longo prazo, entender essas redes controladas por PHACTR1 pode abrir caminho para terapias mais precisas que ajustem ciclos celulares, manejo de ferro ou função mitocondrial em direção a um estado mais saudável em pessoas em risco de doença cardiovascular.
Citação: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Palavras-chave: PHACTR1, doença vascular, multi-ômica, mitocôndrias, metabolismo do ferro