Clear Sky Science · pt
Alvo no PAK4 promove piroptose induzida por gemcitabina no câncer de pâncreas via eixo NLRP1/caspase-3/GSDME
Por que matar células cancerígenas de forma “incendiária” pode importar
O câncer de pâncreas está entre os mais letais, e mesmo nossas melhores drogas quimioterápicas frequentemente deixam de funcionar à medida que os tumores desenvolvem resistência. Este estudo investiga uma reviravolta surpreendente: a mesma droga, a gemcitabina, pode matar células tumorais de maneira mais explosiva e inflamatória chamada piroptose — se um “freio” molecular chave chamado PAK4 for desligado. Entender e mirar esse freio pode tornar tratamentos existentes mais eficazes para muitos pacientes.
Um câncer persistente que ignora o tratamento
Adenocarcinoma ductal pancreático geralmente é diagnosticado tardiamente e responde mal às terapias, de modo que a gemcitabina permanece um fármaco central apesar de suas limitações. Tipicamente a gemcitabina mata células por apoptose, uma forma ordenada e silenciosa de morte programada. Mas mais da metade dos tumores pancreáticos examinados neste estudo produziu níveis altos de uma proteína chamada GSDME, que pode converter essa morte silenciosa em piroptose — uma forma rápida e “explosiva” de morte celular que danifica a membrana e libera sinais inflamatórios. Isso levantou uma questão chave: se os tumores podem sofrer piroptose, por que tantos ainda resistem à gemcitabina?
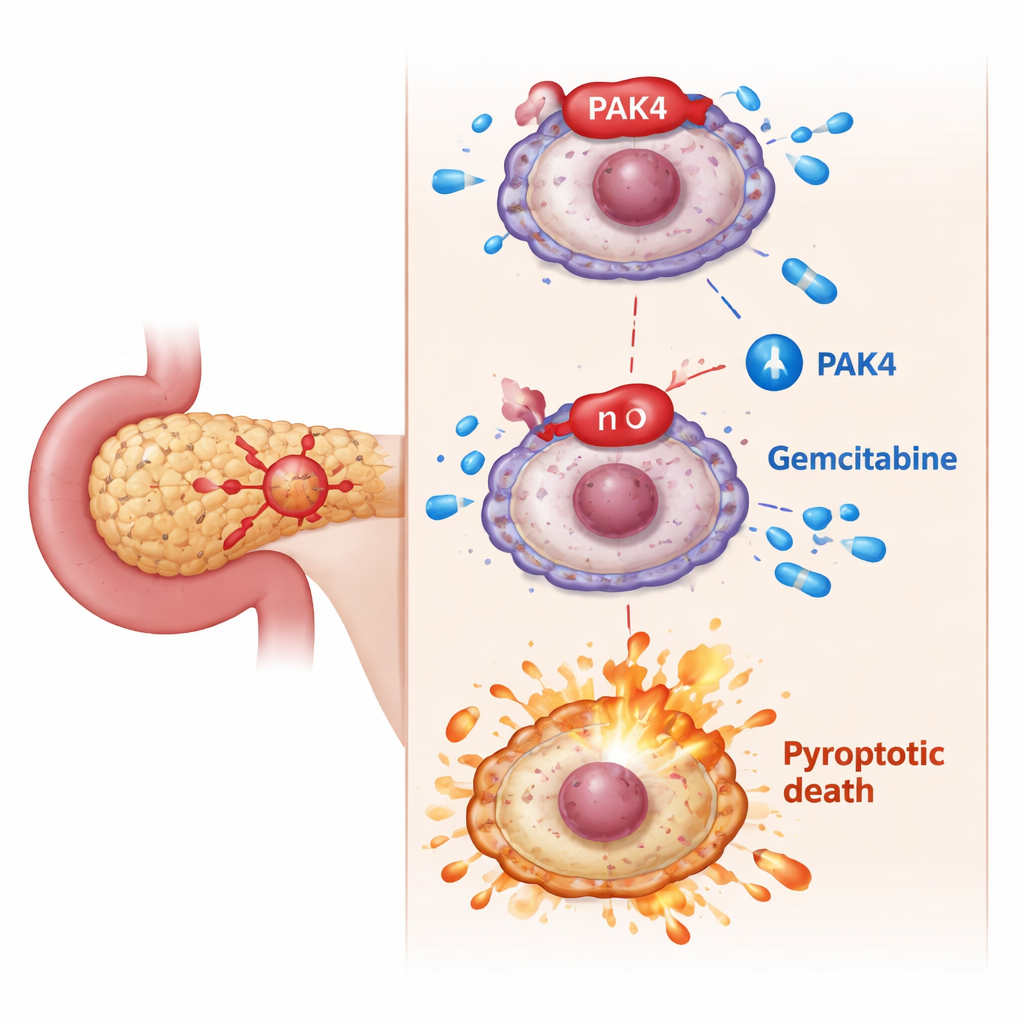
O freio oculto: PAK4 bloqueia a morte celular incendiária
Os pesquisadores focalizaram o PAK4, uma proteína promotora de crescimento conhecida por estar hiperativa no câncer de pâncreas e associada a má resposta à gemcitabina. Em experimentos celulares, células cancerígenas com altos níveis de PAK4 eram mais difíceis de eliminar com gemcitabina. Quando a equipe reduziu o PAK4, a gemcitabina tornou-se subitamente muito mais letal: as células exibiram características clássicas de piroptose — inchaço, bolhas semelhantes a balões, rupturas na membrana e maior liberação do conteúdo intracelular. No nível molecular, essa mudança dependia da clivagem da GSDME em um fragmento ativo pela caspase-3. Bloquear a caspase-3 impediu que a GSDME desencadeasse a piroptose, confirmando que o PAK4 normalmente age para segurar esse caminho de morte sob controle.
Como o PAK4 desarma o alarme de morte da célula
Ao aprofundar, os cientistas constataram que o PAK4 não ataca a GSDME diretamente. Em vez disso, sabota um “sensor de alarme” upstream chamado NLRP1. Em pacientes, níveis mais altos de NLRP1 foram associados a melhor sobrevida, sugerindo que ele ajuda o organismo a conter tumores. Em células cancerígenas, quando o NLRP1 foi removido, a morte celular induzida por gemcitabina e a ativação da GSDME caíram acentuadamente, mostrando que o NLRP1 alimenta a maquinaria da piroptose. Os níveis de PAK4 e NLRP1 eram inversamente relacionados em amostras tumorais: onde o PAK4 era alto, o NLRP1 era baixo. O estudo mostrou que o PAK4 ativo atua através de outra proteína, a ligase E3 Mdm2, para marcar o NLRP1 para destruição pelo sistema de descarte celular. Ao marcar o NLRP1 dessa forma, o PAK4 impede a ativação de uma reação em cadeia — via caspase-9 e caspase-3 — que normalmente culminaria na piroptose mediada por GSDME.
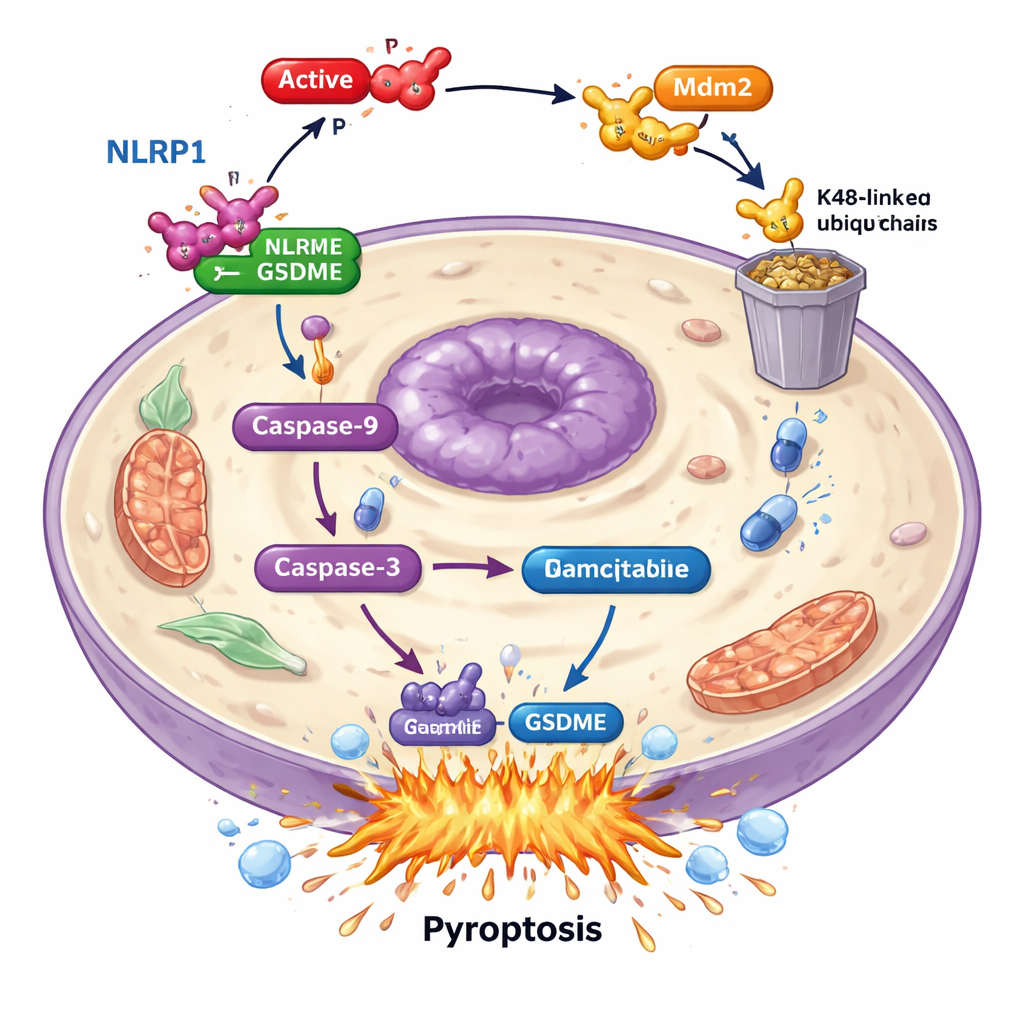
Desligar o PAK4 para turbinar a quimioterapia
Como o PAK4 atua como um freio sobre a piroptose, a equipe testou se bloquear sua atividade poderia reativar o poder letais da gemcitabina. Eles usaram um inibidor de PAK4 de pequena molécula chamado PF-3758309. Por si só, esse inibidor já empurrou células de câncer pancreático em direção à piroptose, aumentando a ativação da caspase-3, a clivagem da GSDME e a ruptura da membrana celular. Quando combinado com gemcitabina, o efeito foi ainda mais forte: mais células morreram por piroptose e os sinais moleculares da via de morte foram amplificados. Em modelos murinos portadores de tumores pancreáticos humanos, tanto a redução do PAK4 quanto o tratamento com o inibidor de PAK4 fizeram a gemcitabina encolher tumores de forma mais eficaz e aumentaram marcadores piroptóticos dentro dos cânceres.
O que isso significa para pacientes e tratamentos futuros
Em termos claros, este trabalho revela uma trava molecular — o PAK4 — que impede células de câncer de pâncreas de morrerem de forma particularmente destrutiva durante a quimioterapia. Ao desativar o PAK4, os médicos podem ser capazes de empurrar tumores tratados com gemcitabina para a piroptose, tornando o fármaco mais eficaz e potencialmente mobilizando o sistema imunológico contra o câncer. Embora mais estudos em modelos derivados de pacientes e ensaios clínicos sejam necessários, o estudo propõe um roteiro claro: mirar a via PAK4–Mdm2–NLRP1–GSDME para converter tumores resistentes em suscetíveis, usando drogas que já existem em combinações mais inteligentes.
Citação: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Palavras-chave: câncer de pâncreas, resistência à gemcitabina, piroptose, PAK4, terapia direcionada