Clear Sky Science · pt
Fluvastatina suprime o início e a progressão do câncer de mama ao direcionar CYP4Z1
Por que um remédio para colesterol importa no câncer de mama
Muitas mulheres tratadas por câncer de mama desenvolvem níveis alterados de gorduras no sangue e enfrentam a ameaça contínua de recidiva ou metastização. Este estudo explora uma ideia interessante: um comprimido comum para reduzir colesterol, a fluvastatina, poderia ser reaproveitado para frear ou prevenir o câncer de mama ao desativar uma proteína que alimenta células tumorais particularmente perigosas, semelhantes a células-tronco?
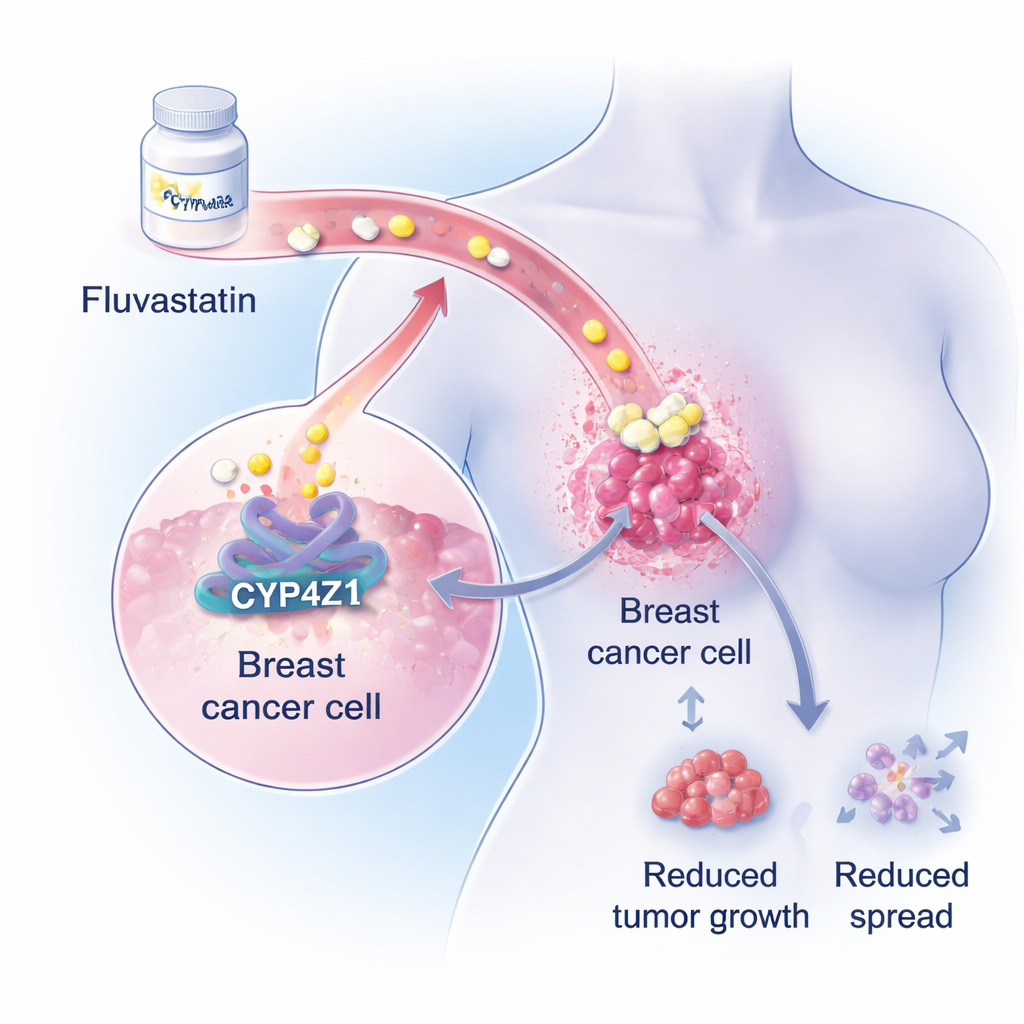
Um motor oculto dentro dos tumores de mama
Os pesquisadores focam em uma proteína pouco conhecida chamada CYP4Z1, encontrada em altos níveis nas células de câncer de mama, mas não no tecido mamário saudável. Trabalhos anteriores mostraram que o CYP4Z1 ajuda as células cancerosas a se comportarem mais como células-tronco — células capazes de se autorrenovar indefinidamente, resistir à quimioterapia e reiniciar tumores após o tratamento. Em grandes análises genéticas e bioquímicas, a equipe agora demonstra que o CYP4Z1 hiperativo impulsiona fortemente vias de síntese de lipídios dentro das células de câncer de mama, especialmente a produção de triglicerídeos, uma gordura de armazenamento importante. Como muitas pacientes com câncer de mama já desenvolvem distúrbios de lipídios no sangue durante a quimioterapia, esse papel promotor de gordura do CYP4Z1 sugeriu uma oportunidade para fármacos redutores de lipídios já existentes.
Reposicionando a fluvastatina da saúde cardíaca para o cuidado do câncer
Para testar essa ideia, os cientistas triaram uma pequena biblioteca de 23 medicamentos aprovados pelo FDA usados para reduzir lipídios sanguíneos. A fluvastatina, uma estatina amplamente prescrita para colesterol alto, destacou-se: bloqueou diretamente a atividade enzimática do CYP4Z1 de forma dependente da dose. Em doses muito menos prejudiciais às células mamárias normais do que às células cancerosas, a fluvastatina reduziu acentuadamente marcadores-chave de stemness, a capacidade das células de câncer de mama formarem “esferas tumorais” flutuantes e sua capacidade de migrar e invadir por barreiras semelhantes a tecidos em testes de laboratório. Também tornou as células tumorais mais sensíveis ao quimioterápico adriamicina, sugerindo que poderia potencializar tratamentos existentes.
Testando o medicamento em animais vivos
A equipe então avaliou a fluvastatina em modelos murinos. Em camundongos implantados com células humanas de câncer de mama, o tratamento periódico com fluvastatina retardou o crescimento tumoral, reduziu os níveis de um marcador de stemness (ALDH1A1) e do marcador de divisão celular Ki67 nos tumores, e diminuiu o número de nódulos metastáticos que surgiram nos pulmões. Importante, os camundongos que receberam fluvastatina mantiveram o peso corporal e não apresentaram anomalias importantes no sangue ou na medula óssea, apoiando um perfil de segurança favorável na dose testada. Em um modelo genético mais realista — camundongos modificados para desenvolver tumores de mama impulsionados por um gene causador de câncer — os pesquisadores também introduziram o CYP4Z1 humano no tecido mamário. Esses animais desenvolveram mais lesões pré-cancerosas e cancerosas, e mais metástases no fígado e nos pulmões, do que os controles. O tratamento com fluvastatina reduziu substancialmente tanto o número de lesões mamárias quanto de metástases à distância, especialmente nos camundongos que carregavam o gene adicional CYP4Z1.
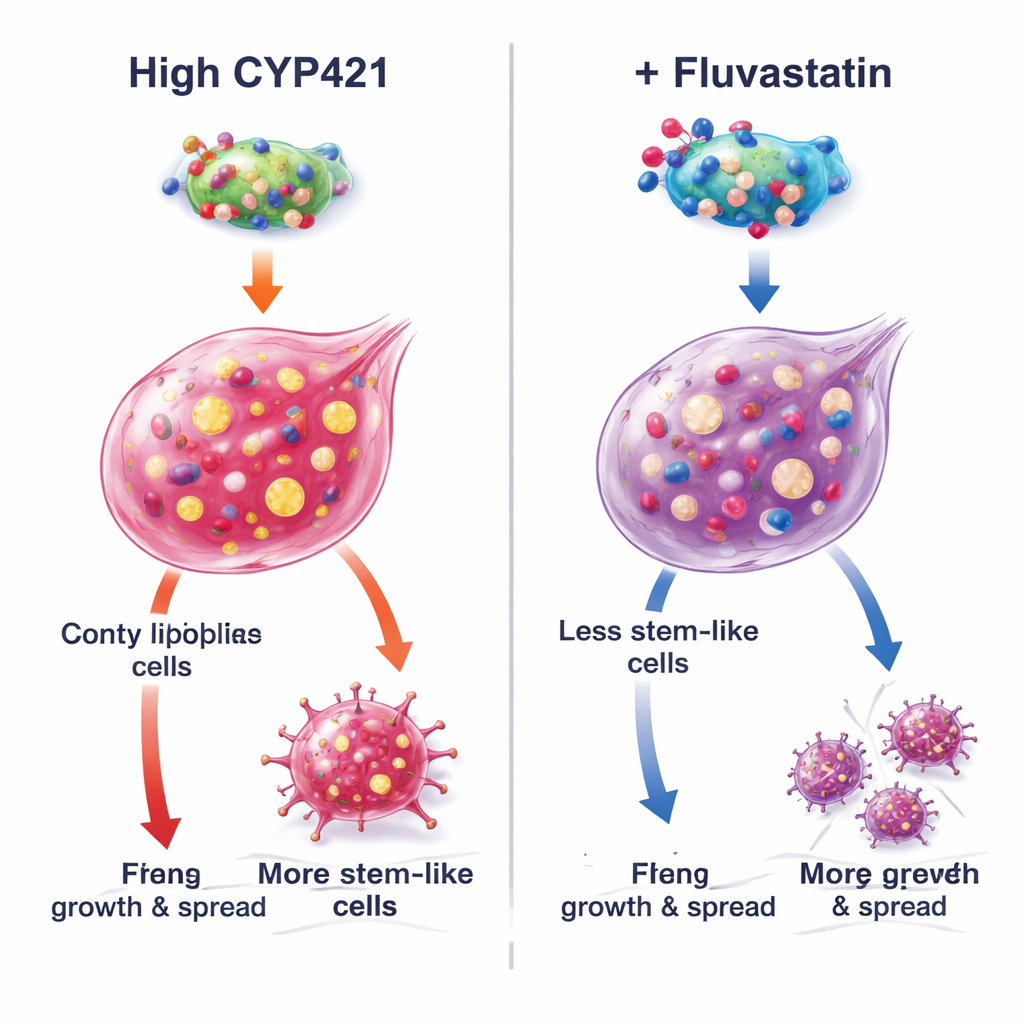
Como a fluvastatina desativa uma proteína que promove o câncer
Para entender o mecanismo, os autores combinaram modelagem computacional com engenharia proteica precisa. Eles previram que a fluvastatina se encaixa no sítio ativo do CYP4Z1 em três aminoácidos críticos (Lys109, Pro444 e Arg450). Quando esses locais foram mutados, a atividade do CYP4Z1 caiu e a fluvastatina não pôde mais inibi‑lo adicionalmente, confirmando essas posições como pontos de ancoragem. Em células que naturalmente não expressam CYP4Z1, a adição da proteína normal aumentou a stemness e ativou a sinalização PI3K/AKT promotora de crescimento, enquanto a fluvastatina reverteu esses efeitos. Versões mutantes do CYP4Z1 foram menos potentes e menos responsivas ao fármaco. Experimentos adicionais mostraram que o impacto da fluvastatina enfraqueceu quando a produção de triglicerídeos foi artificialmente aumentada, ou quando o CYP4Z1 foi silenciado, ressaltando que os efeitos mais fortes do medicamento provêm do bloqueio dessa proteína específica e de suas consequências na síntese de lipídios, em vez de induzir morte celular via “ferroptose” dependente de ferro.
O que isso significa para pacientes
No geral, o estudo sugere que a fluvastatina, além de reduzir o colesterol, pode conter os estágios iniciais e a disseminação tardia do câncer de mama em modelos experimentais ao direcionar o CYP4Z1, uma proteína que impulsiona o metabolismo lipídico e o comportamento semelhante a células‑tronco nos tumores. Como a fluvastatina já é aprovada e sua segurança é bem caracterizada, esses achados oferecem um caminho promissor para testes clínicos mais rápidos como terapia adjuvante, particularmente em pacientes cujos tumores expressam fortemente o CYP4Z1. Embora mais estudos sejam necessários para testar essa abordagem em humanos e identificar quaisquer alvos adicionais do medicamento, a pesquisa abre a porta para usar um remédio familiar para o coração como parte de uma nova estratégia contra cânceres de mama agressivos e propensos à recidiva.
Citação: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
Palavras-chave: câncer de mama, fluvastatina, células-tronco cancerígenas, metabolismo lipídico, reposicionamento de medicamentos