Clear Sky Science · pt
miRNAs diferencialmente expressos no córtex temporal de pacientes com Alzheimer e sua associação com a patologia da tau
Por que pequenos interruptores cerebrais importam na doença de Alzheimer
A doença de Alzheimer rouba lentamente a memória e a independência das pessoas, mas ainda não dispomos de tratamentos que a interrompam ou revertam. Este estudo examina alguns dos menores interruptores de controle do cérebro — curtas moléculas de RNA chamadas microRNAs — que ajudam a determinar quais proteínas as células produzem. Ao analisar tecido cerebral de pessoas que tiveram Alzheimer, os pesquisadores investigaram se alterações nesses microRNAs estão ligadas a uma característica-chave da doença: o acúmulo e a propagação de formas anormais da proteína tau dentro das células cerebrais.
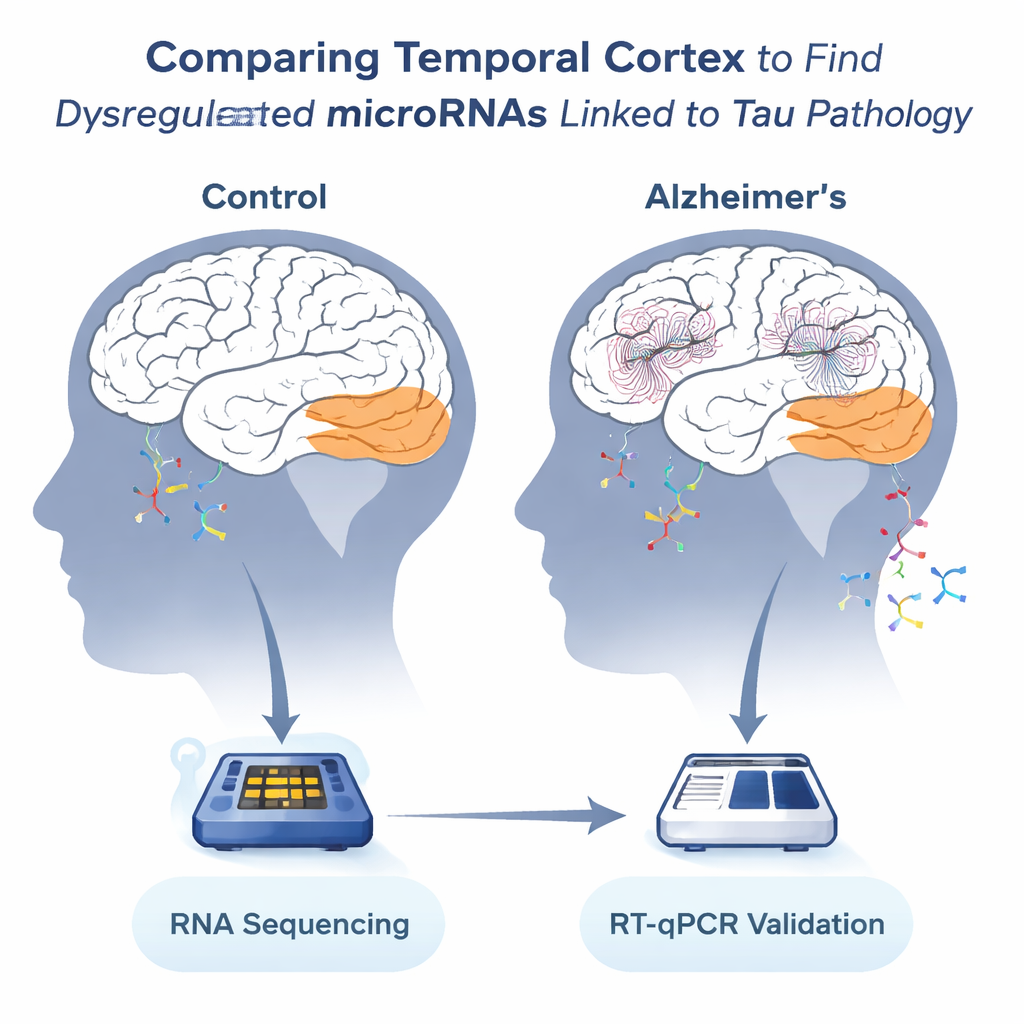
Examinando mensagens em uma região cerebral vulnerável
A equipe concentrou-se no córtex temporal, uma região importante para a linguagem e a memória que é fortemente afetada no Alzheimer. Após a morte, amostras de 36 indivíduos — 13 sem Alzheimer e 23 com a doença — foram coletadas em dois bancos de cérebros europeus. Os cientistas extraíram RNA desse tecido e usaram sequenciamento de alto rendimento para contabilizar centenas de microRNAs diferentes. Como o tecido cerebral se degrada após a morte, eles verificaram cuidadosamente a qualidade do RNA e selecionaram 19 amostras com integridade aceitável para a análise mais detalhada, usando depois as 36 amostras para confirmar as descobertas principais.
Descobrindo uma assinatura de microRNAs do Alzheimer
Entre 449 microRNAs detectados, 13 destacaram-se por estarem consistentemente alterados no córtex temporal de pacientes com Alzheimer. Oito estavam reduzidos e cinco aumentados em comparação com cérebros controle. Vários dos sinais mais fortes envolveram microRNAs já suspeitos de ter papel no Alzheimer: miR-129-5p, miR-132-3p e miR-146b-5p estavam todos mais baixos, enquanto miR-151a-5p estava mais alto. Essas moléculas são abundantes no cérebro e conhecidas por regular redes de genes relacionadas à saúde neuronal. Usando uma técnica secundária mais direcionada (RT-qPCR), os autores validaram que esses mesmos microRNAs mudaram na mesma direção, mesmo ao incluir amostras de qualidade inferior, o que reforça a confiança de que o padrão é real.
Ligando pequenos interruptores ao agravamento dos emaranhados de tau
A gravidade do Alzheimer no cérebro costuma ser avaliada pelo estágio de Braak, que reflete o quanto os emaranhados de tau se espalharam por diferentes regiões. Os pesquisadores acharam que os níveis de miR-129-5p, miR-132-3p e miR-146b-5p diminuíam progressivamente conforme o estágio de Braak aumentava, enquanto miR-151a-5p tendia a subir. Eles também mediram diretamente uma forma altamente fosforilada e propensa a formar emaranhados da tau nas mesmas amostras. Cérebros com mais dessa tau anômala mostraram o mesmo padrão: menos miR-129-5p, miR-132-3p e miR-146b-5p, e mais miR-151a-5p. Em outras palavras, as alterações nos microRNAs acompanharam tanto a classificação microscópica quanto os sinais bioquímicos da patologia da tau, sugerindo que estão intimamente ligadas ao processo da doença em vez de serem espectadores aleatórios.
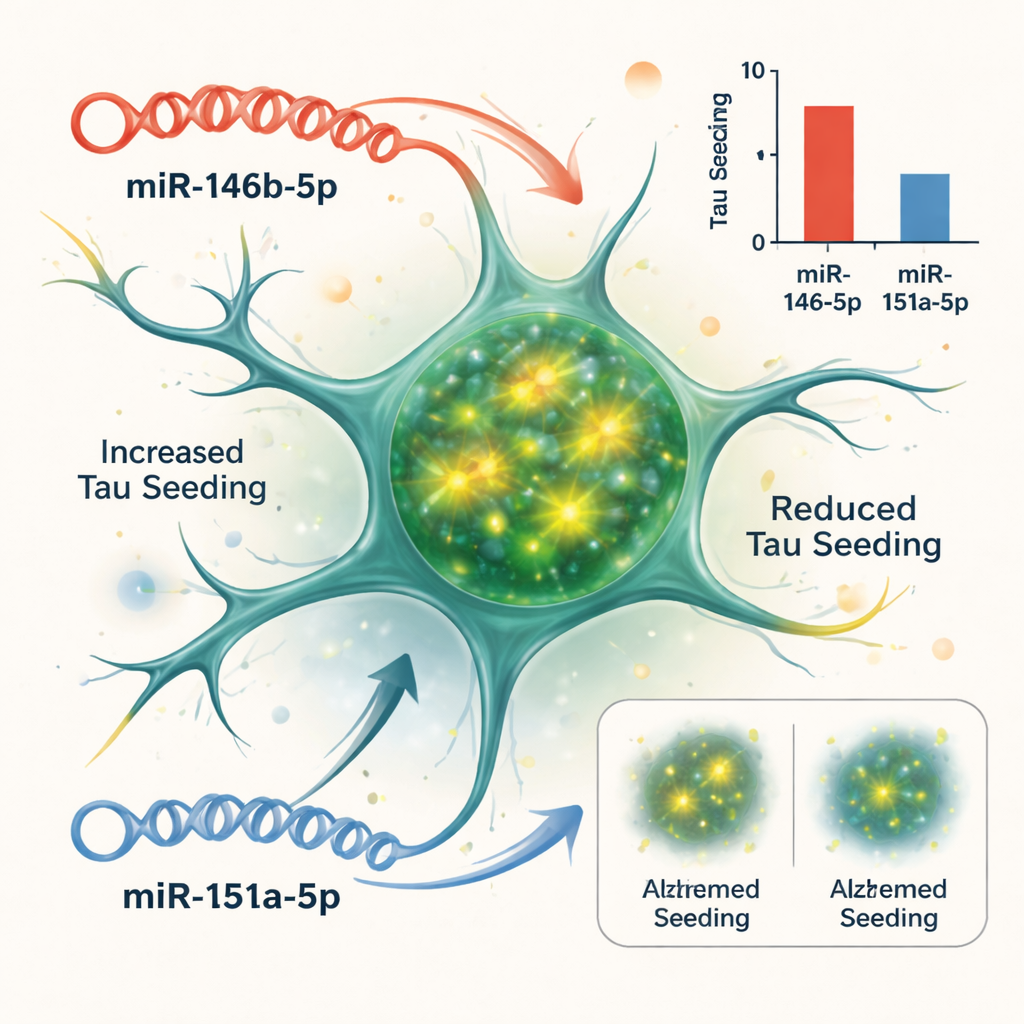
Testando causa e efeito em um modelo celular
Correlação não prova que microRNAs provoquem a doença, então a equipe recorreu a um sistema celular que reporta com que facilidade a tau pode “semeadura” e formar novos agregados. Eles usaram células biossensoras projetadas para acender quando fibras de tau se formam dentro delas. Quando adicionaram material rico em tau de cérebros com Alzheimer, as células produziram um forte sinal de fluorescência. Ao aumentar ou bloquear microRNAs específicos nessas células, os cientistas puderam ver quais alteravam essa semeadura de tau. Dois se destacaram: aumentar miR-146b-5p piorou a semeadura da tau, enquanto bloqueá-lo reduziu a semeadura; por outro lado, aumentar miR-151a-5p atenuou a semeadura da tau, enquanto inibi-lo tornou a semeadura mais robusta. Outros microRNAs testados tiveram pouco efeito neste ensaio.
O que isso pode significar para diagnóstico e tratamento futuros
Para entender o que esses microRNAs podem estar fazendo, os autores usaram ferramentas computacionais para mapear seus alvos gênicos previstos em vias biológicas conhecidas. Os microRNAs abaixo regulados — especialmente miR-129-5p, miR-132-3p e miR-146b-5p — foram ligados a redes envolvidas na sobrevivência dos neurônios, na sinalização química nas sinapses e em vias relacionadas ao Alzheimer. Isso sugere que a perda de sua influência “freadora” normal poderia perturbar múltiplos sistemas protetores ao mesmo tempo, enquanto o aumento de miR-151a-5p pode representar uma tentativa tardia e parcial do cérebro de contrariar a agregação da tau. Embora este trabalho dependa de tecido pós-morte e de modelos celulares simplificados, ele fortalece a ideia de que microRNAs específicos tanto espelham quanto modulam a patologia da tau. A longo prazo, medir essas moléculas no líquido cefalorraquidiano ou no sangue poderia ajudar a acompanhar a progressão da doença, e ajustar com precisão seus níveis no cérebro pode oferecer uma nova via para desacelerar ou impedir a propagação da tau tóxica.
Citação: Nagaraj, S., Quintanilla-Sánchez, C., Ando, K. et al. Differentially expressed miRNAs in the temporal cortex of Alzheimer’s disease patients and their association to tau pathology. Commun Biol 9, 253 (2026). https://doi.org/10.1038/s42003-026-09530-0
Palavras-chave: Doença de Alzheimer, microRNA, patologia da tau, córtex temporal, neurodegeneração