Clear Sky Science · pt
Bloqueio direcionado do splicing gênico pode desregular microRNAs primários embutidos em íntrons
Mensagens ocultas dentro de nossos genes
Muitas terapias gênicas recentes atuam ajustando as mensagens de RNA das nossas células, mas esses RNAs frequentemente escondem “anotações na margem” que os cientistas estão apenas começando a compreender. Este artigo mostra que drogas projetadas para corrigir splicing defeituoso de genes podem, acidentalmente, aumentar pequenos RNAs reguladores enterrados em íntrons — os trechos não codificantes entre os segmentos gênicos — com efeitos surpreendentes sobre a montagem e o desenvolvimento do cérebro.
Terapias gênicas que reescrevem o RNA
Oligonucleotídeos antisenso, ou ASOs, são pequenos fragmentos sintéticos de material genético que se ligam ao RNA e alteram como ele é lido ou processado. Vários ASOs já estão sendo testados ou usados para doenças genéticas raras, especialmente aquelas causadas por falhas no splicing do RNA — a etapa que costura os segmentos codificadores de um gene. A maioria dos testes de segurança foca se um ASO restaura a proteína correta e evita efeitos colaterais óbvios. Mas muitos genes também carregam RNAs não codificantes, incluindo microRNAs, dentro de seus íntrons. Essas moléculas minúsculas podem modular fortemente a atividade gênica, e até metade dos microRNAs conhecidos em vertebrados se origina de íntrons. O novo estudo pergunta: o que acontece com esses microRNAs embutidos quando forçamos mudanças no splicing com ASOs?
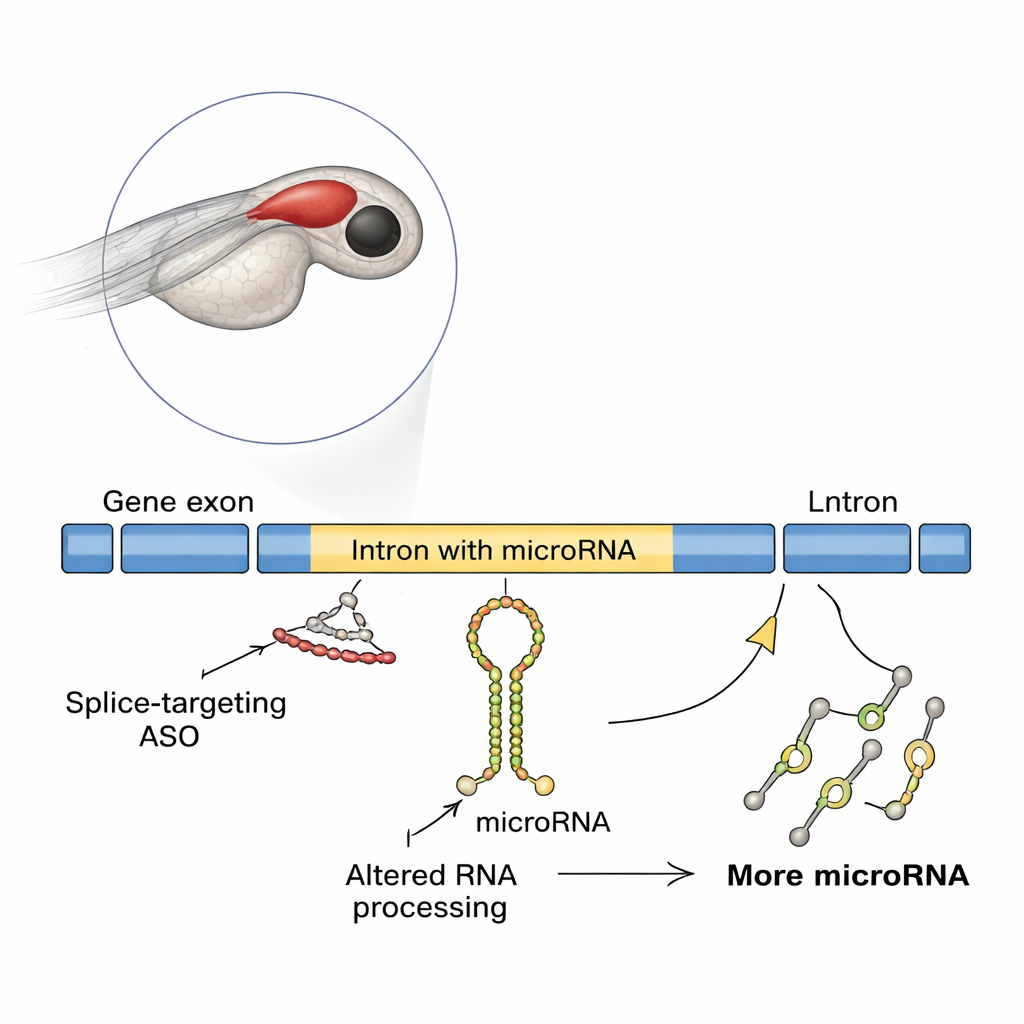
Um efeito surpreendente em cérebros de peixes em desenvolvimento
Os pesquisadores usaram o peixe-zebra, um modelo vertebrado popular cujos embriões transparentes facilitam o acompanhamento do desenvolvimento cerebral. Eles focaram em um gene chamado slit3, que ajuda a orientar fibras nervosas e contém um microRNA chamado mir-218a-1 dentro de um de seus íntrons. Quando a equipe bloqueou o início da tradução de slit3, o desenvolvimento dos axônios secretores de hormônio da hipófise parecia normal. Mas quando usaram um ASO diferente que bloqueava o splicing em um sítio de emenda específico de slit3, os axônios que deveriam projetar-se para a hipófise posterior foram drasticamente reduzidos, embora o número de neurônios produtores de ocitocina tenha permanecido o mesmo. Testes moleculares mostraram que esse ASO bloqueador de splicing causou retenção de íntron no RNA do gene, aumentando inesperadamente os níveis do transcrito de slit3, de seu íntron longo e do transcrito primário intrônico de mir-218a-1.
MicroRNA, não perda de proteína, impulsiona os defeitos
Para desvendar o que causou o problema axonal, os autores compararam vários cenários. Bloquear apenas o mir-218a-1 maduro não alterou os níveis de slit3, e um ASO separado direcionado a um sítio de splicing diferente próximo ao microRNA não produziu defeitos axonais nem aumentou o mir-218a-1. De forma crucial, quando o ASO bloqueador de splicing de slit3 foi combinado com um ASO que neutraliza o mir-218a-1, a fiação axonal se recuperou em grande parte. Da mesma forma, em peixes-zebra geneticamente deficientes em mir-218a-1, o mesmo ASO bloqueador de splicing de slit3 deixou de causar defeitos axonais, enquanto injetar um mimético sintético de mir-218a pôde reproduzir o fenótipo em peixes normais. Esses experimentos indicam que o aumento do microRNA intrônico — e não uma proteína Slit3 truncada — é o principal motor da perturbação do desenvolvimento.
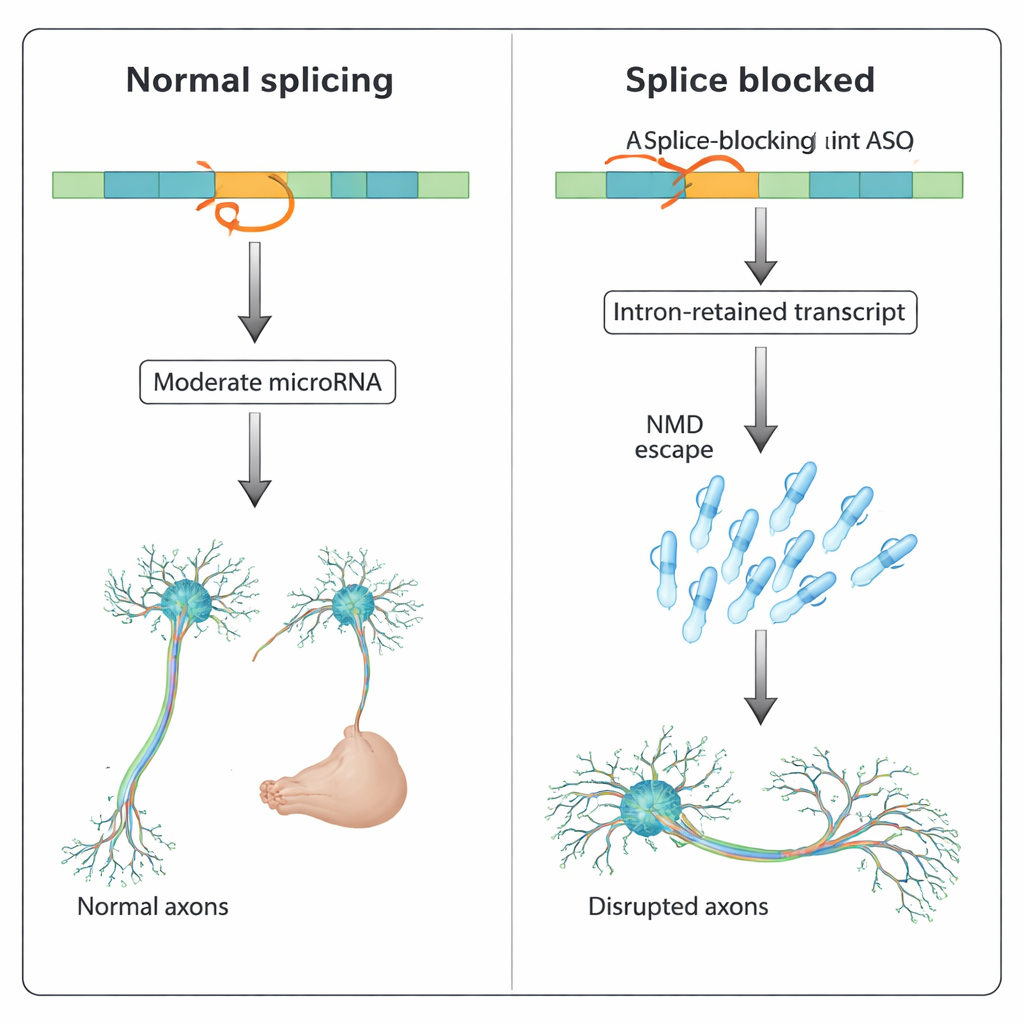
Um padrão mais amplo em múltiplos genes
A equipe então perguntou se esse efeito é único ao slit3. Eles pesquisaram o genoma do peixe-zebra e encontraram dezenas de genes codificadores de proteína que hospedam microRNAs intrônicos, muitos envolvidos no desenvolvimento e na sinalização. Dois desses genes, pank2 e dnm2a, já haviam apresentado problemas de desenvolvimento severos quando seu splicing foi bloqueado por ASOs, incluindo acúmulo de fluido no cérebro, inchaço cardíaco e deformidades corporais — problemas que os nocautes genéticos dos mesmos genes não reproduziram. Neste estudo, co-injetar ASOs que bloquearam especificamente os microRNAs intrônicos mir-103 (em pank2) ou mir-199-5p (em dnm2a) resgatou parcialmente esses fenótipos induzidos por ASO. Em alguns casos, o bloqueio do microRNA também restaurou a expressão do gene hospedeiro, enquanto em outros não, sugerindo que a atividade elevada do microRNA em si pode ser prejudicial mesmo quando as mudanças nos níveis globais são modestos.
O que isso significa para tratamentos futuros
As descobertas revelam que ASOs direcionados ao splicing podem fazer mais do que causar exclusão de éxons ou retenção de íntrons: eles podem estabilizar transcritos com íntron retido que escapam do sistema de controle de qualidade celular e aumentar microRNAs primários intrônicos, que então desregulam redes de genes-alvo. Em neurônios em desenvolvimento, essa atividade desenfreada de microRNAs pode distorcer o crescimento axonal e a conectividade. Para desenvolvedores de fármacos, isso significa que fenótipos incomuns ou “off-target” em testes animais podem nem sempre decorrer de vias genéricas de toxicidade, como ativação de p53, mas de efeitos não intencionais sobre RNAs intrônicos ocultos. Comparar cuidadosamente ASOs que bloqueiam a tradução e ASOs que bloqueiam o splicing, e monitorar a expressão de microRNAs intrônicos, pode ajudar a sinalizar esses riscos precocemente e refinar o design de ASOs antes que cheguem aos pacientes.
Citação: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Palavras-chave: oligonucleotídeos antisenso, microRNA, splicing de RNA, desenvolvimento do peixe-zebra, segurança da terapia gênica