Clear Sky Science · pt
Nimbolida melhora SDRA e colite ulcerativa ao interromper a ativação do inflamassoma NLRP3
Por que acalmar a inflamação descontrolada importa
Muitas doenças graves, desde insuficiência pulmonar que ameaça a vida até doenças dolorosas do intestino, são impulsionadas não apenas por germes ou lesões, mas pelo próprio sistema imune do corpo entrando em excesso. Este estudo investiga se um composto natural chamado nimbolida, derivado da árvore neem, pode agir como um “freio” preciso em uma potente máquina inflamatória dentro de nossas células imunes, abrindo possivelmente um caminho mais seguro para tratar condições como síndrome do desconforto respiratório agudo (SDRA) e colite ulcerativa.
Um alarme problemático dentro das células imunes
No centro desta história está um sistema de alarme molecular chamado inflamassoma NLRP3. Quando células imunes detectam perigo — sinais de infecções, tecidos danificados ou cristais — ele pode montar‑se como uma estrutura de Lego feita de três partes: o sensor NLRP3, o adaptador ASC e a enzima Caspase‑1. Uma vez montado, esse complexo ativa mensageiros potentes como IL‑1β e IL‑18 e pode desencadear uma forma inflamatória de morte celular chamada piroptose. Embora essa resposta ajude a eliminar ameaças, quando está hiperativada contribui para doenças crônicas e agudas, incluindo artrite, complicações do diabetes, doença de Alzheimer, SDRA e doença inflamatória intestinal. Indústrias farmacêuticas tentaram domar o NLRP3 com compostos sintéticos, mas muitos candidatos fracassaram por toxicidade, efeitos colaterais ou mau desempenho no organismo, deixando clara a necessidade de inibidores mais seguros e seletivos.
Descobrindo um inibidor potente de origem vegetal
Os pesquisadores rastrearam 126 compostos naturais para ver quais bloqueavam melhor a liberação de IL‑1β por células imunes de camundongos. A nimbolida sobressaiu, reduzindo a secreção de IL‑1β em mais de 80% nas doses testadas. Experimentos adicionais mostraram que a nimbolida reduziu fortemente a ativação da Caspase‑1, a liberação de IL‑1β e a morte piroptótica em macrófagos derivados de medula óssea de camundongos, com potência semelhante a um medicamento de referência chamado MCC950. Importante, a nimbolida não reduziu a liberação de outros mensageiros imunes como IL‑6, sugerindo que age de forma focalizada em vez de simplesmente desligar a imunidade. Testada contra diferentes gatilhos que ativam NLRP3 — como ATP, nigericina, cristais de alumínio e imiquimode — a nimbolida consistentemente diminuiu a atividade do inflamassoma, inclusive em células humanas THP‑1. Em contraste, não bloqueou dois inflamassomas relacionados, AIM2 e NLRC4, destacando sua especificidade pelo NLRP3.
Como a nimbolida bloqueia a máquina inflamatória
Para entender como a nimbolida funciona, a equipe investigou se ela interfere nas etapas iniciais de “priming” controladas pela via NF‑κB, ou nas etapas posteriores em que o inflamassoma se monta fisicamente. Tratamento de curto prazo, administrado após o priming, deixou sinais e expressão gênica de priming intactos, mas ainda assim reduziu IL‑1β e ativação da Caspase‑1, mostrando que a nimbolida age principalmente na etapa de montagem. Testes bioquímicos detalhados revelaram que a nimbolida não altera fluxos de potássio ou cálcio, dano mitocondrial, ou a interação de NLRP3 com sua proteína auxiliar NEK7. Em vez disso, ela interrompe o aperto de mão crucial entre NLRP3 e ASC, reduz o agrupamento de ASC em “specks” e impede NLRP3 de formar oligômeros de ordem superior. Usando ensaios de ligação e modelagem molecular, os autores mostraram que a nimbolida se liga diretamente à região NACHT do NLRP3 em um aminoácido específico, Lis565. Quando esse sítio foi mutado, a nimbolida deixou de proteger o NLRP3 da degradação ou de romper sua ligação com ASC, confirmando Lis565 como o ponto chave de ancoragem. Notavelmente, enquanto outros fármacos frequentemente visam a atividade ATPase do NLRP3, a nimbolida bloqueia a montagem sem afetar o uso de ATP, oferecendo um modo de ação distinto.
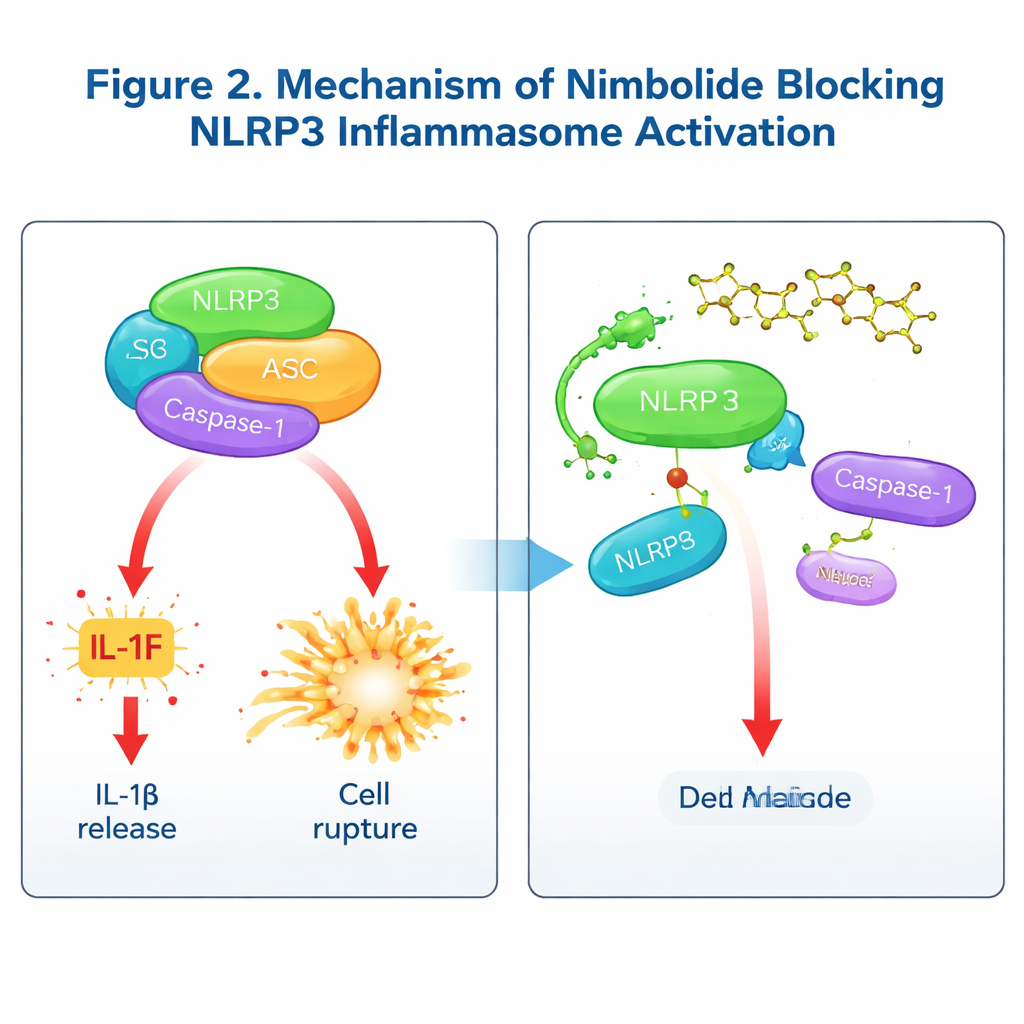
Testando a nimbolida em doenças pulmonares e intestinais
A equipe em seguida investigou se esse efeito molecular se traduz em proteção real em modelos de doença. Em camundongos expostos a uma toxina bacteriana para induzir SDRA, o tratamento com nimbolida antes da agressão reduziu dano ao tecido pulmonar, acúmulo de líquido e vazamento de proteína para os espaços aéreos. Houve menos células imunes invasoras nos pulmões e níveis mais baixos de IL‑1β no tecido pulmonar e no sangue. Benefícios semelhantes foram observados em um modelo em que a toxina foi administrada diretamente pelas vias aéreas. Em um modelo separado de colite ulcerativa, em que camundongos ingeriram um químico que machuca o cólon, a nimbolida limitou a perda de peso, melhorou a consistência das fezes e escores de sangramento, preservou o comprimento do cólon e reduziu sinais microscópicos de inflamação e erosão tecidual, junto com diminuição de IL‑1β no cólon. Crucialmente, em camundongos geneticamente modificados sem NLRP3, a doença já era mais branda e a nimbolida não trouxe benefício adicional, enfatizando que seus efeitos protetores dependem de bloquear o NLRP3.
O que isso pode significar para tratamentos futuros
Para não especialistas, a lição chave é que a nimbolida age como um freio inteligente em um dos interruptores inflamatórios mais potentes do corpo. Ao se ligar a um sítio preciso no NLRP3 e evitar que o inflamassoma se monte, ela acalma a inflamação excessiva tanto nos pulmões quanto no intestino sem desligar amplamente as defesas imunes. Embora a nimbolida em si ainda precise de melhorias em aspectos como estabilidade e entrega antes de virar um medicamento, este trabalho a posiciona como um ponto de partida promissor — e um modelo — para projetar drogas de nova geração contra doenças dirigidas pelo NLRP3, como SDRA e colite ulcerativa.
Citação: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
Palavras-chave: nimbolida, inflamassoma NLRP3, inflamação, síndrome do desconforto respiratório agudo, colite ulcerativa