Clear Sky Science · pt
Estudo de associação epigenômica de interleucina-6 circulante conecta metilação do DNA à saúde imunometabólica e inflamatória
Por que isso importa para a saúde do dia a dia
Inflamação crônica e de baixo grau molda silenciosamente nosso risco de doenças como diabetes tipo 2, doenças cardíacas e doença inflamatória intestinal. Um elemento-chave nesse processo é uma proteína de sinalização no sangue chamada interleucina‑6 (IL‑6). Este estudo investiga uma questão fundamental: como a IL‑6 interage com nosso epigenoma — as marcas químicas no DNA que ajudam a controlar a atividade dos genes — e o que isso significa para nossa saúde a longo prazo?
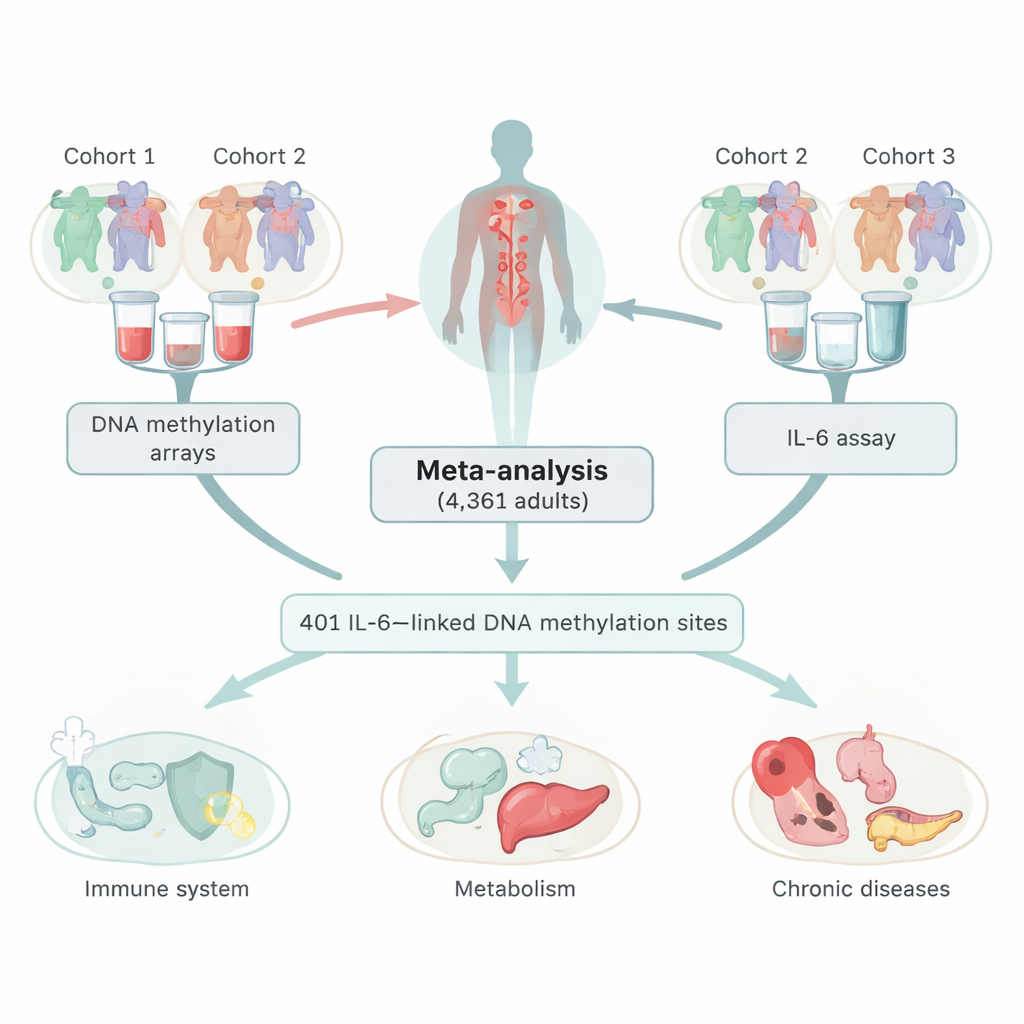
Analisando marcadores químicos no DNA
Os pesquisadores combinaram dados de três grandes estudos europeus, abrangendo 4.361 adultos que forneceram amostras de sangue. Nessas amostras, mediram tanto os níveis de IL‑6 quanto a metilação do DNA, uma marca química comum no DNA que pode aumentar ou diminuir a atividade de genes sem alterar o código genético. Ao escanear mais de 400.000 locais pelo genoma, identificaram 401 posições onde os níveis de metilação se correlacionavam com a quantidade de IL‑6 circulante no sangue. A maioria desses locais mostrou um padrão inverso: níveis mais altos de IL‑6 andavam de mãos dadas com menor metilação nesses pontos. A equipe verificou cuidadosamente que essas associações não eram simplesmente efeitos colaterais do tabagismo, diferenças nos tipos de células sanguíneas ou outro marcador inflamatório chamado proteína C‑reativa (PCR).
Conectando inflamação ao metabolismo e à doença
Em seguida, os autores investigaram se esses locais de DNA ligados à IL‑6 se sobrepunham a sinais observados em outros grandes estudos epigenéticos. Encontraram forte enriquecimento para traços com componente inflamatório ou metabólico, incluindo índice de massa corporal, gorduras no sangue, pressão arterial, glicemia, diabetes tipo 2, doença renal crônica e condições psiquiátricas e relacionadas ao estresse. Muitos dos mesmos pontos de metilação já haviam sido associados à PCR, mas os padrões sugerem que IL‑6 e PCR carregam assinaturas epigenéticas em parte distintas. Em outras palavras, as marcas químicas associadas à IL‑6 não são apenas uma cópia das associadas à PCR e podem fornecer informação adicional sobre o estado inflamatório e metabólico de uma pessoa.
Onde no genoma a ação acontece
Para entender o que esses locais de metilação podem estar fazendo, a equipe os mapeou em regiões regulatórias conhecidas do genoma. Descobriram que os locais associados à IL‑6 estavam concentrados em elementos de controle ativos, como potenciadores (enhancers) — trechos de DNA que ajudam a ligar genes — em vez de em regiões silenciosas. Esses locais também ficavam próximos a sequências de ligação para fatores de transcrição que regulam diretamente a IL‑6 e respostas ao estresse, incluindo NF‑κB, Atf4, CHOP e Nrf2. Ao combinar dados de metilação com grandes conjuntos de expressão gênica, os pesquisadores ligaram mais de 400 genes aos locais relacionados à IL‑6. Muitos desses genes estão no centro do controle imunológico e metabólico, incluindo SOCS3, IL6R, AIM2, IFI16, MTOR e RORC, e participam de vias que impulsionam ativação e uso de energia em um tipo especializado de célula T (células Th17) implicado em doenças inflamatórias crônicas.
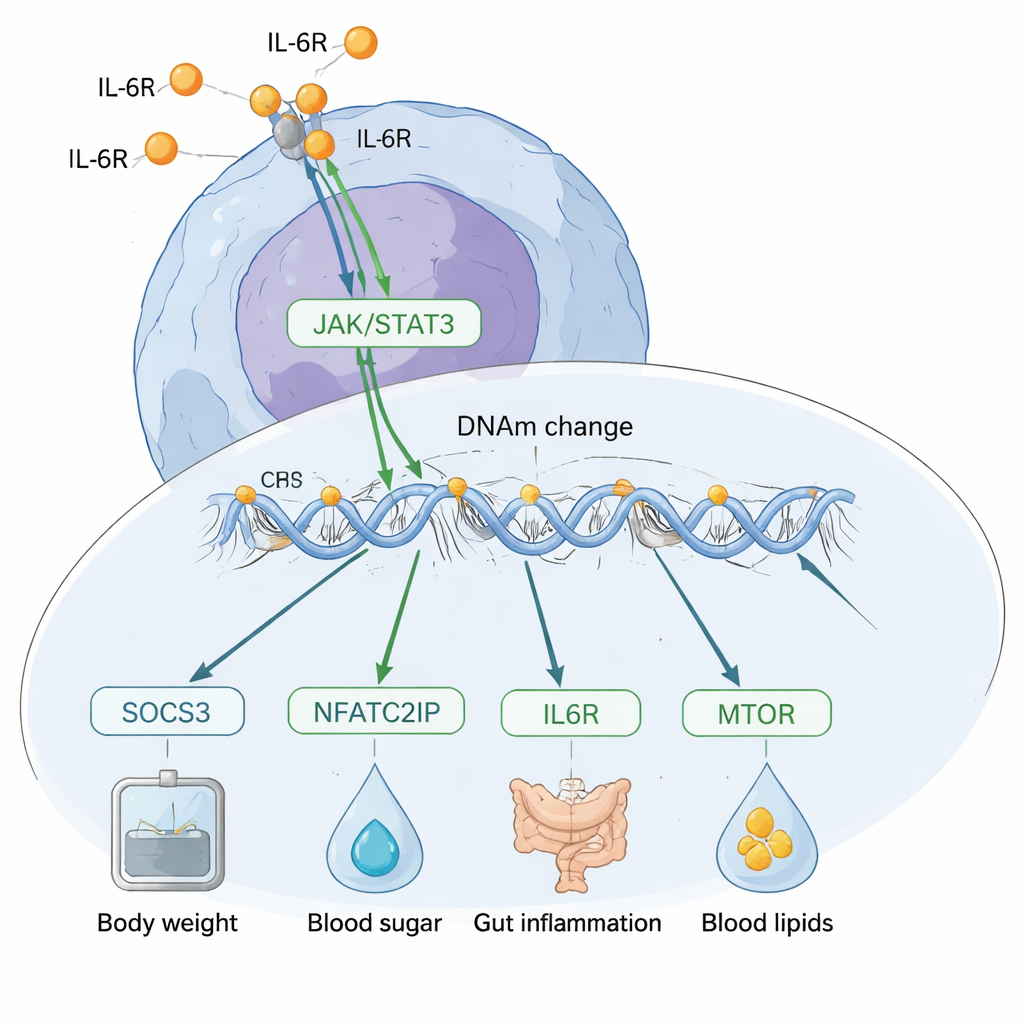
Em que direção corre a causa e o efeito?
Um grande desafio é descobrir se a metilação do DNA está causando mudanças na IL‑6 ou se a IL‑6 está remodelando a metilação. A equipe usou vários truques genéticos para sondar essa direção. Em todo o genoma, suas análises de “triangulação” apoiaram um modelo em que a IL‑6, em sua maior parte, dirige mudanças na metilação do DNA, em vez do contrário. Depois concentraram-se em sítios específicos e encontraram que mudanças de metilação próximas ao gene SOCS3 parecem mediar o impacto da IL‑6 em fatores de risco como peso corporal, colesterol, níveis de PCR e doença inflamatória intestinal. Em contraste, um local de destaque próximo a um regulador gênico chamado NFATC2IP mostrou sinais de influenciar a própria produção de IL‑6 e também parece afetar múltiplas condições, incluindo índice de massa corporal, diabetes tipo 2 e inflamação intestinal.
O que isso significa para prevenção e tratamento futuros
Para um leitor não especialista, a mensagem central é que IL‑6 e marcas epigenéticas no DNA estão intimamente entrelaçadas de formas que tocam muitas doenças comuns. Na maior parte das vezes, a IL‑6 parece deixar uma “pegada” química no genoma, particularmente em células imunológicas, marcando e possivelmente estabilizando estados pró‑inflamatórios. Em alguns sítios-chave, porém, a metilação pode ajudar a definir quanto IL‑6 é produzido e quão fortemente vias imunes respondem. Essas descobertas apontam para padrões de metilação do DNA como indicadores promissores baseados no sangue da saúde inflamatória e metabólica, e sugerem que alterações epigenéticas cuidadosamente direcionadas — especialmente em torno de genes como SOCS3 e NFATC2IP — podem um dia complementar medicamentos que bloqueiam a IL‑6 na prevenção ou tratamento de doenças crônicas.
Citação: Sinke, L., van Dongen, J., Delerue, T. et al. Epigenome-wide association study of circulating interleukin-6 connects DNA methylation to immunometabolic and inflammatory health. Commun Biol 9, 242 (2026). https://doi.org/10.1038/s42003-026-09520-2
Palavras-chave: interleucina-6, metilação do DNA, inflamação, doença metabólica, epigenética