Clear Sky Science · pt
MAT2A aumenta a transcrição de PARN via SRF para acelerar a glicólise e impulsionar a progressão maligna no osteossarcoma
Por que este estudo sobre câncer ósseo é importante
O osteossarcoma é o câncer ósseo mais comum em crianças e adolescentes, e os tratamentos praticamente não mudaram nas últimas décadas. Muitos pacientes jovens ainda enfrentam prognósticos ruins, especialmente quando a doença se espalha ou resiste à quimioterapia. Este estudo revela uma proteína “interruptor mestre” chamada MAT2A que ajuda células de osteossarcoma a crescer, a reprogramar seu uso de energia e a formar tumores agressivos — e mostra que um fármaco direcionado contra MAT2A pode retardar ou reduzir esses tumores em modelos laboratoriais.
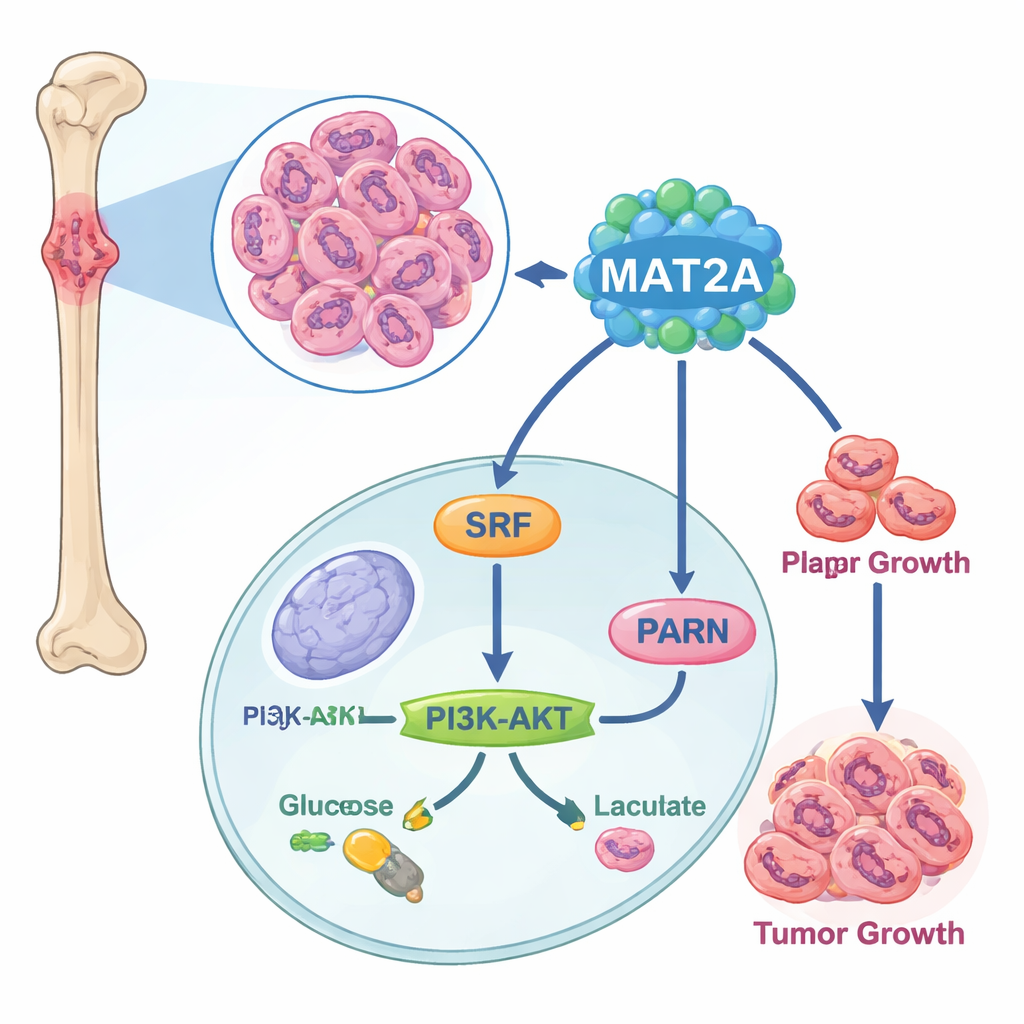
Um motor oculto dentro das células tumorais
Os pesquisadores começaram comparando amostras de câncer ósseo com tecido ósseo normal ao nível de célula única. Eles descobriram que o tecido de osteossarcoma contém mais células construtoras de tumor e menos células imunes, e que um gene em particular — MAT2A — estava incomumente ativo nas células cancerosas. Análises de bancos de dados públicos de câncer e de linhas celulares cultivadas em laboratório confirmaram que os níveis de MAT2A eram muito maiores no osteossarcoma do que em células ósseas saudáveis, e que pacientes com mais MAT2A tendiam a ter doença mais avançada e acometimento de linfonodos. Isso colocou MAT2A no centro das atenções como um potencial impulsionador da doença, em vez de um espectador passivo.
Reduzir MAT2A desacelera o crescimento do câncer
Para testar quão importante MAT2A é para o comportamento tumoral, a equipe usou ferramentas genéticas para diminuir os níveis de MAT2A em linhas celulares de osteossarcoma. Quando MAT2A foi silenciada, as células cancerosas dividiram-se mais lentamente e foram mais propensas a sofrer morte celular programada. Em camundongos implantados com essas células modificadas, os tumores cresceram muito mais devagar e ficaram significativamente menores, mesmo com o peso corporal dos animais permanecendo estável. Esses experimentos mostraram que as células de osteossarcoma dependem fortemente de MAT2A tanto para sua sobrevivência quanto para sua capacidade de formar tumores.
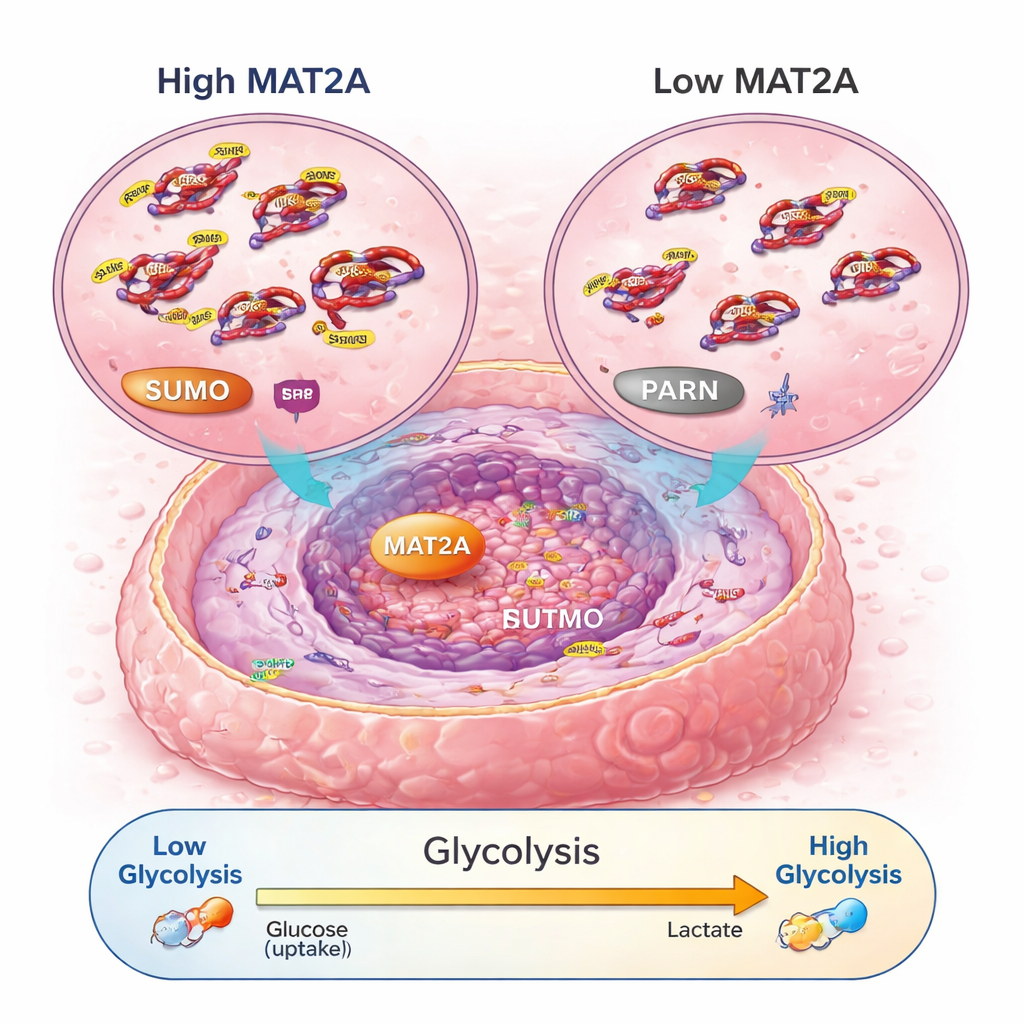
Um circuito de sinalização que aumenta o uso de combustível celular
Aprofundando, os cientistas descobriram que MAT2A faz mais do que sua função metabólica usual. No núcleo, ele se liga a um fator de transcrição chamado SRF, ajudando a manter o SRF estável e ativo ao promover uma marca química conhecida como SUMO. Por sua vez, o SRF liga um gene chamado PARN, que então ativa a bem conhecida via PI3K–AKT e aumenta a maquinaria da glicólise aeróbica — uma forma rápida, porém ineficiente, de as células produzirem energia que as células cancerosas favorecem. Quando MAT2A foi reduzido, as células cancerosas produziram menos ATP (sua moeda de energia), captaram menos glicose, produziram menos ácido lático e migraram de volta para uma respiração mais calma baseada em oxigênio. Perturbar PARN ou AKT podia anular os efeitos pró-crescimento e pró-glicólise de MAT2A, confirmando que esse circuito — MAT2A para SRF para PARN para PI3K–AKT — atua como um circuito chave de energia e crescimento no osteossarcoma.
Uma função não tradicional e um alvo passível de droga
De forma marcante, uma versão de MAT2A que carecia de sua atividade enzimática normal ainda sustentava a estabilidade do SRF e a ativação de PARN, o que significa que esse papel promotor do câncer não depende de sua reação química habitual. Em vez disso, MAT2A age mais como um andaime que organiza outras proteínas. Isso tem implicações práticas: drogas não precisam necessariamente bloquear seu centro catalítico para enfraquecer tumores. Os pesquisadores testaram um inibidor de pequena molécula chamado FIDAS-5, projetado para atingir MAT2A, tanto em culturas celulares quanto em modelos de camundongo. O tratamento reduziu o SRF nuclear, diminuiu a sinalização de PARN e PI3K–AKT, atenuou a glicólise, desacelerou o crescimento celular e desencadeou a morte das células cancerosas. Em camundongos, o FIDAS-5 reduziu ou retardou tumores sem perda de peso perceptível, sugerindo efeitos colaterais toleráveis nesse contexto.
O que isso significa para pacientes e terapias futuras
Para leigos, a mensagem central é que as células de osteossarcoma dependem de MAT2A para manter seus programas de crescimento e seus motores de queima de açúcar funcionando a plena velocidade. Ao estabilizar proteínas de controle chave e amplificar uma cadeia de sinais, MAT2A ajuda os tumores a crescerem mais rápido e se tornarem mais agressivos. Bloquear essa proteína — seja por métodos baseados em genes ou por um fármaco como o FIDAS-5 — corta esse suporte, forçando as células cancerosas a desacelerar, consumir energia de forma menos frenética e, em última análise, morrer. Embora muito trabalho ainda seja necessário antes que tais tratamentos cheguem à clínica, este estudo posiciona MAT2A como um novo alvo promissor na luta contra o câncer ósseo, abrindo um caminho potencial para terapias mais precisas e menos tóxicas para pacientes jovens.
Citação: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Palavras-chave: osteossarcoma, MAT2A, metabolismo do câncer, via PI3K AKT, terapia direcionada