Clear Sky Science · pt
Análise computacional da heterogeneidade de epítopos em imuno-colorações a partir de séries de diluição de anticorpos
Por que a qualidade da coloração por anticorpos importa
De rastrear células cancerígenas a diagnosticar infecções, a biologia moderna depende fortemente de anticorpos que “iluminam” moléculas específicas dentro das células. No entanto, muitos laboratórios enfrentam um problema recorrente: colorações fracas, ruidosas ou simplesmente enganosas. Este artigo apresenta um método prático, baseado em computador, para extrair mais informações de uma série de diluição de anticorpos rotineira, ajudando pesquisadores a ajustar suas colorações para imagens mais limpas, medições mais confiáveis e até novas formas de rotular vários alvos em um único canal de cor. 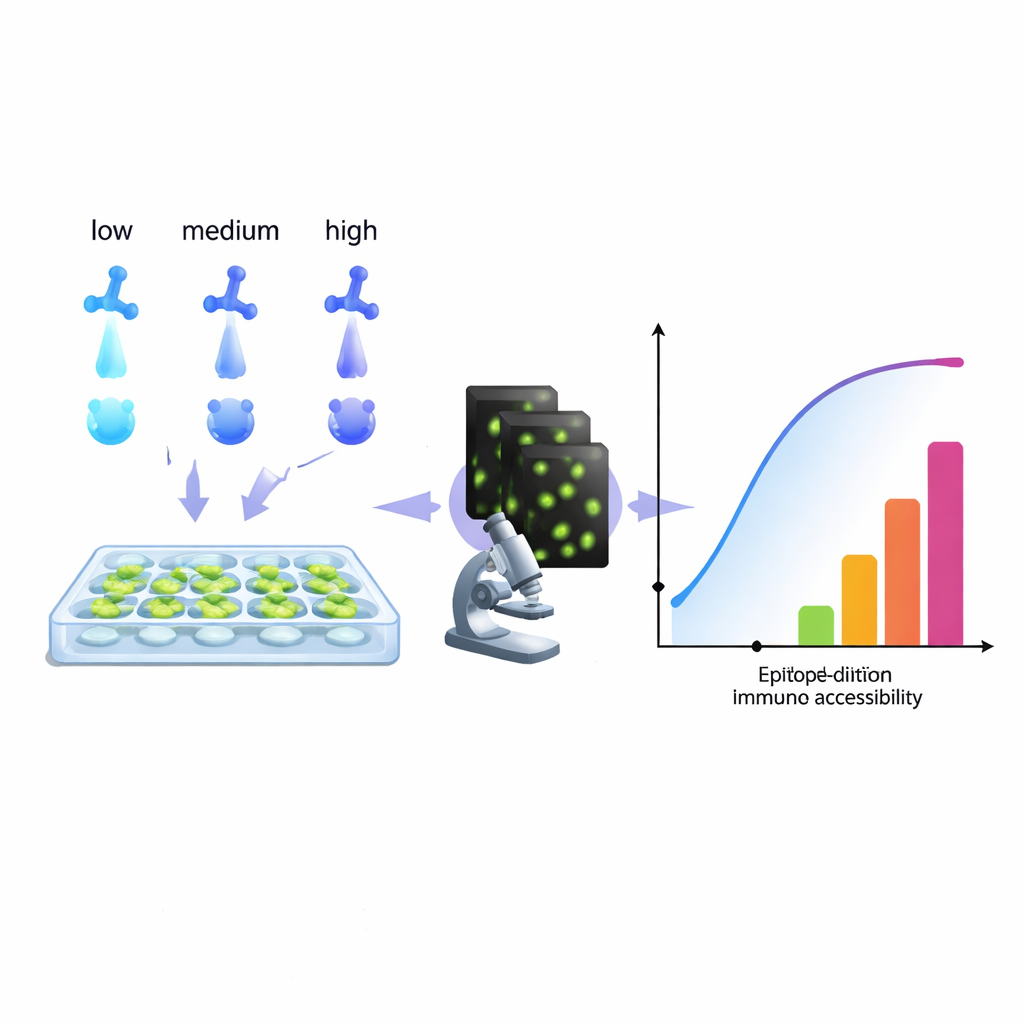
Como os cientistas normalmente ajustam colorações por anticorpos
Quando montam um experimento de imunocoloração, os pesquisadores geralmente estimam uma concentração de anticorpo a partir da ficha técnica, testam algumas diluições e escolhem a que “parece boa”. Por trás dessa escolha, porém, inúmeros fatores sutis — forma da proteína, aglomeração dentro das células, pH e a capacidade do anticorpo de se acomodar — determinam se o anticorpo permanece ligado ou é lavado. Ferramentas tradicionais que medem a ligação de anticorpos, como ressonância plasmônica de superfície, funcionam melhor com proteínas purificadas em superfícies artificiais, não em células ou tecidos densamente compactados. Isso significa que os valores obtidos podem não refletir o sistema biológico real onde o anticorpo é usado. Como resultado, laboratórios podem, sem saber, escolher concentrações que aumentam o fundo difuso ou ocultam alvos importantes, porém menos acessíveis.
Transformando séries de diluição simples em “mapas de acessibilidade”
Os autores propõem uma abordagem diferente: encarar uma série de diluição padrão como um conjunto rico de dados e ajustá-la com um modelo que reflita o que a imagem realmente observa — anticorpos que permanecem ligados mesmo após lavagens repetidas. Ao analisar como o sinal cresce com a concentração, o algoritmo deles reconstrói um “histograma de acessibilidade”. Em vez de tentar isolar constantes puras de ligação química, esse histograma agrupa sítios-alvo em “classes de epítopo” técnicas, com base em quão fáceis são de marcar em condições reais. Um mesmo epítopo biológico pode aparecer em várias classes se, por exemplo, for fácil alcançá‑lo em uma parte da célula e mais difícil em uma região congestionada. Crucialmente, esse método funciona diretamente com a leitura do microscópio, sem necessidade de proteínas purificadas ou hardware extra, de modo que qualquer laboratório capaz de executar uma série de diluição e quantificar fluorescência pode, em princípio, construir tais histogramas. 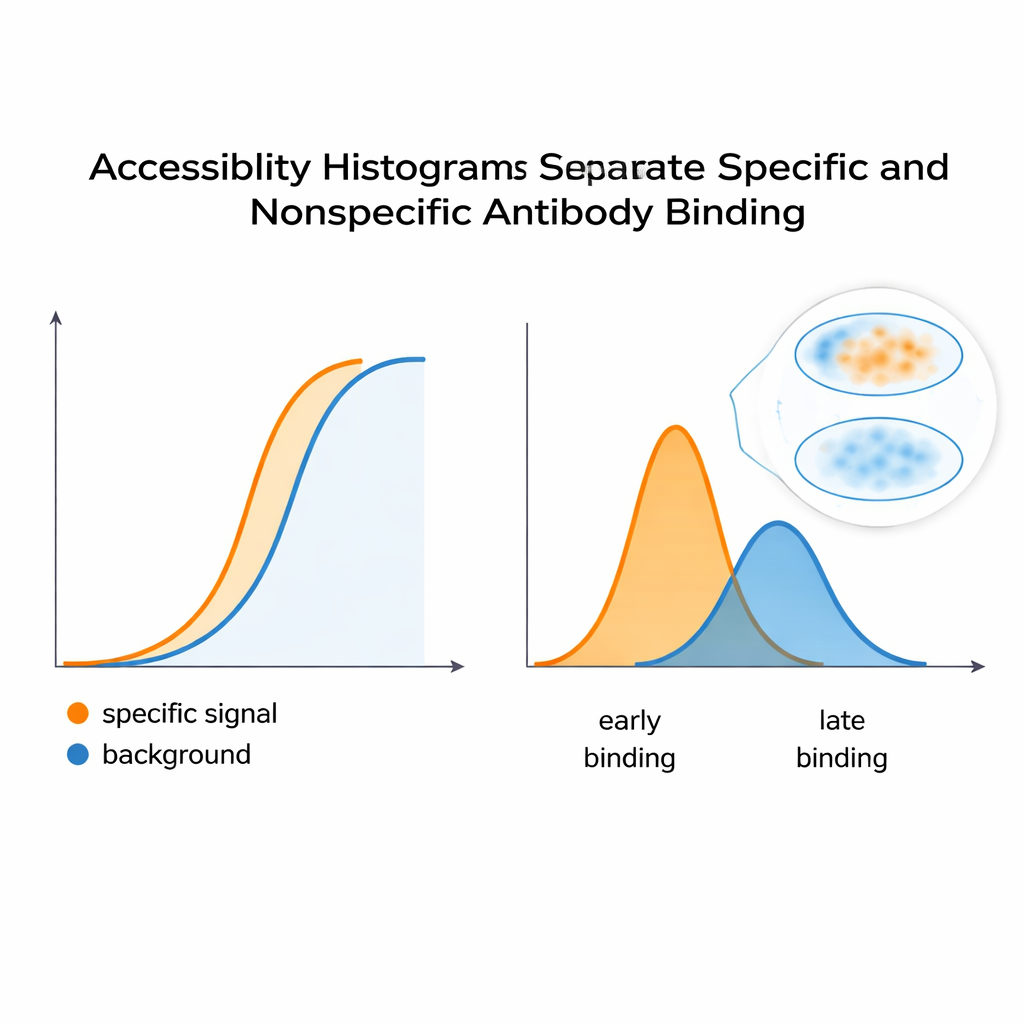
Separando sinal verdadeiro do fundo
Para testar se esses histogramas realmente capturam o comportamento da coloração, a equipe construiu um sistema controlado usando células HeLa e dois anticorpos monoclonais: um que imita um sinal desejado e específico e outro que age como um fundo indesejado. Quando misturados, a curva de fluorescência combinada parecia uma resposta única e suave — nada sugeria à vista a existência de dois contribuintes distintos. Mas a análise computacional dividiu essa curva em picos separados no histograma de acessibilidade, revelando pelo menos duas classes de epítopo subjacentes. Uma estratégia semelhante, aplicada a um anticorpo que reconhece um sítio sensível à conformação em uma subunidade reguladora da PKA, mostrou que mudanças na conformação da proteína — desencadeadas por uma molécula chamada cAMP — deslocaram a distribuição de epítopos acessíveis. Isso sugere que o método pode sinalizar quando estruturas proteicas se abrem ou se fecham, alterando a facilidade com que anticorpos se ligam dentro das células.
Escolhendo diluições melhores e marcando mais com uma cor
Como cada pico no histograma de acessibilidade contribui principalmente em uma faixa de concentração específica, os autores usam esses picos como guia para escolher diluições “ideais”. Picos de baixa acessibilidade que aparecem apenas em níveis muito altos de anticorpo provavelmente incluem ligação não específica, enquanto picos iniciais frequentemente refletem o alvo pretendido. Ao modelar como picos individuais constroem a curva geral de dose–resposta, a equipe pode sugerir diluições que maximizam o sinal específico antes que picos problemáticos entrem em cena — às vezes muito mais diluídas do que as recomendações do fornecedor. Eles estendem ainda essa ideia para uma forma engenhosa de “multiplexagem computacional”. Marcando a mesma amostra fixa repetidamente com concentrações cuidadosamente escolhidas, imageando após cada rodada e subtraindo imagens anteriores das posteriores, isolam sinais ligados a diferentes classes de acessibilidade, efetivamente separando múltiplos alvos dentro de um único canal de fluorescência.
O que isso significa para o trabalho diário de laboratório
Em termos práticos, este trabalho transforma um passo rotineiro de solução de problemas — executar uma série de diluição de anticorpos — em uma ferramenta quantitativa. Os histogramas de acessibilidade ajudam cientistas a identificar complexidade oculta nas suas colorações, escolher diluições que reduzem o fundo enganoso e, em alguns casos, separar sinais sobrepostos sem precisar de marcadores fluorescentes adicionais. Embora o modelo subjacente seja intencionalmente simples e não capture todos os detalhes moleculares, ele foi projetado para ser fácil de usar e robusto o suficiente para dados do mundo real. Se amplamente adotada, essa abordagem pode tornar técnicas baseadas em anticorpos — desde imagens básicas até ensaios diagnósticos — mais confiáveis, mais informativas e menos dependentes de tentativa e erro.
Citação: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
Palavras-chave: coloração por anticorpo, imunofluorescência, acessibilidade de epítopos, resposta à dose, multiplexagem computacional