Clear Sky Science · pt
Avanços estratégicos para estudos estruturais por cryo-EM de pequenas GPCRs (<100 kDa)
Por que pequenos interruptores celulares importam para a medicina
Muita da medicina moderna atua ao manipular discretamente pequenos interruptores na membrana das nossas células, chamados receptores acoplados à proteína G (GPCRs). Esses interruptores detectam hormônios, odores e fármacos — e cerca de um terço de todos os medicamentos aprovados age sobre eles. Para projetar fármacos mais seguros e inteligentes, os cientistas precisam de imagens 3D detalhadas desses receptores, especialmente em suas formas “desligadas” ou inativas, que são o alvo de muitos fármacos. Este artigo explica como pesquisadores estão aprendendo a visualizar alguns dos menores GPCRs com crio‑microscopia eletrônica (cryo‑EM), um método de imagem poderoso que observa moléculas congeladas em um estado próximo ao natural.
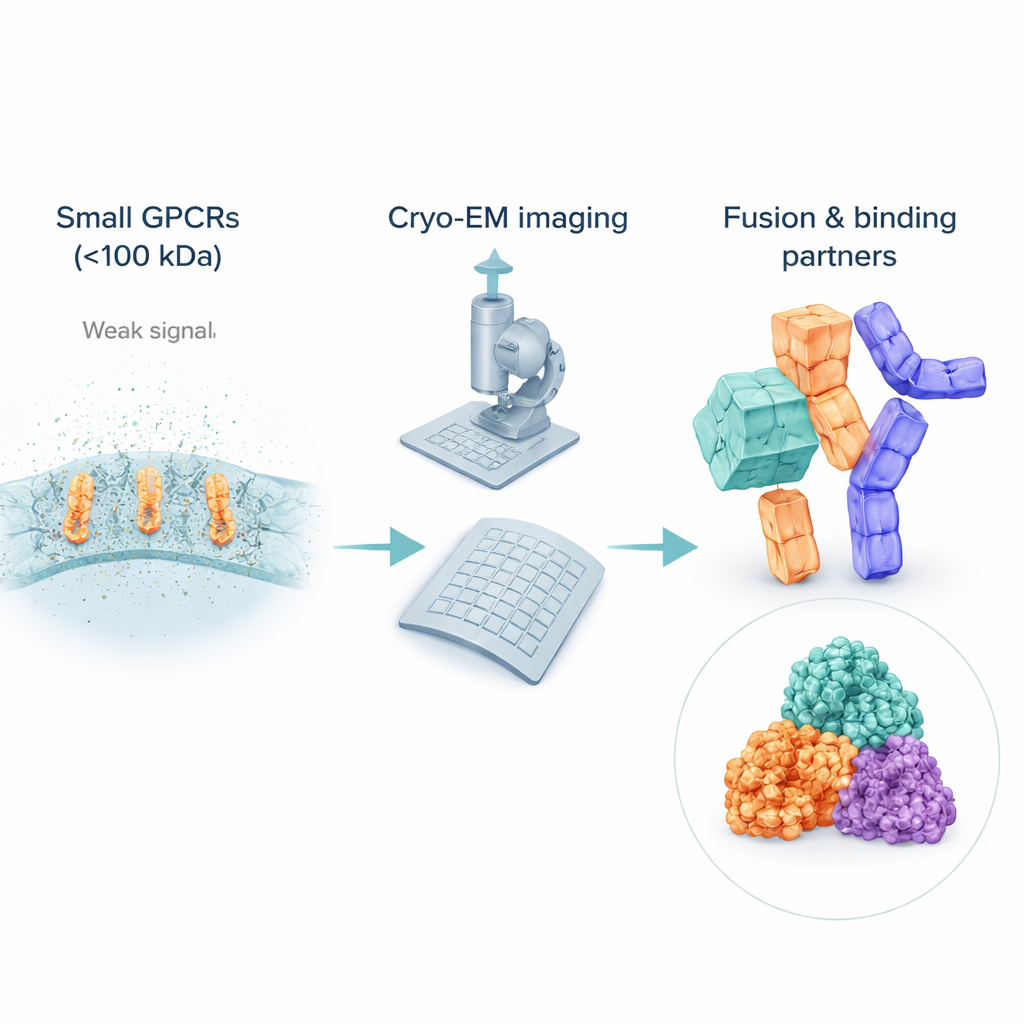
O desafio de ver receptores muito pequenos
Embora a cryo‑EM tenha revolucionado a biologia estrutural, ela ainda encontra dificuldades com moléculas pequenas e flexíveis. Muitos GPCRs inativos pesam bem menos que 100 kilodaltons, o que os torna difíceis de detectar e alinhar em imagens ruidosas. Para mantê‑los solúveis, os cientistas os envolvem em bolhas de detergente ou mimetizadores de lipídios, que podem na verdade parecer “maiores” ao feixe de elétrons do que o próprio receptor, abafando o sinal da proteína de interesse. Ao contrário dos receptores ativos, ligados a parceiros volumosos como proteínas G, os GPCRs inativos frequentemente carecem de características externas proeminentes, de modo que os computadores têm dificuldade para combinar muitas imagens em uma visão 3D nítida. Como resultado, a maioria das estruturas de GPCR inativos ainda vem de métodos mais antigos de raios X, deixando uma lacuna na cobertura por cryo‑EM exatamente onde muitos fármacos atuam.
Aumentando o tamanho dos receptores com ajudantes integrados
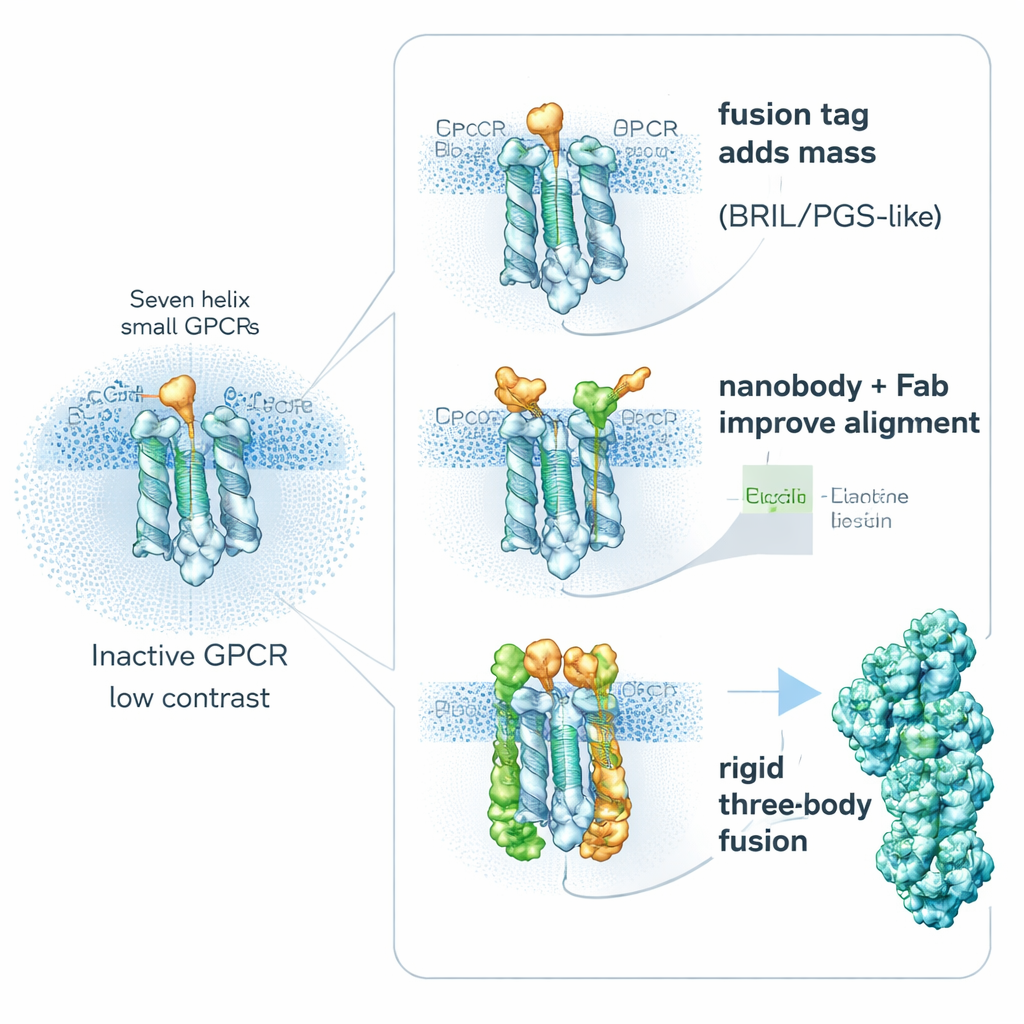
Uma estratégia-chave é surpreendentemente simples: tornar o receptor intencionalmente “mais pesado”. Pesquisadores fundem geneticamente pequenas proteínas auxiliares estáveis em partes flexíveis dos GPCRs para aumentar seu tamanho e rigidez, sem bloquear as regiões importantes de ligação de fármacos. Ajudantes populares incluem BRIL (um feixe de quatro hélices), PGS (um fragmento de enzima termicamente estável) e uma proteína maior em forma de braçadeira chamada calcineurina. Esses parceiros de fusão costumam ser inseridos em uma alça interna móvel que conecta duas hélices. Ao rigidificar essa região, reduzem‑se os borrões causados pelo movimento molecular e fornecem formas reconhecíveis que ajudam os computadores a alinhar as partículas. Estudos mostram que a posição e a orientação exatas do pedaço fundido podem determinar o sucesso do projeto: em um receptor, uma etiqueta PGS colocada em posição diferente melhorou a resolução de um embaçado de 6 angstroms para um muito mais claro de 3,7 angstroms.
Emprestando anticorpos e ligantes projetados como alças
Uma segunda via evita inserir grandes fusões no receptor e, em vez disso, fixa “alças” de alta afinidade por fora. Pequenos fragmentos de anticorpos chamados nanobodies e ligantes relacionados podem ser levantados para reconhecer GPCRs inativos e se prender a alças internas flexíveis. Um exemplo marcante é o Nanobody‑6, criado inicialmente como sensor para um receptor opioide e depois reutilizado, com ajustes modestos, para estabilizar vários outros GPCRs em suas formas inativas. Por se ligar deslocado do centro, ele oferece a cada partícula uma pista clara de orientação, tornando a média de imagens mais confiável. Pesquisadores frequentemente estendem essa ideia adicionando uma segunda camada — um fragmento de anticorpo convencional que reconhece o nanobody em si — criando um complexo mais volumoso e rígido que aparece nitidamente na cryo‑EM. Outros ligantes projetados, como DARPins, podem ser usados como espaçadores modulares ou como conectores a gaiolas proteicas maiores, ampliando ainda mais o sinal de alvos muito pequenos.
Projeto de amostras mais inteligente e processamento de imagem com reforço de IA
Fundir ajudantes ou adicionar ligantes é apenas parte da história. A revisão enfatiza que boas estruturas começam com constructos de receptor cuidadosamente projetados: aparar regiões terminais soltas, introduzir mutações estabilizadoras e usar ferramentas modernas de predição estrutural para identificar partes propensas a causar problemas. Na parte de imageamento, truques mais antigos como placas de fase, que aumentam o contraste para partículas tênues, estão sendo complementados ou mesmo substituídos por ferramentas de inteligência artificial. Programas de deep learning conseguem identificar partículas minúsculas escondidas em micrografias ruidosas, e novos algoritmos podem classificar imagens em diferentes conformações quando receptores amostram múltiplos estados. Juntamente com ajudantes fiduciais, esses avanços empurram a cryo‑EM na direção de resolver de forma confiável proteínas de membrana que antes eram consideradas pequenas demais ou muito dinâmicas para estudar.
O que isso significa para fármacos futuros
O artigo conclui que não existe um único ajudante “mágico” que funcione para todos os receptores, mas um conjunto de ferramentas em crescimento — parceiros de fusão, ligantes semelhantes a anticorpos e métodos guiados por IA — vem abrindo de forma constante a paisagem inativa dos GPCRs para a cryo‑EM. Para não especialistas, a conclusão essencial é que, ao fazer pequenos receptores parecerem maiores e mais ordenados ao microscópio, os cientistas finalmente podem obter imagens detalhadas das formas exatas às quais muitos fármacos preferem se ligar. Esses roteiros estruturais devem acelerar o projeto de medicamentos que desliguem esses interruptores celulares com mais precisão — ou ajustem finamente sua atividade — com menos efeitos colaterais.
Citação: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Palavras-chave: Receptores acoplados à proteína G, crio-microscopia eletrônica, descoberta de fármacos, biologia estrutural, andaimes de nanobody