Clear Sky Science · pt
Ligando tensão molecular e trações celulares: uma abordagem multiescala para a mecânica das adesões focais
Como as Células Sentem e Puxam seu Ambiente
Cada vez que uma célula se move, se divide ou remodela um tecido, ela puxa discretamente seu entorno. Essas pequenas forças mecânicas são cruciais na cicatrização, na disseminação do câncer e no desenvolvimento de órgãos, mas são difíceis de visualizar e ainda mais de medir. Este estudo apresenta uma nova maneira de observar essas forças por dois ângulos ao mesmo tempo: o quanto uma célula inteira puxa um material macio e quanto força carregam as “molhinhas moleculares” individuais dentro dos pontos de ancoragem da célula. Ao vincular essas perspectivas, o trabalho ajuda a explicar como as células detectam rigidez e regulam sua aderência ao mundo ao redor.
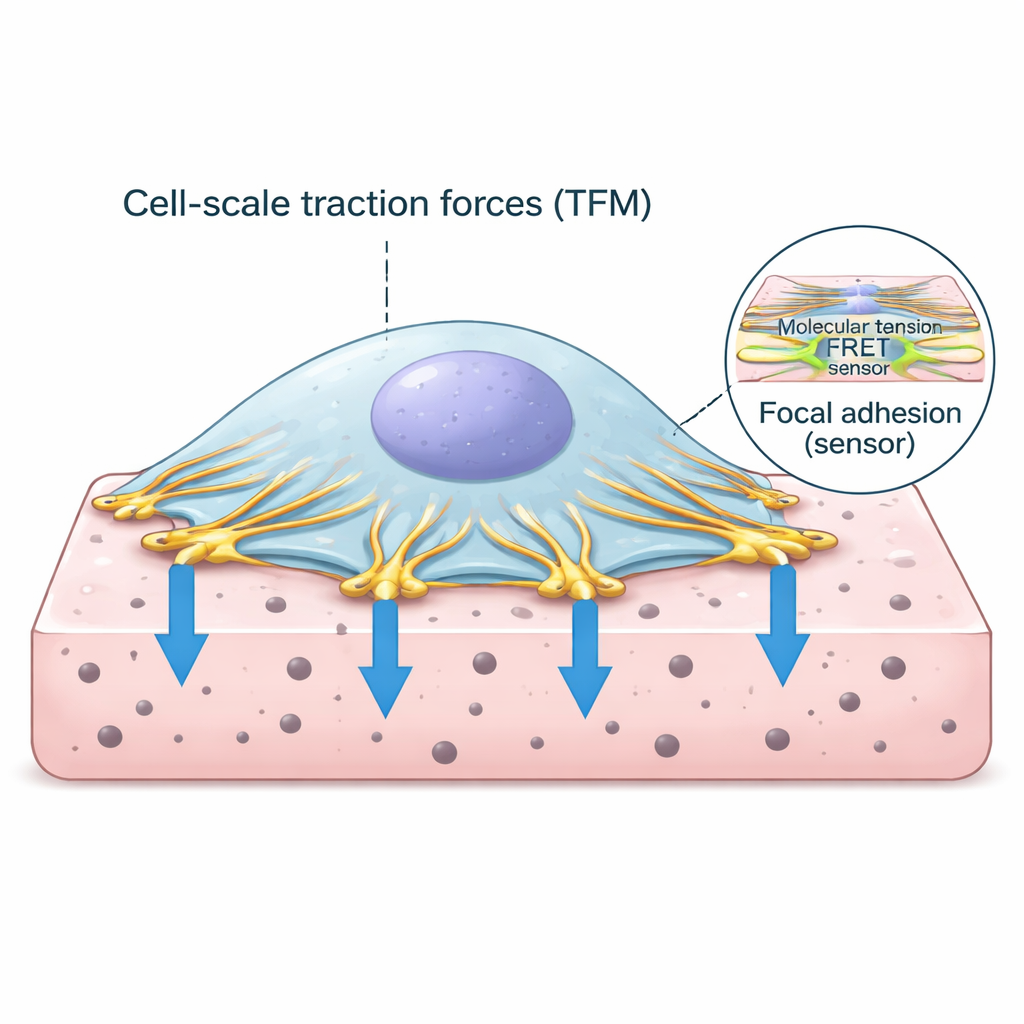
Os Pontos de Aderência da Célula ao Mundo Externo
As células não flutuam simplesmente nos tecidos; elas se ancoram por pontos de contato especializados chamados adesões focais. Nesses locais, o andaime interno de fibras de actina da célula conecta-se a proteínas que atravessam a membrana celular e se prendem à matriz circundante. Uma das proteínas-chave nesse complexo de ancoragem é a vinculina, que funciona como um elo sensível à força. Quando a maquinaria contrátil da célula puxa a actina, a vinculina percebe a carga e ajuda a reforçar a conexão. Entender quanto de força passa por esses elos, e como isso se relaciona com a tração geral da célula, é central para decifrar como os tecidos se mantêm saudáveis ou se tornam doentes.
Duas Janelas para a Força Celular
Os pesquisadores combinaram duas técnicas poderosas em um único fluxo de trabalho. Primeiro, a microscopia de força de tração mede quanto uma célula deforma um substrato macio e gelatinoso acompanhando o movimento de minúsculas esferas fluorescentes no gel. A partir desses deslocamentos das esferas, é possível calcular a distribuição das forças de empuxo e tração sob a célula. Segundo, uma vinculina especialmente projetada carrega um sensor de tensão fluorescente que muda seu sinal luminoso quando é esticado. Usando imageamento avançado de tempo de vida (lifetime), a equipe converteu esse sinal de luz em uma leitura da tensão molecular sobre a vinculina. Eles desenharam hidrogéis finos e planos que podiam ser imageados em alta resolução e escreveram software personalizado para alinhar, segmentar e analisar ambos os conjuntos de dados até o nível de pontos de adesão individuais.
Como a Rigidez Muda o Esforço da Célula
Quando as células foram cultivadas em géis macios versus mais rígidos, seu comportamento geral mudou de forma clara. Em substratos mais rígidos, as células se espalharam mais e exerceram forças de tração mais fortes na superfície do gel. Ao mesmo tempo, a leitura fluorescente do sensor de vinculina indicou maior tensão molecular dentro das adesões focais. Curiosamente, as características estruturais básicas dessas adesões — como o número ou o tamanho médio — não mudaram muito entre os géis macios e rígidos. Em vez disso, mudou a organização das forças. Adesões grandes, orientadas radialmente e com mais vinculina tendiam a carregar tração maior, sugerindo que tanto a geometria quanto a composição molecular desses locais ajudam a definir o quanto a célula puxa.
Uma Relação Complexa entre Forças Locais e Moleculares
Ao examinar com mais detalhe adesões individuais, revelou-se que a ligação entre tração local e tensão na vinculina não é universal. Em algumas células, adesões que geravam maior tração também exibiam maior tensão na vinculina, o que implica que contatos engajados e portadores de carga distribuem a força mais diretamente através de seus elos moleculares. Em outras células, apareceu o padrão oposto: regiões de tração forte associavam-se a menor tensão em vinculina, enquanto outras adesões suportavam mais carga molecular sem produzir grandes puxões para fora. Muitas células não mostraram padrão claro algum. Esses comportamentos distintos provavelmente refletem diferentes estados celulares — como espalhamento ativo, adesão estável ou retração — e sugerem que as células podem redistribuir forças através de sua rede de adesões de várias maneiras.
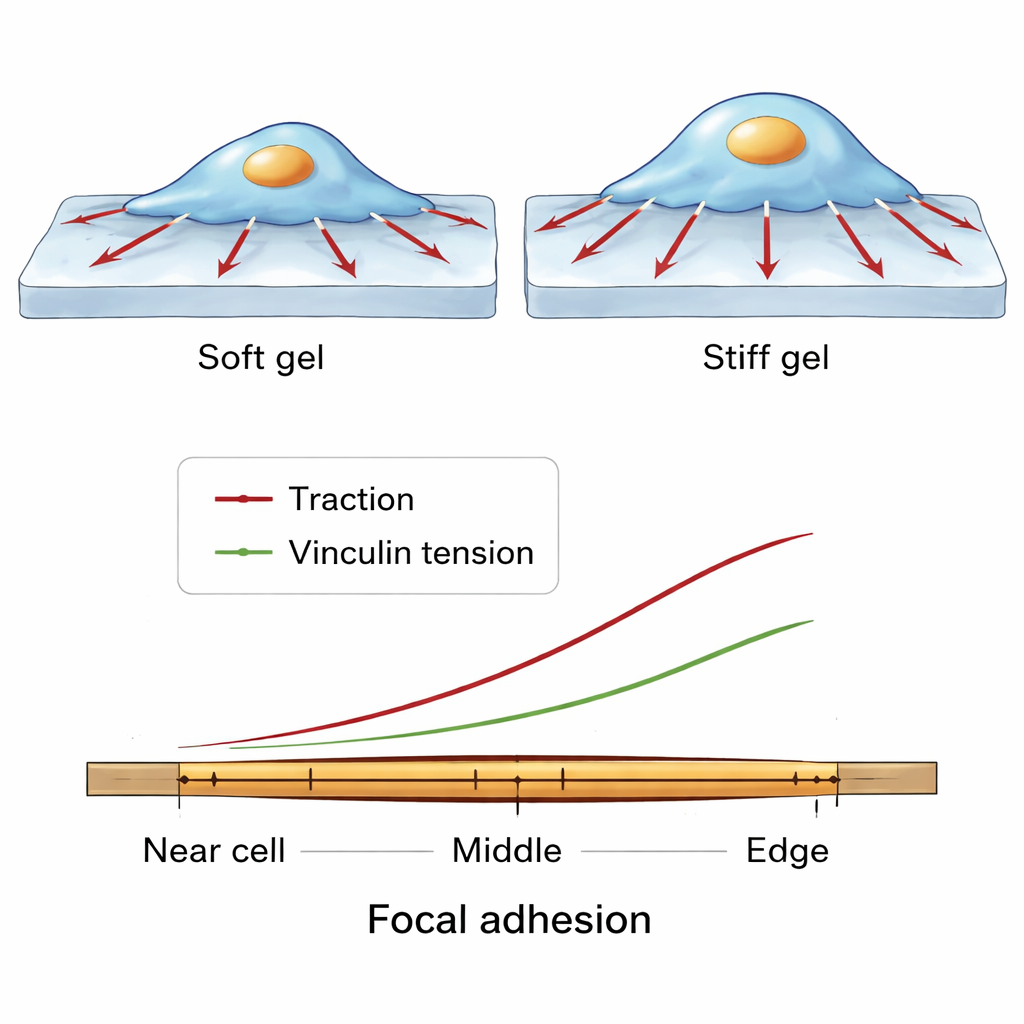
Padões de Força em Escala Fina ao Longo de um Único Ponto de Aderência
A equipe então aumentou ainda mais a resolução, examinando como as forças variam ao longo do comprimento de uma única adesão focal, do lado mais próximo do centro da célula até a borda junto ao perímetro celular. Através de muitas células e condições, emergiu um padrão consistente. As moléculas de vinculina estavam mais densamente agrupadas em direção ao meio da adesão. Contudo, tanto a tração exercida no substrato quanto a tensão molecular sobre a vinculina aumentavam em direção à extremidade externa, mais periférica. Isso sugere um ato de equilíbrio: em regiões centrais, muitas moléculas de vinculina podem compartilhar a carga, de modo que cada uma sente menos tensão, enquanto na borda externa menos moléculas carregam relativamente mais força, suportando um puxão local forte ao mesmo tempo que mantêm a adesão intacta.
O Que Isso Significa para Saúde e Doença
Ao unir mapas de tração de célula inteira com medições de tensão ao nível proteico, este estudo oferece um retrato multiescala de como as células gerenciam sua pega mecânica. O trabalho mostra que, à medida que o ambiente se torna mais rígido, as células tanto puxam com mais força quanto carregam mais suas ligações de vinculina, mas que a relação detalhada entre forças externas e tensão molecular varia de adesão para adesão e de célula para célula. Ao mesmo tempo, um padrão espacial robusto de distribuição de forças dentro de adesões individuais parece ser conservado. Para um público não especializado, a mensagem principal é que as células ajustam com precisão tanto onde quanto como puxam, redistribuindo forças por muitas pequenas “molhas” moleculares para se adaptar a diferentes ambientes mecânicos — um princípio que pode sustentar processos tão diversos quanto desenvolvimento de tecidos, fibrose e invasão cancerígena.
Citação: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
Palavras-chave: mecânica celular, adesões focais, vinculina, microscopia de força de retração, mecanotransdução