Clear Sky Science · pt
Dinâmica temporal da clivagem colateral de RNA por LbuCas13a em células humanas
Transformando uma defesa bacteriana em um interruptor de autodestruição preciso
Pesquisadores descobriram uma maneira de converter uma proteína imune bacteriana em um interruptor de “autodestruição” altamente seletivo para células humanas. Ao aproveitar uma enzima CRISPR chamada LbuCas13a, eles conseguem reconhecer uma mensagem de RNA escolhida dentro da célula e então degradar quase todo o restante do RNA dessa célula. Para leitores não especializados, isso é instigante porque as mensagens de RNA controlam quais proteínas a célula produz; aprender a apagá‑las sob demanda abre portas para novos tratamentos contra o câncer, estratégias antivirais e ferramentas de pesquisa poderosas.
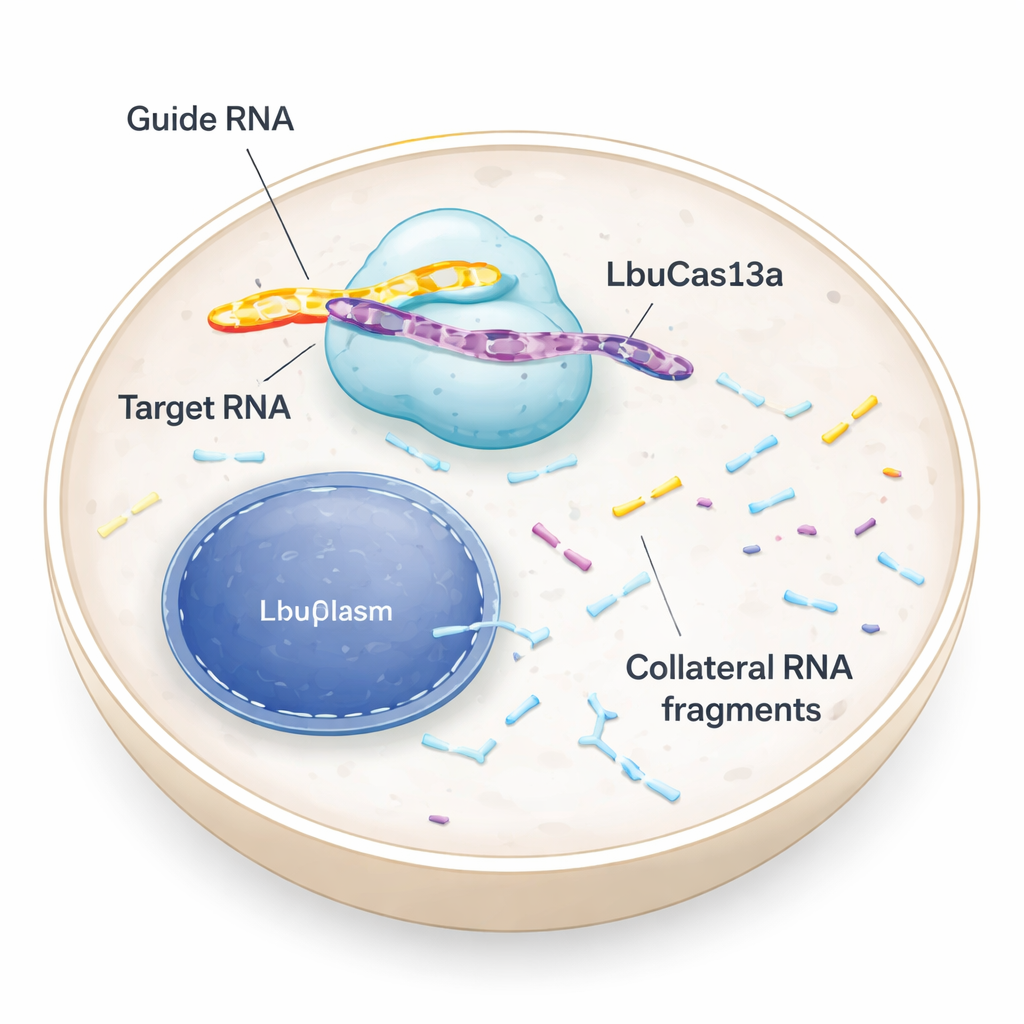
Uma tesoura molecular que mira RNA, não DNA
A maioria das pessoas já ouviu falar de ferramentas CRISPR que cortam DNA, reescrevendo o código genético. LbuCas13a é diferente: ela reconhece e corta RNA, as mensagens temporárias que carregam instruções do DNA até as fábricas de proteínas da célula. Em bactérias, enzimas Cas13 fazem parte da defesa antiviral. Uma vez que detectam um RNA viral, elas não apenas fatiam esse invasor, mas também começam a cortar muitos outros RNAs próximos. Essa atividade “colateral” pode levar células infectadas à dormência ou à morte, ajudando a proteger a comunidade bacteriana. Testes iniciais em células de animais e humanas sugeriam que o corte colateral do Cas13 era fraco ou ausente, de modo que a enzima era usada principalmente como um “desligador” preciso de RNA. O novo estudo revisita essa suposição e mostra que, sob condições certas, a atividade colateral em células humanas pode ser tanto forte quanto útil.
Desencadeando o corte colateral em células humanas
A equipe comparou várias variantes de Cas13 e descobriu que LbuCas13a era especialmente potente. Eles entregaram proteína LbuCas13a purificada pré-carregada com um pequeno RNA guia diretamente em células humanas, uma forma de “injeção” molecular de proteína chamada entrega de ribonucleoproteína (RNP). Quando o guia correspondia a um RNA alvo — como um gene marcador fluorescente ou mensagens naturais abundantes como GAPDH e RNA ribossômico 18S — a enzima primeiro fatiou esse alvo e então começou a degradar muitos outros RNAs. Em aproximadamente 50 minutos, o perfil geral de RNA da célula mudou dramaticamente, com fragmentos de clivagem distintos aparecendo. Esse efeito colateral foi observado com diferentes métodos de entrega e em uma variedade de tipos celulares, mostrando que não era uma peculiaridade de uma linhagem celular ou de um alvo artificial.
Da fragmentação de RNA à morte celular e seleção
O que acontece com uma célula cujas mensagens de RNA desaparecem repentinamente? Usando imagem de células vivas, os pesquisadores observaram que células que expressavam o RNA alvo gradualmente entravam em apoptose, uma forma organizada de morte celular programada marcada por sinais característicos de “alarme precoce” antes da célula se fragmentar. Importante, células vizinhas que não expressavam o RNA alvo permaneceram em grande parte inalteradas, demonstrando que a autodestruição é específica. O grupo então explorou essa propriedade como uma ferramenta de seleção. Quando misturaram células portadoras do alvo com células normais e ativaram LbuCas13a, as células com o alvo foram seletivamente depletadas ao longo de vários dias. Repetir o tratamento várias vezes reduziu ainda mais sua fração. Eles mostraram que isso poderia enriquecer por células com edição gênica bem‑sucedida e também ser ajustado para atacar células cancerosas que superproduzem um oncogene, aqui CDK4, enquanto poupava células relacionadas que produzem muito menos desse RNA.
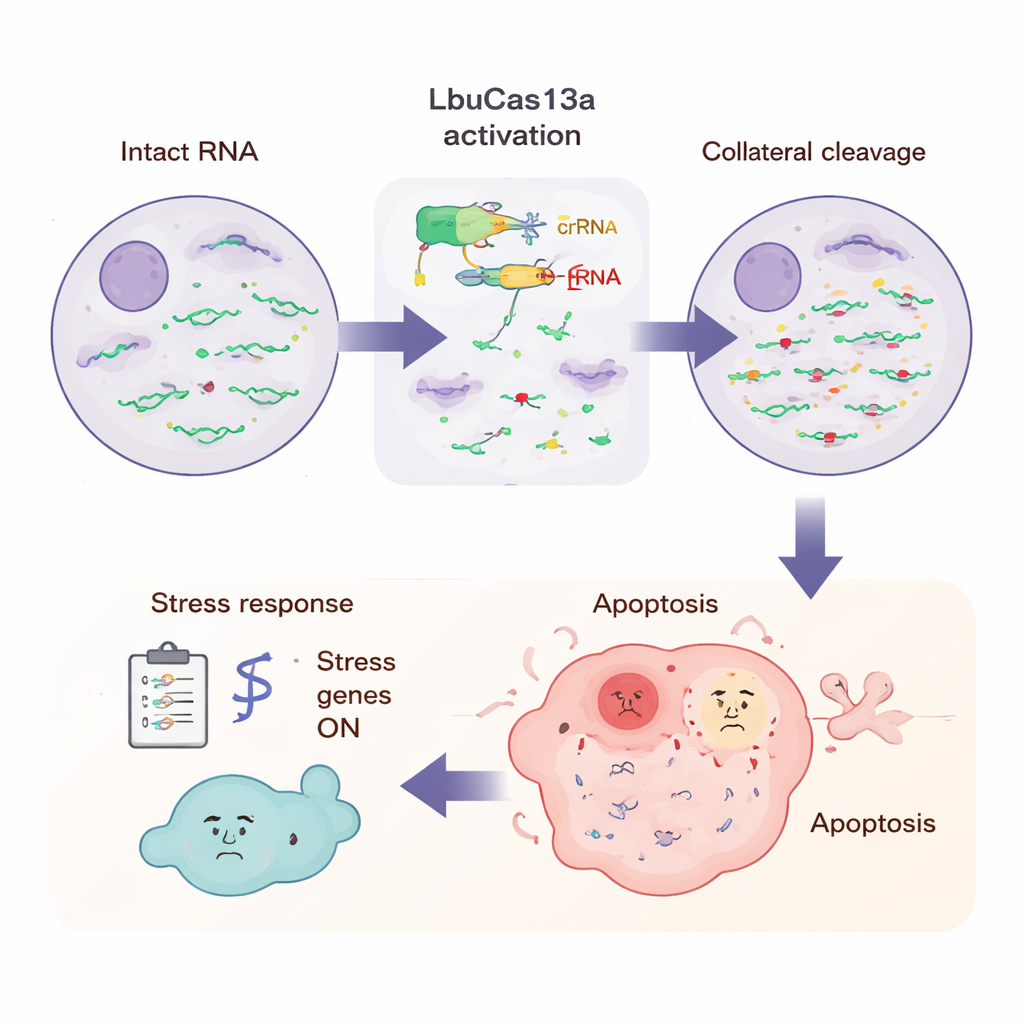
O que a célula experimenta durante o ataque
Para ver o panorama completo, os cientistas mediram todos os RNAs na célula em vários pontos temporais após a ativação de LbuCas13a. Ao adicionar padrões de RNA conhecidos como controle, puderam determinar que a maioria dos RNAs codificadores de proteína no citoplasma caiu mais da metade em poucas horas, enquanto certos RNAs — como mensagens mitocondriais e alguns RNAs não codificadores nucleares — foram em grande parte poupados. Sequenciamento de leitura longa revelou que a clivagem ocorria em posições nucleotídicas repetidas e específicas, frequentemente em regiões de laço flexível do RNA ricas na base uracila, correspondendo a padrões vistos em experimentos em tubo de ensaio. Em pontos temporais mais tardios, muitos genes de estresse e de imunidade inata foram ativados, incluindo aqueles ligados a sinais inflamatórios e defesas antivirais. Esse padrão sugere que a célula percebe o súbito afluxo de extremidades de RNA quebrado de maneira semelhante à detecção de uma infecção viral, acionando um programa de alarme que culmina em apoptose.
Por que isso importa e para onde pode levar
Em termos simples, o estudo mostra que LbuCas13a pode ser transformada em um “interruptor letal” guiado por RNA para células: se uma célula produz em excesso um RNA particular, ativar LbuCas13a contra esse RNA provoca perda quase global de RNA, um alarme tipo imune e então morte celular controlada. Como o processo depende fortemente da abundância do RNA alvo, ele poderia ser usado para eliminar células que superexpressam genes prejudiciais — como certas células cancerosas — ou para limpar células indesejadas em culturas mistas durante pesquisas ou na fabricação de terapias celulares. Ao mesmo tempo, o trabalho é um alerta: ferramentas CRISPR voltadas ao RNA podem ter efeitos colaterais poderosos que precisam ser cuidadosamente gerenciados. Entender quando e como a clivagem colateral de RNA ocorre é essencial para usar com segurança as tecnologias Cas13 na medicina e na biotecnologia.
Citação: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Palavras-chave: CRISPR-Cas13, clivagem de RNA, morte celular, direcionamento do câncer, ferramentas de edição gênica