Clear Sky Science · pt
Percepções estruturais sobre o tráfego de metaloclustres no andaime de montagem da nitrogenase NifEN
Como a Natureza Constrói uma Ferramenta Química Poderosa
O nitrogênio está por toda parte no ar, mas a maior parte dos seres vivos não consegue utilizá‑lo nessa forma. Uma enzima especial chamada nitrogenase resolve esse problema convertendo o nitrogênio atmosférico em amônia, um ingrediente fundamental para a vida e para fertilizantes. No centro da nitrogenase fica um denso “cluster” metálico que realiza a química pesada, mas como as células montam essa peça intrincada permaneceu obscuro. Este artigo espreita dentro desse processo de construção, revelando como uma proteína andaime chamada NifEN atua como um cais flexível e um sistema transportador para a carga metálica do cluster.
Uma Fábrica Molecular por Trás do Fertilizante e dos Combustíveis
A nitrogenase é a contraparte natural dos processos industriais que produzem amônia e combustíveis líquidos. Em vez de reatores gigantes, microrganismos usam uma máquina proteica compacta impulsionada pela energia celular. Seu desempenho depende de um centro metálico singularmente complexo, construído a partir de ferro, enxofre, molibdênio, carbono e um grupo orgânico lateral. Montar esse núcleo é delicado demais para deixar ao acaso, então as células empregam uma equipe de proteínas auxiliares em revezamento. Uma das mais importantes é a NifEN, que recebe um precursor quase completo composto apenas por ferro (chamado L‑cluster), ajuda a convertê‑lo na forma madura (o M‑cluster) e então o entrega à enzima nitrogenase ativa. Entender como a NifEN gerencia esse tráfego pode informar esforços para projetar micróbios que produzam fertilizantes mais limpos ou novos combustíveis à base de carbono.
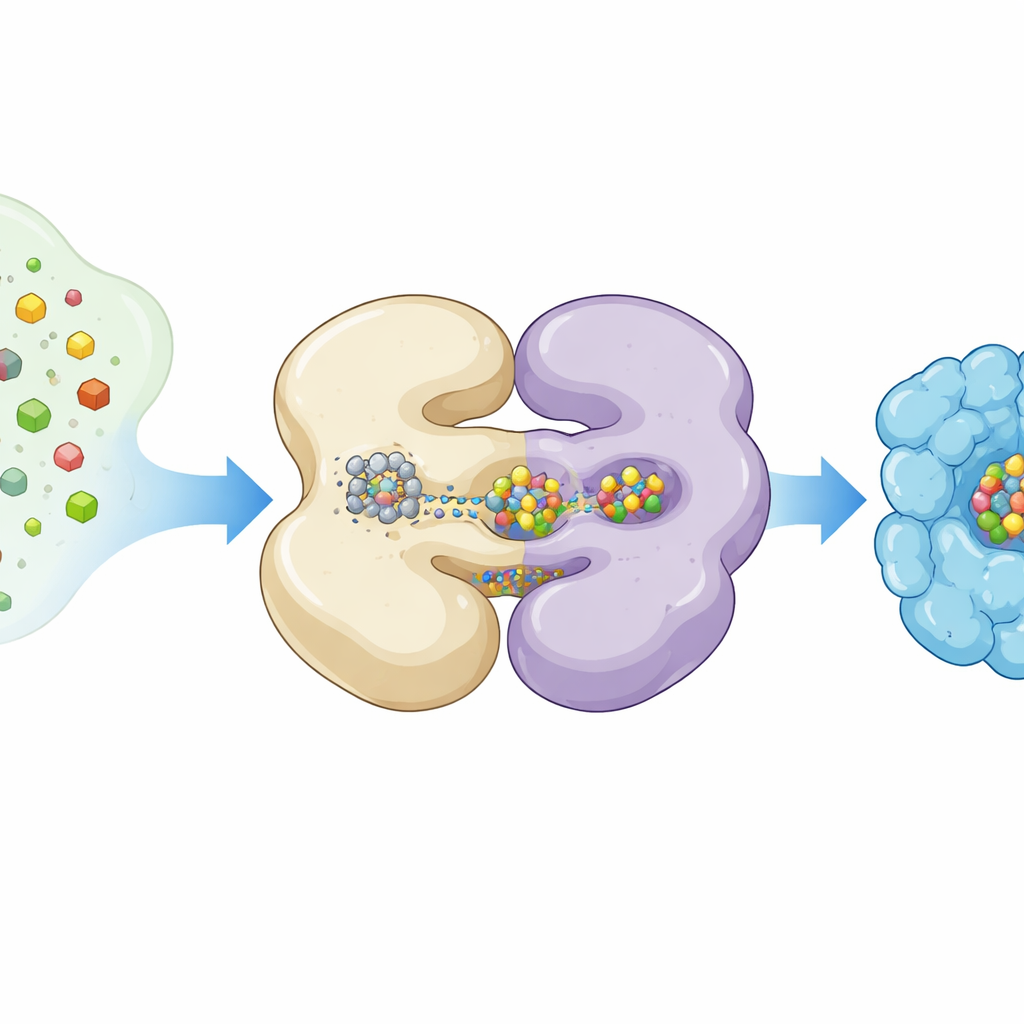
Vendo uma Máquina em Movimento com Instantâneos Congelados
Os autores usaram criomicroscopia eletrônica, uma técnica que imagina proteínas em temperaturas extremamente baixas, para capturar a NifEN em diferentes poses de trabalho. Eles expressaram NifEN em bactérias de laboratório de modo que algumas cópias da proteína carregassem um L‑cluster e outras ficassem vazias. Ao classificar milhões de imagens de partículas individuais, reconstruíram duas formas principais: uma forma “apo” sem o cluster móvel e uma forma “holo” com o cluster ligado em um sítio interno. Ambas as formas compartilham um núcleo formado por quatro subunidades organizadas em dois pares, mas quando o L‑cluster está presente, uma metade da NifEN torna‑se visivelmente mais ordenada e várias hélices giram para dentro, apertando‑se ao redor da carga metálica.
Um Túnel Oculto para a Carga Metálica
Comparar as estruturas vazia e carregada revelou uma característica marcante: um longo túnel que atravessa o dímero de NifEN. No estado vazio, essa passagem é ampla e aberta; após a ligação do cluster ela se estreita à medida que a proteína prende seu passageiro. Estruturas cristalinas anteriores haviam mostrado uma posição alternativa “externa” para o L‑cluster perto da superfície proteica. Ao juntar todas as visões, os pesquisadores inferiram que o cluster pode ocupar pelo menos dois pontos na NifEN — um enterrado no interior e outro exposto — e mover‑se entre eles ao longo de um trajeto curvo controlado por mudanças em um domínio flexível. Esse movimento parece ser mais relaxado do que na nitrogenase final, cuja unidade ativa é mantida rigidamente no lugar, sugerindo que a NifEN foi construída para a transferência e não para a catálise de longo prazo.
Parceiros de Acoplamento e uma Rota Contínua
Para entender como a NifEN se conecta aos seus parceiros a montante e a jusante, a equipe combinou suas estruturas experimentais com modelos computacionais do AlphaFold 3 e imagens de microscopia eletrônica de menor resolução de complexos proteicos. Os modelos sugerem que a enzima NifB, que fabrica o L‑cluster a partir de peças menores de ferro‑enxofre, se acopla em um vale em uma face da NifEN. Ali, um túnel contínuo pode ser traçado desde os próprios centros metálicos da NifB diretamente para o túnel da NifEN e até a estação interna do L‑cluster. Na face oposta da NifEN, um sítio de acoplamento diferente acomoda a NifH, a proteína que insere o molibdênio e um grupo orgânico lateral para completar o cofator. Nessa configuração, o L‑cluster fica na posição superficial, idealmente posicionado para modificação. Mutar aminoácidos chave que revestem a rota proposta perturba o carregamento, o movimento ou a maturação do cluster, fornecendo suporte experimental para esse modelo de esteira transportadora.
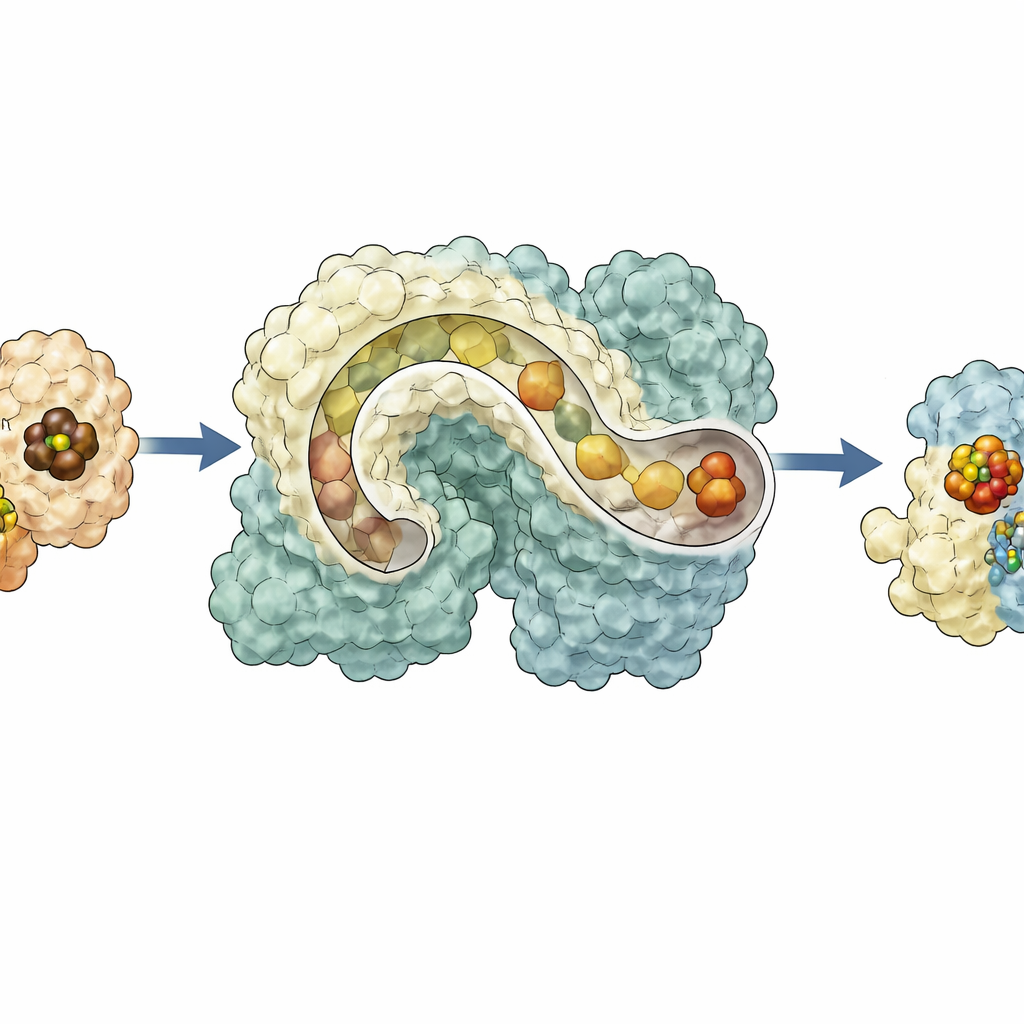
Por Que um Andaime Flexível Importa
Tomados em conjunto, os resultados pintam a NifEN como um centro dinâmico que recebe um núcleo metálico da NifB de um lado, desloca‑o para uma baia interna de espera, e então o apresenta na superfície oposta para acabamento pela NifH antes de guiar o cluster maduro de volta para o interior para entrega à nitrogenase. Esse esquema de tráfego regulado por conformação explica como múltiplas etapas delicadas podem ser coordenadas dentro de uma única estrutura proteica e sugere como enzimas antigas podem ter evoluído de andaimes mais flexíveis para os catalisadores altamente especializados de hoje. Para não‑especialistas, o trabalho mostra que, mesmo na escala nanométrica, a natureza depende de linhas de montagem, túneis e peças móveis para construir as ferramentas moleculares que sustentam os ciclos globais do nitrogênio, a produção de alimentos e, potencialmente, futuras tecnologias verdes.
Citação: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Palavras-chave: nitrogenase, montagem de metaloclustres, andaime NifEN, criomicroscopia eletrônica, fixação biológica do nitrogênio