Clear Sky Science · pt
Decodificando o eixo imunorregulatório ERS–CAF via IA multimodal e seu valor prognóstico e preditivo terapêutico pan‑câncer
Observando tumores sem bisturi
Médicos oncológicos reconhecem cada vez mais que o que circunda um tumor pode importar tanto quanto o próprio tumor. Mas amostrar repetidamente esse bairro oculto com biópsias é invasivo e frequentemente impraticável. Este estudo mostra como a inteligência artificial (IA) pode ler exames de imagem de rotina e lâminas de microscopia para inferir processos imunes e semelhantes a cicatrizes, difíceis de medir dentro dos tumores, potencialmente transformando imagens diárias em uma espécie de "biópsia digital" que funciona em diferentes tipos de câncer.
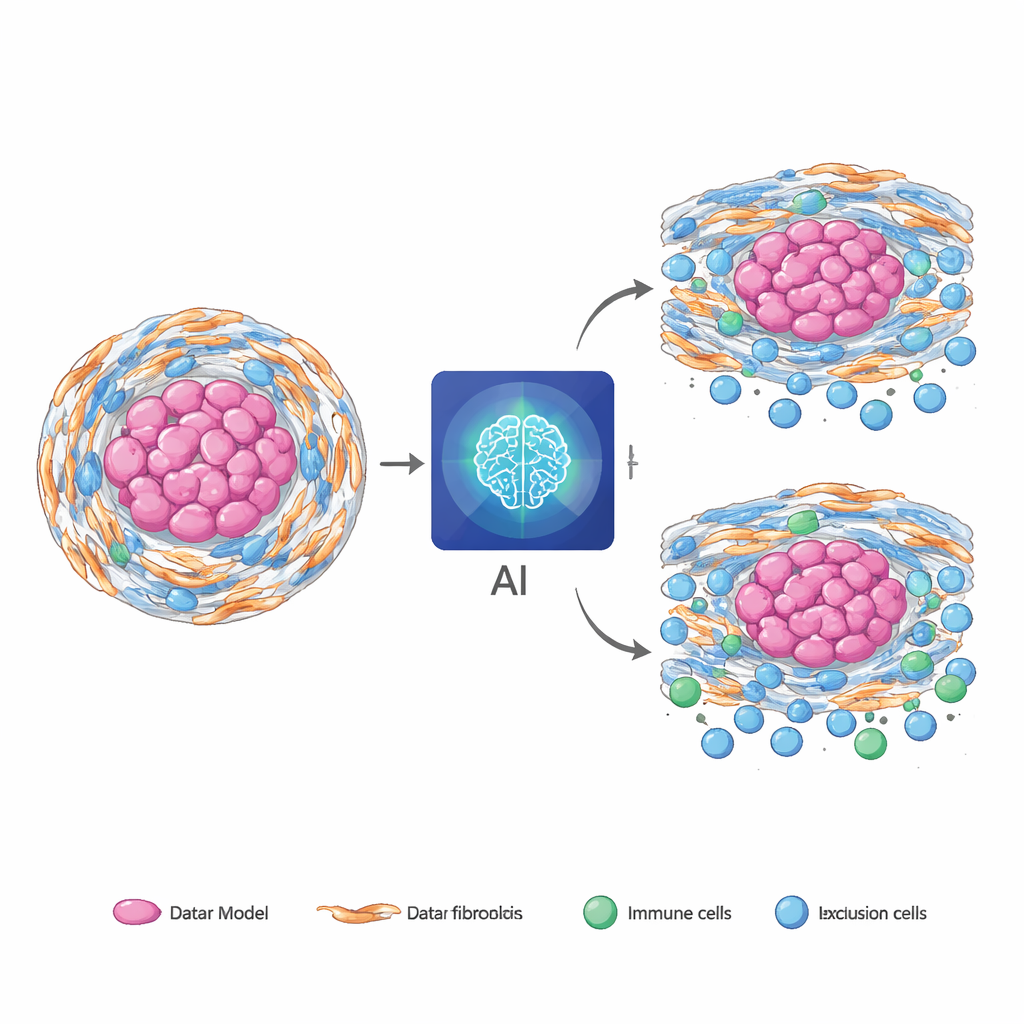
As células de suporte ocultas que moldam o câncer
Muitos tumores sólidos estão envoltos por uma concha resistente e fibrosa formada por células de suporte especializadas chamadas fibroblastos. Quando essas células estão sob estresse dentro da fábrica de proteínas da célula (o retículo endoplasmático), elas adotam um estado agressivo que ajuda o câncer. No cordoma, um câncer ósseo raro, esses fibroblastos estressados constroem uma matriz densa e ajudam a manter células imunes do lado de fora, tornando os tratamentos menos eficazes. Ambientes fibrosos e pobres em resposta imune semelhantes aparecem em outros cânceres, como pâncreas e colorretal, sugerindo que essa biologia não é exclusiva de uma doença. O desafio é que as maneiras atuais de medir esses fibroblastos estressados e seu comportamento de bloqueio imune dependem de amostras teciduais e testes moleculares complexos, que são difíceis de repetir e podem perder regiões importantes do tumor.
Ensinando a IA a ver biologia invisível
Os pesquisadores perguntaram se ressonâncias magnéticas padrão pré‑operatórias e lâminas de patologia H&E de rotina já continham pistas visuais sobre essa barreira imune mediada por fibroblastos estressados. Eles criaram três “escores de referência” numéricos a partir do sequenciamento de RNA tumoral: um capturando quão ativo está o programa de estresse nos fibroblastos, outro resumindo com que força essas células parecem sinalizar para células imunes, e outro descrevendo quão diversa é a população de células imunes e de suporte ao redor. Em vez de prever milhares de genes, a IA foi treinada para prever apenas esses três escores biologicamente significativos a partir das imagens. Para isso, a equipe combinou dois ramos: um que analisa textura e forma da RM e outro que varre milhares de pequenas regiões na lâmina digital e usa um mecanismo de atenção guiado por linguagem para focar em áreas que correspondem às descrições de especialistas de tecido fibrótico e pobre em imune.
Combinando exames e lâminas para sinais mais fortes
Em 126 pacientes com cordoma com RM, lâminas de patologia, dados de RNA e acompanhamento pareados, o modelo multimodal fundido superou modelos que usavam apenas RM ou apenas lâminas. Suas previsões dos três escores moleculares concordaram de perto com as medições baseadas em RNA e permaneceram bem calibradas entre diferentes hospitais e scanners. Quando patologistas marcaram independentemente regiões fibróticas e excluídas de imune, os “pontos quentes” da IA tendiam a acender nessas mesmas áreas, sugerindo que estava rastreando biologia genuína em vez de apenas tamanho do tumor. O modelo também captou prognóstico: escores previstos mais altos de fibroblastos em estresse e de sinalização associaram‑se a pior sobrevida, enquanto maior diversidade prevista do microambiente ofereceu proteção parcial. Adicionar esses escores derivados por IA aos fatores clínicos de rotina melhorou a capacidade de separar pacientes de alto e baixo risco ao longo do tempo.
De tumores raros a cânceres comuns
Um teste chave foi saber se um modelo treinado inteiramente em cordoma poderia ser usado “como está” em outros cânceres mais comuns. Aplicada sem retreinamento a tumores de pâncreas, estômago e colorretal de grandes conjuntos públicos, a versão apenas para lâminas do modelo ainda mostrou alinhamento significativo entre suas previsões baseadas em imagem e escores recém‑calculados a partir de RNA. Em alguns desses cânceres, os escores da IA melhoraram a previsão de sobrevida dos pacientes além das informações clínicas padrão e ajudaram a distinguir quais pacientes eram mais propensos a se beneficiar da quimioterapia. Para facilitar a implementação onde a patologia digital é limitada, a equipe destilou o modelo multimodal completo em uma versão somente RM que manteve a maior parte do poder preditivo enquanto rodava mais rápido e usava menos capacidade de processamento.
O que isso pode significar para pacientes
Em conjunto, os resultados sustentam a ideia de que imagens médicas de rotina codificam discretamente informações sobre células de suporte estressadas, exclusão imune e diversidade do microambiente — características que normalmente exigiriam testes moleculares caros. Embora o trabalho atual seja retrospectivo e precise de validação prospectiva, aponta para um futuro em que um exame padrão e uma lâmina podem sinalizar não invasivamente tumores com uma barreira imune fibrótica hostil, orientar quais pacientes podem se beneficiar de testes adicionais ou terapias personalizadas, e fazê‑lo através de múltiplos tipos de câncer sem ônus extra para os pacientes.
Citação: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Palavras-chave: microambiente tumoral, imagens de câncer, inteligência artificial, fibroblastos, imunoterapia