Clear Sky Science · pt
DARE-FUSE: aprendizado guiado por evidências alinhadas por domínio para segmentação e classificação conjuntas de tumores cerebrais em MRI
Por que exames cerebrais mais inteligentes importam
Os tumores cerebrais estão entre os diagnósticos mais temidos na medicina, e a ressonância magnética (MRI) é a principal ferramenta que os médicos usam para ver onde um tumor começa e termina. Ainda assim, mesmo radiologistas experientes podem ter dificuldade para delimitar com precisão um tumor e avaliar como ele muda ao longo do tempo, especialmente quando suas bordas se confundem com tecido cerebral inchado. Este artigo apresenta o DARE-FUSE, um novo sistema de inteligência artificial projetado para interpretar exames de MRI do cérebro com maior confiabilidade, traçando limites tumorais mais nítidos e oferecendo explicações mais claras de suas decisões para apoiar cirurgiões, oncologistas e pacientes.
Bordas difusas e clínicas sobrecarregadas
Em hospitais reais, os exames de MRI do cérebro são desafiadores. Tumores frequentemente se misturam ao edema circundante, implantes metálicos podem distorcer a imagem, e diferentes hospitais usam configurações de varredura ligeiramente distintas. Radiologistas precisam percorrer manualmente centenas de imagens, marcar o tumor fatia a fatia e então decidir como ele está se comportando. Esse trabalho é demorado, cansativo e sujeito a discordâncias entre especialistas. Ferramentas de IA existentes podem ajudar a contornar tumores ou rotular exames como “com tumor” ou “sem tumor”, mas a maioria dos sistemas trata essas tarefas separadamente, e muitos fracassam quando as imagens vêm de novos centros ou contêm crescimentos sutis e irregulares nas margens.
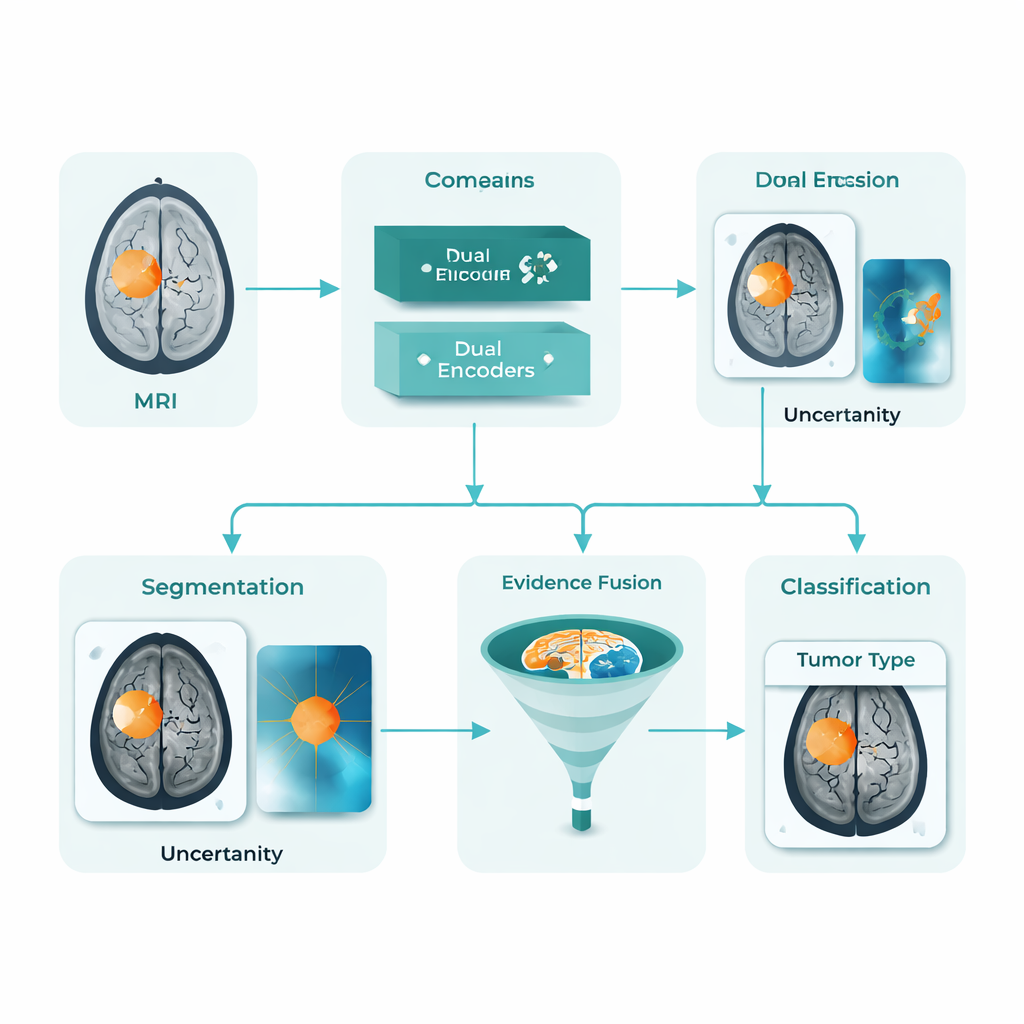
Um assistente de IA unificado para mapas e rótulos tumorais
O DARE-FUSE enfrenta vários desses obstáculos ao mesmo tempo. Ele é construído como um fluxo único que tanto traça o tumor em cada fatia de MRI (segmentação) quanto classifica imagens inteiras em grupos diagnósticos (classificação). No seu núcleo estão duas “visões” cooperantes: uma rede ajustada para formas detalhadas e limites, e outra voltada para padrões globais que distinguem diferentes tipos de tumor. Um módulo especial de alinhamento mantém essas visões sincronizadas entre hospitais e aparelhos, de modo que características aprendidas em um conjunto de dados não prejudiquem o desempenho em outro. O sistema também estima sua própria incerteza, sinalizando essencialmente áreas onde tem menos certeza sobre o contorno exato do tumor — algo vital para uso clínico seguro.
Usando pistas de mapas de calor e reconstruções “livres de tumor”
Em vez de confiar em um único sinal, o DARE-FUSE aprende a partir de vários tipos de evidência. Um ramo produz mapas de calor, mostrando quais partes do cérebro mais sustentam a decisão de classificação da IA. Outro ramo usa um modelo generativo para imaginar como o mesmo exame poderia parecer se o tumor fosse removido, e então compara essa versão “livre de tumor” com o original. As diferenças entre as duas destacam mudanças estruturais sutis e bordas que podem não sobressair fortemente em um mapa de calor padrão. Um módulo de fusão combina essas pistas em um mapa contínuo de “priori tumoral”: regiões onde várias fontes concordam são tratadas como tumor central, enquanto regiões de menor certeza são adicionadas com mais cautela e ponderadas para baixo quando a incerteza do modelo é alta. Esse priori combinado orienta o contorno final, ajudando a evitar tanto bolsões de tumor perdidos quanto ilhas espúrias em tecido saudável.
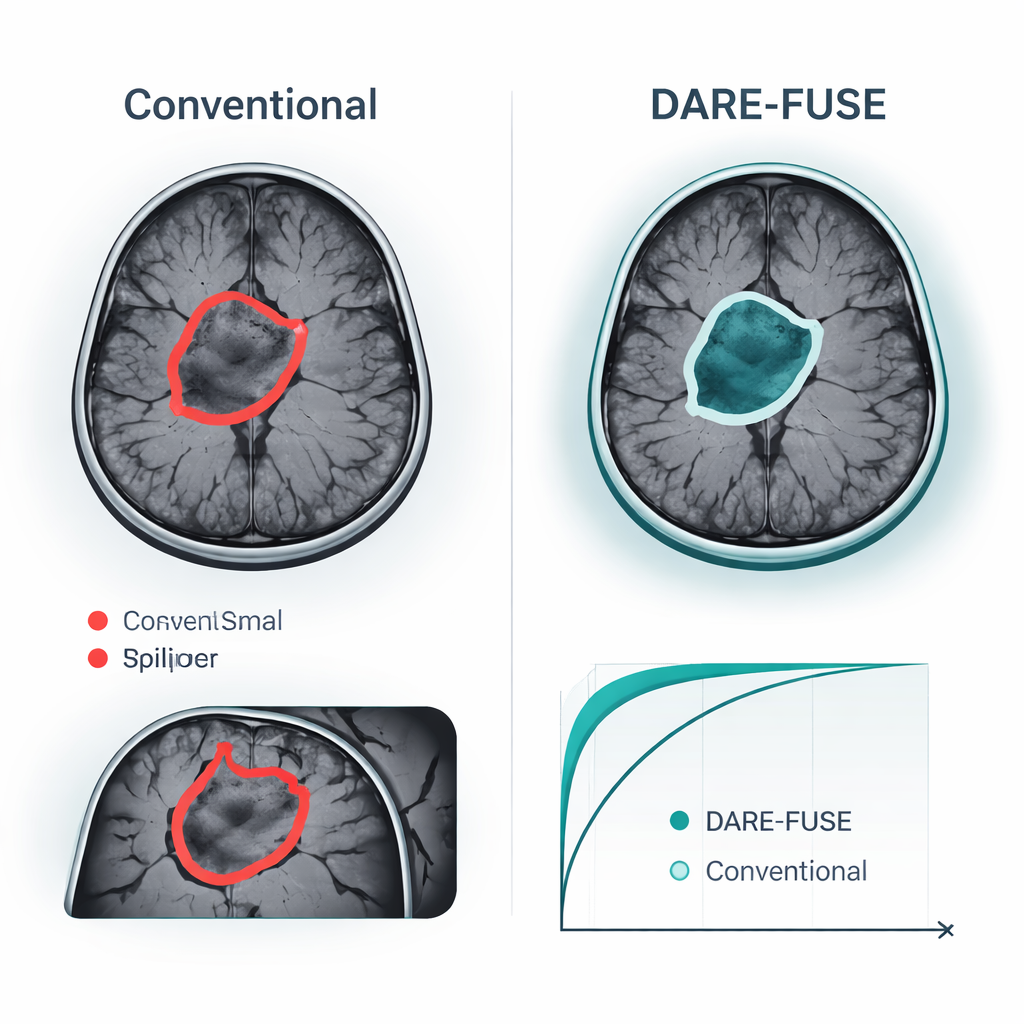
Ganhos comprovados em conjuntos públicos de tumores cerebrais
Os autores testaram o DARE-FUSE em seis grandes desafios multicêntricos de tumores cerebrais (a série BraTS) e em quatro coleções públicas de MRI usadas para classificação ao nível da imagem. Em todas as edições do BraTS, o sistema igualou ou superou os melhores modelos recentes de aprendizado profundo, alcançando sobreposição ligeiramente maior entre suas máscaras tumorais previstas e os desenhos de especialistas, e erros consistentemente menores na superfície tumoral medida. Esses ganhos foram mais marcantes em casos difíceis: tumores pequenos, bordas de baixo contraste e formas complexas e irregulares. Em tarefas de classificação — decidir, por exemplo, se um exame mostra um glioma, meningioma, tumor da hipófise ou nenhum tumor — o DARE-FUSE também superou baselines fortes baseados em transformers e métodos fracamente supervisionados em acurácia e em uma medida padrão de discriminação (AUC). Importante: quando os pesquisadores reduziram artificialmente o número de anotações detalhadas, o novo sistema degradou-se de forma mais graciosa e manteve vantagem sobre competidores semissupervisionados e fracamente supervisionados.
O que isso pode significar para pacientes
Para pacientes e clínicos, a principal promessa do DARE-FUSE não é um algoritmo chamativo, mas um suporte de imagem mais confiável e interpretável. Na prática, o sistema poderia propor um contorno tumoral, destacar regiões onde tem menos confiança e exibir mapas de calor explicando quais regiões da imagem fundamentam sua classificação. Médicos poderiam aceitar regiões de baixa incerteza como contorno inicial e então concentrar a atenção nas áreas sinalizadas em vez de redesenhar tudo do zero. Medidas mais precisas e consistentes de volume e forma tumoral poderiam melhorar o planejamento do tratamento, o direcionamento em radioterapia e o acompanhamento da resposta ao longo do tempo. Embora os autores enfatizem que sua ferramenta é um assistente — não um substituto — para o julgamento especializado, os resultados apontam para sistemas de IA que podem ver tumores com mais clareza e comunicar seu nível de confiança de maneiras que os clínicos possam agir.
Citação: Liu, Y., Sun, C., Niu, Y. et al. DARE-FUSE: domain aligned evidence guided learning for joint brain tumor MRI segmentation and classification. npj Digit. Med. 9, 178 (2026). https://doi.org/10.1038/s41746-026-02365-3
Palavras-chave: tumor cerebral em MRI, segmentação de imagens médicas, aprendizado profundo em radiologia, suporte à decisão clínica, IA consciente de incerteza