Clear Sky Science · pt
Autoencoders mascarados, pré-treinamento generalizável e especialistas integrados para segmentação aprimorada de gliomas
Por que exames mais inteligentes importam para tumores cerebrais
Os tumores cerebrais chamados gliomas estão entre os cânceres mais letais, mas os médicos ainda gastam muito tempo traçando manualmente as bordas do tumor em exames de ressonância magnética. Esse contorno cuidadoso orienta cirurgia e radioterapia, mas pode levar 15–20 minutos por paciente e precisa ser repetido ao longo do tempo. O estudo apresenta o MAGPIE, um sistema de inteligência artificial que aprende com dezenas de milhares de exames cerebrais sem rótulos humanos e, depois, precisa apenas de um punhado de casos rotulados por especialistas para mapear gliomas de forma confiável. Para os pacientes, isso pode significar um planejamento de tratamento mais rápido e consistente, mesmo em hospitais que não dispõem de grandes conjuntos de dados curados.
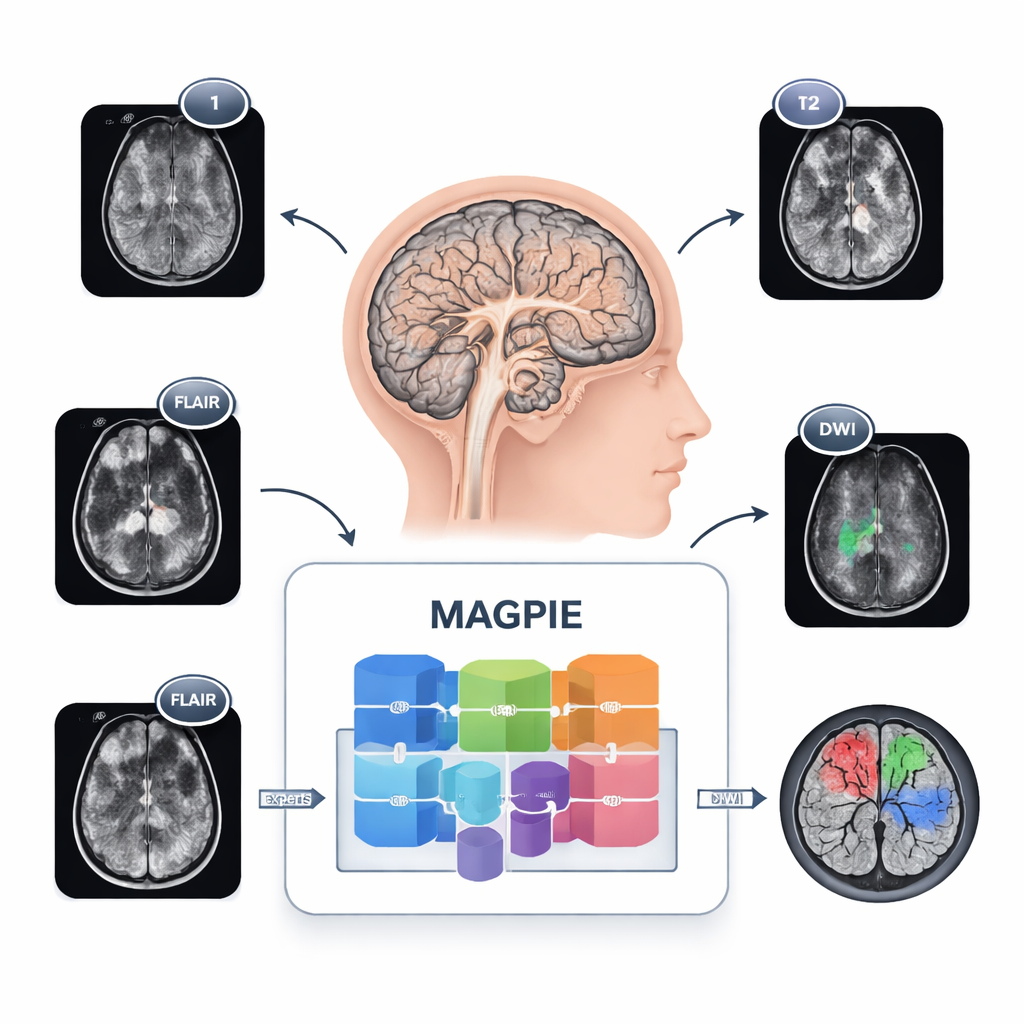
Ver tumores de uma nova maneira
Gliomas são difíceis de mapear porque não formam massas bem delimitadas. Células cancerosas se espalham ao longo das conexões cerebrais, criando margens difusas e pequenos focos satélites difíceis de detectar. Diferentes hospitais também usam configurações e combinações de sequências de RM distintas, de modo que uma ferramenta treinada em um local pode falhar em outro. O MAGPIE enfrenta tudo isso de uma vez. Primeiro, foi exposto a 43.505 exames de RM cerebrais não rotulados, provenientes de muitos estudos e tipos de aparelhos. Nessa fase, aprendeu padrões gerais de tecido cerebral saudável e doente tentando reconstruir partes faltantes das imagens e comparando diferentes versões aumentadas do mesmo cérebro, o que o força a focar em características estáveis e significativas em vez de detalhes frágeis de pixels.
Permitindo que múltiplos especialistas compartilhem o trabalho
Em vez de atuar como um modelo monolítico, o MAGPIE contém uma “mistura de especialistas” em seu interior. Ao analisar um novo exame, ele ativa apenas um pequeno subconjunto de oito sub-redes especializadas para cada região da imagem. Durante o treinamento, esses especialistas naturalmente dividem a tarefa: alguns se tornam sensíveis ao anel brilhante e ativo de crescimento do tumor; outros se concentram no núcleo necrosado; outros aprendem o anel esmaecido de edema ao redor do tumor; e alguns focam principalmente no fundo cerebral normal e nos limites anatômicos. Os autores demonstram isso medindo quão fortemente a atividade de cada especialista se sobrepõe às diferentes zonas tumorais delineadas por radiologistas. Essa divisão de trabalho melhora a precisão mantendo o custo computacional gerenciável — apenas cerca de metade dos parâmetros do modelo está ativa para cada fragmento dado.
Lidando com exames do mundo real, heterogêneos
Os protocolos clínicos de RM estão longe de ser uniformes. Alguns pacientes têm quatro sequências, outros menos; aparelhos de fabricantes diferentes produzem imagens sutilmente distintas. O projeto do MAGPIE trata cada sequência de RM como um “token” separado e aprende dinamicamente quanto peso dar a cada uma, em vez de esperar um conjunto fixo de entradas em uma ordem fixa. Essa abordagem agnóstica ao canal permite que o sistema se adapte se, por exemplo, uma sequência com contraste estiver ausente, mas a FLAIR estiver presente. O modelo também usa mecanismos avançados de atenção que lhe permitem tanto “ver de longe”, capturando espalhamento em longa distância ao longo de tratos de substância branca, quanto “ver com precisão”, detectando lesões muito pequenas de apenas alguns milímetros.
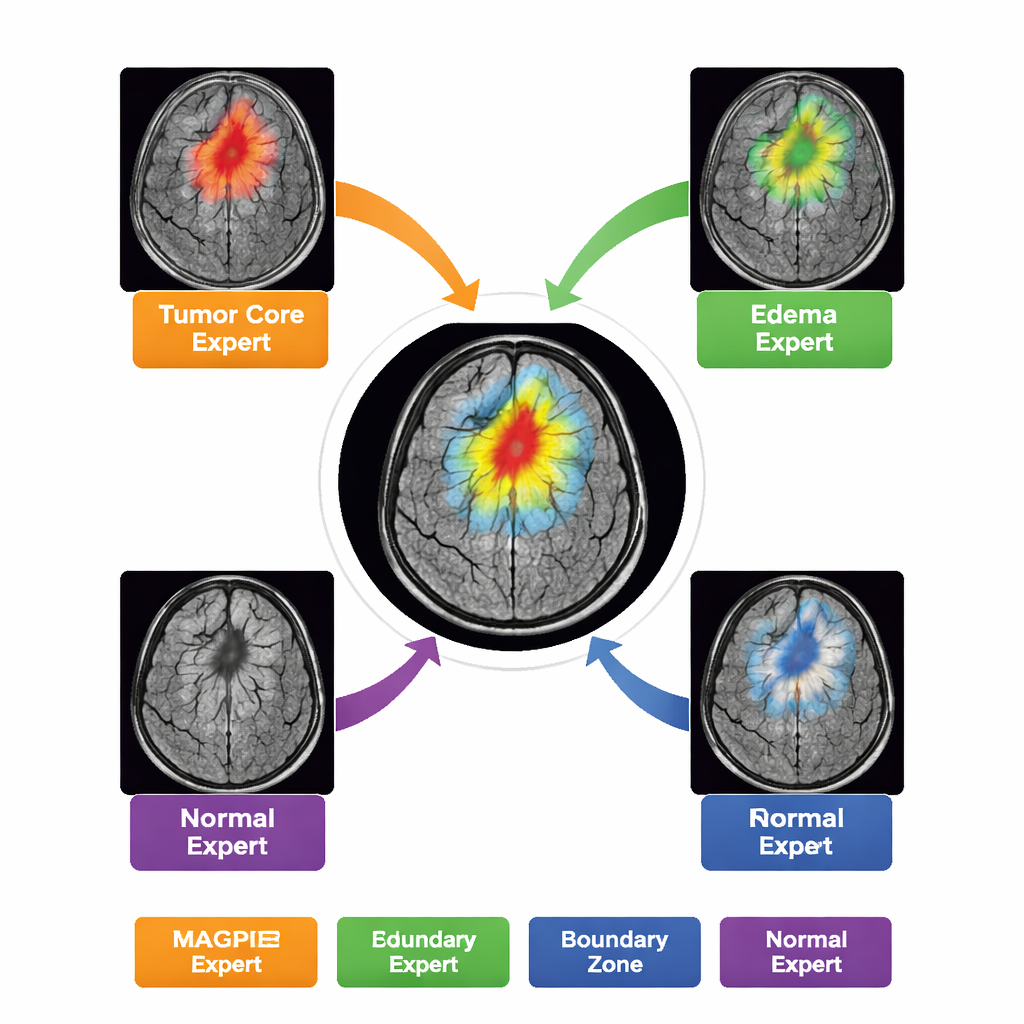
Fazer mais com muito menos rótulos
Após o pré-treinamento, os pesquisadores ajustaram finamente o MAGPIE com apenas 20 casos de glioma totalmente rotulados e o compararam a modelos padrão treinados do zero nas mesmas condições. Em um grande benchmark de tumores cerebrais (BraTS21), o MAGPIE alcançou uma pontuação Dice — uma medida comum de sobreposição em imagem médica — de cerca de 61%, superando a melhor versão treinada do zero por aproximadamente 2,6 pontos percentuais e superando um método auto-supervisionado anterior robusto sem apresentar qualquer “transferência negativa” prejudicial. Em dados desafiadores fora da distribuição — exames de doenças diferentes, tipos de aparelho e configurações de imagem distintas — também se manteve melhor, alcançando mais de 70% de Dice em um conjunto de lesões da substância branca sem ajuste adicional. Crucialmente, esse nível de desempenho normalmente exige da ordem de 400 casos rotulados; o MAGPIE o atinge com apenas cerca de 5% desse esforço.
O que isso pode significar para pacientes e clínicas
Para não especialistas, a mensagem central é que o MAGPIE transforma uma montanha de exames de RM não rotulados em um assistente potente que precisa de pouquíssimo treinamento especializado para se tornar clinicamente útil. Ele pode delinear tumores cerebrais complexos com fronteiras realistas, detectar pequenos focos satélites que outros sistemas perdem e continuar funcionando de forma confiável quando os exames vêm de máquinas desconhecidas ou carecem de certas sequências. Essa combinação pode reduzir o tempo de anotação dos radiologistas em cerca de 95%, diminuir a barreira para que hospitais menores implantem IA avançada em imagem e apoiar um planejamento mais preciso de cirurgia e radioterapia. Embora sejam necessárias validações adicionais em tipos raros de tumor e casos de baixo grau, o estudo mostra como um aprendizado auto-supervisionado bem projetado pode aproximar a segmentação robusta e eficiente de tumores cerebrais da prática clínica cotidiana.
Citação: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Palavras-chave: segmentação de glioma, RM cerebral, aprendizado auto-supervisionado, mistura de especialistas, IA em imagem médica