Clear Sky Science · pt
Fusão multimodal de modelos fundamentais de patologia e radiologia para subtipagem de glioma segundo a OMS 2021
Unindo Duas Visões dos Tumores Cerebrais
Quando uma pessoa recebe o diagnóstico de um tumor cerebral, os médicos precisam saber não apenas que há um tumor, mas qual é exatamente o tipo. Diferentes tipos de tumor respondem de formas muito distintas à cirurgia, radiação e medicamentos. Hoje, essa “subtipagem” detalhada costuma exigir testes genéticos que podem ser lentos, caros e nem sempre disponíveis. Este estudo investiga se um sistema computacional inteligente que analisa tanto imagens cerebrais quanto lâminas de tecido ao microscópio pode inferir esses subtipos de forma confiável, potencialmente acelerando e ampliando o acesso a tratamentos de precisão.
Por Que o Tipo de Tumor Importa
Os gliomas difusos em adultos estão entre os cânceres cerebrais mais letais, embora frequentemente apresentem aparência semelhante em exames convencionais e ao microscópio. Diretrizes modernas os classificam em três subtipos genéticos que diferem muito em agressividade e na sobrevida típica dos pacientes. O padrão-ouro atual para distinguir esses subtipos baseia-se em testes moleculares do DNA tumoral. Esses exames exigem tecido adicional, laboratórios especializados e dias a semanas para obter resultados. Os autores questionam se ressonâncias magnéticas (RM) rotineiras e lâminas de patologia digital poderiam ser combinadas para extrair informação suficiente para substituir parte dessa investigação genética.
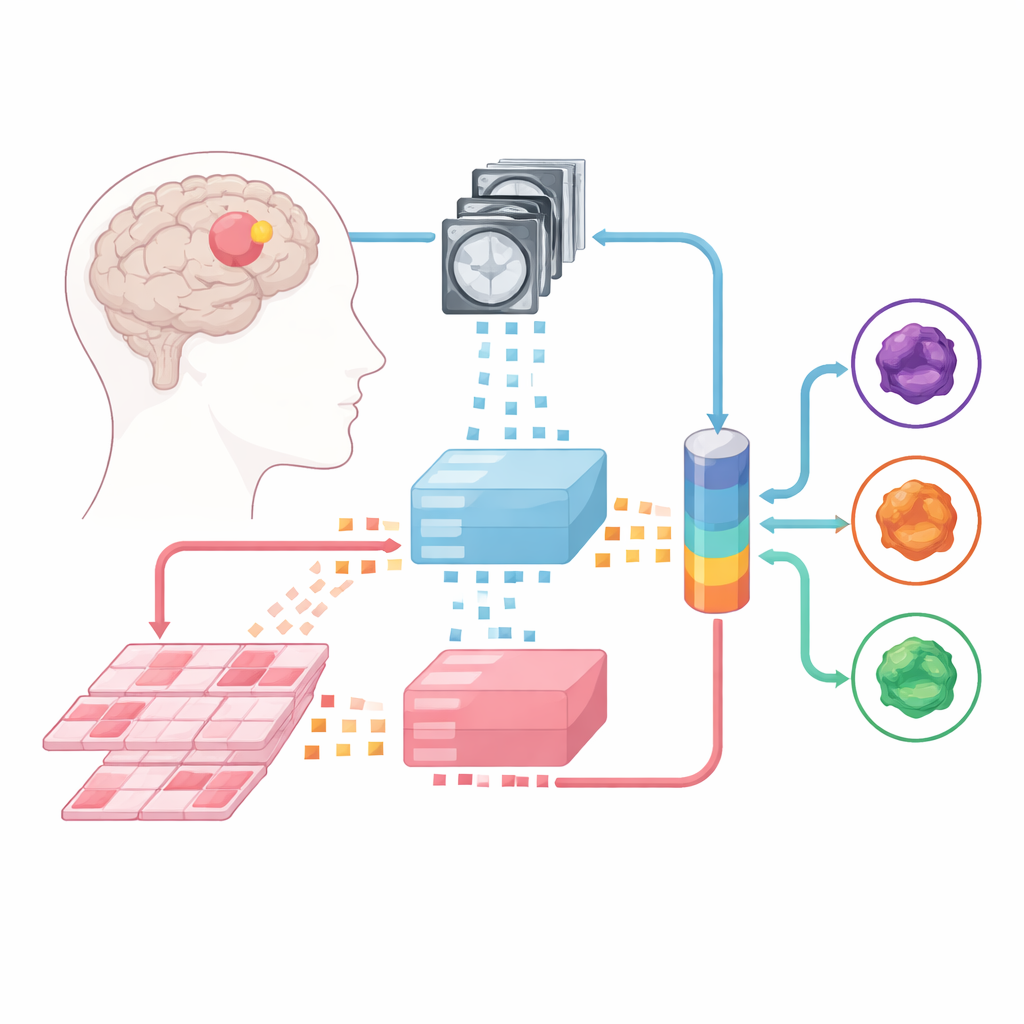
Ensinando Máquinas a Ler Exames e Lâminas
A equipe partiu de “modelos fundamentais” de grande porte — poderosos analisadores de imagens pré-treinados em enormes coleções de imagens médicas. Um desses modelos processa RMs multiparamétricas, e outro lida com lâminas de patologia em alta resolução feitas do tecido tumoral. Cada caso recebido é dividido em pequenos blocos de imagem, que os modelos fundamentais convertem em assinaturas numéricas. Sobre esses “especialistas” fixos, os pesquisadores treinaram três tipos de modelos de fusão que aprendem a combinar informação de RM e patologia: um desenho de fusão tardia (late-fusion), um de fusão precoce (early-fusion) e uma arquitetura mais flexível de mistura de especialistas (mixture-of-experts) que pode decidir dinamicamente quanto confiar em cada fonte.
Combinando Modalidades Sem Parear Pacientes
Um obstáculo prático para métodos multimodais é que hospitais raramente dispõem de grandes conjuntos no qual todo paciente tenha RM e imagens de patologia emparelhadas. Em vez de depender de dados perfeitamente pareados, os autores reuniram coleções separadas: centenas de casos de RM de vários centros e centenas de casos de patologia de outro recurso, além de um conjunto menor de 171 pacientes de um projeto público de câncer que tinham ambos. Durante o treinamento, frequentemente pareavam uma RM de um indivíduo com uma lâmina de patologia de outro, desde que os tumores pertencessem ao mesmo subtipo. Surpreendentemente, modelos treinados com esses dados “não pareados” funcionaram tão bem quanto os treinados com pares verdadeiros de pacientes, e claramente melhor do que simplesmente fazer a média de dois modelos de modalidade única.
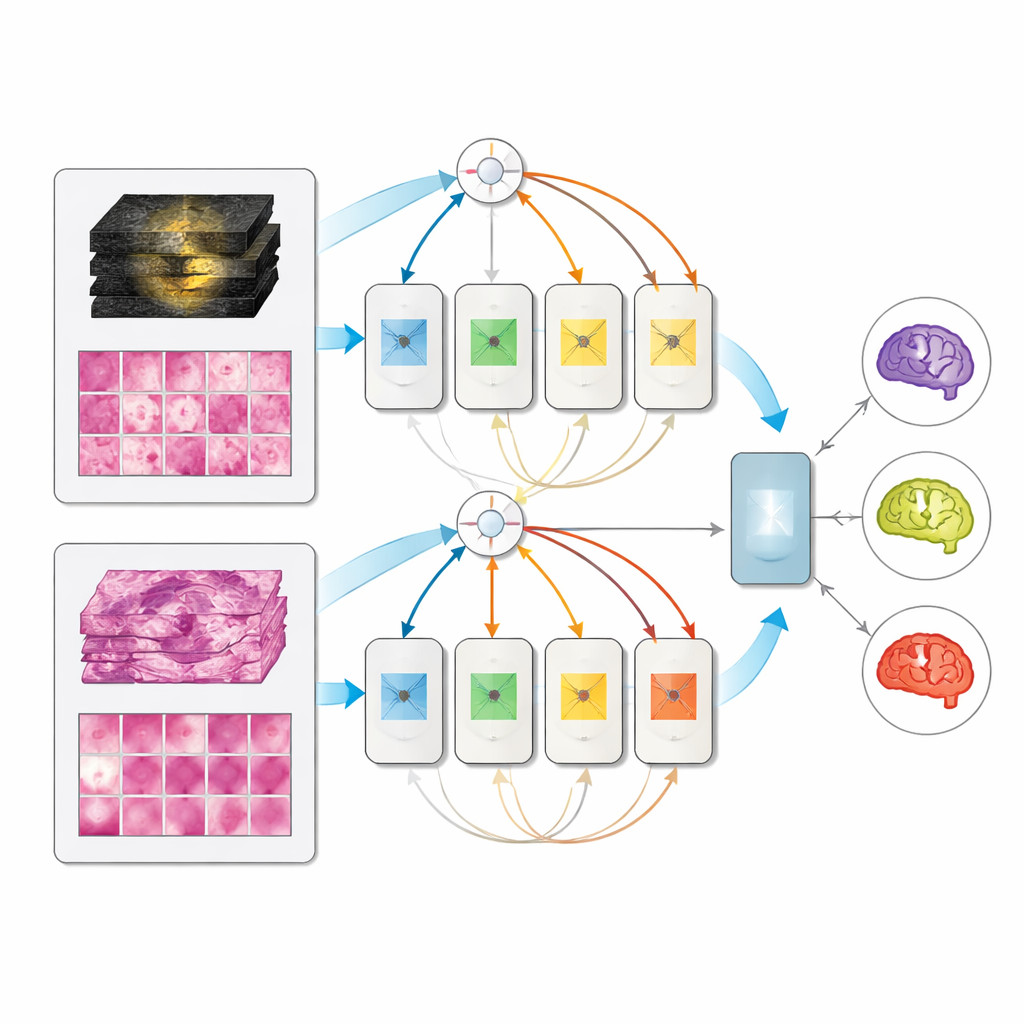
Um Único Modelo que se Adapta ao que Está Disponível
No conjunto retido de 171 pacientes totalmente caracterizados, todos os modelos multimodais superaram seus equivalentes de entrada única, e a arquitetura de mistura de especialistas foi a melhor, alcançando pontuações muito altas na distinção entre os três subtipos. Notavelmente, quando apenas RM ou apenas patologia foi fornecida no teste, o modelo multimodal não colapsou; seu desempenho foi aproximadamente equivalente ao de modelos dedicados a uma única modalidade. Isso significa que uma clínica poderia implantar um sistema unificado que use a informação disponível — apenas imagens pré-cirúrgicas, apenas tecido pós-cirúrgico, ou ambos — em vez de manter ferramentas separadas para cada cenário.
Vendo o que o Modelo Vê
Para aumentar a confiança nas decisões do sistema, os pesquisadores investigaram onde o modelo “olha” e quais características de imagem têm maior importância. Mapas de atenção mostraram que o modelo conjunto amplia seu foco por uma área maior do tumor e dos arredores, tanto na RM quanto nas lâminas de tecido, e que atenção mais difusa tende a coincidir com predições corretas. Uma análise mais profunda das características aprendidas revelou padrões que coincidem com indícios médicos conhecidos: por exemplo, características de RM que destacam núcleos tumorais com realce de contraste e espaços fluidos distorcidos ajudaram a separar tumores mais agressivos, enquanto características de tecido que capturam formas e texturas celulares clássicas auxiliaram no reconhecimento de subtipos específicos de glioma. Também surgiram lacunas interessantes: o modelo não codificou fortemente alguns sinais clássicos dos tumores mais agressivos, o que apoia a ideia de que ele frequentemente trata esse grupo como um “padrão” a menos que haja evidência forte de um subtipo mais favorável.
O que Isso Pode Significar para os Pacientes
Em termos práticos, este trabalho demonstra que um sistema de IA que combina exames cerebrais e imagens microscópicas pode classificar tumores cerebrais com mais precisão do que sistemas que analisam apenas um tipo de imagem, e que pode ser treinado mesmo quando os dois tipos de imagem não vêm dos mesmos pacientes. Se validado adicionalmente em coortes maiores e mais diversas, tais ferramentas poderiam ajudar médicos a estimar o subtipo tumoral mais cedo e de forma mais ampla, especialmente em contextos com acesso limitado a testes genéticos. Embora não substituam exames moleculares, podem servir como guias rápidos e de baixo custo para orientar cirurgiões e oncologistas em direção ao diagnóstico e ao caminho terapêutico mais prováveis.
Citação: Saueressig, C., Scholz, D., Raffler, P. et al. Multimodal fusion of pathology and radiology foundation models for WHO 2021 glioma subtyping. npj Precis. Onc. 10, 118 (2026). https://doi.org/10.1038/s41698-026-01366-5
Palavras-chave: subtipagem de glioma, imagens multimodais, inteligência artificial, RM e patologia, diagnóstico de câncer cerebral