Clear Sky Science · pt
Resposta ao midostaurin na LMA é determinada por um estado celular semelhante a progenitor, seletivamente atingido por miméticos de SMAC
Por que alguns medicamentos contra leucemia deixam de funcionar
Para muitas pessoas com um tipo de câncer sanguíneo chamado leucemia mieloide aguda (LMA), novos medicamentos direcionados trouxeram esperança — mas nem todos se beneficiam, e as respostas frequentemente desaparecem. Este estudo faz uma pergunta simples, porém crucial: por que algumas células leucêmicas ignoram um fármaco amplamente usado, o midostaurin, e podemos encontrar uma combinação inteligente que force essas células teimosas a morrer?
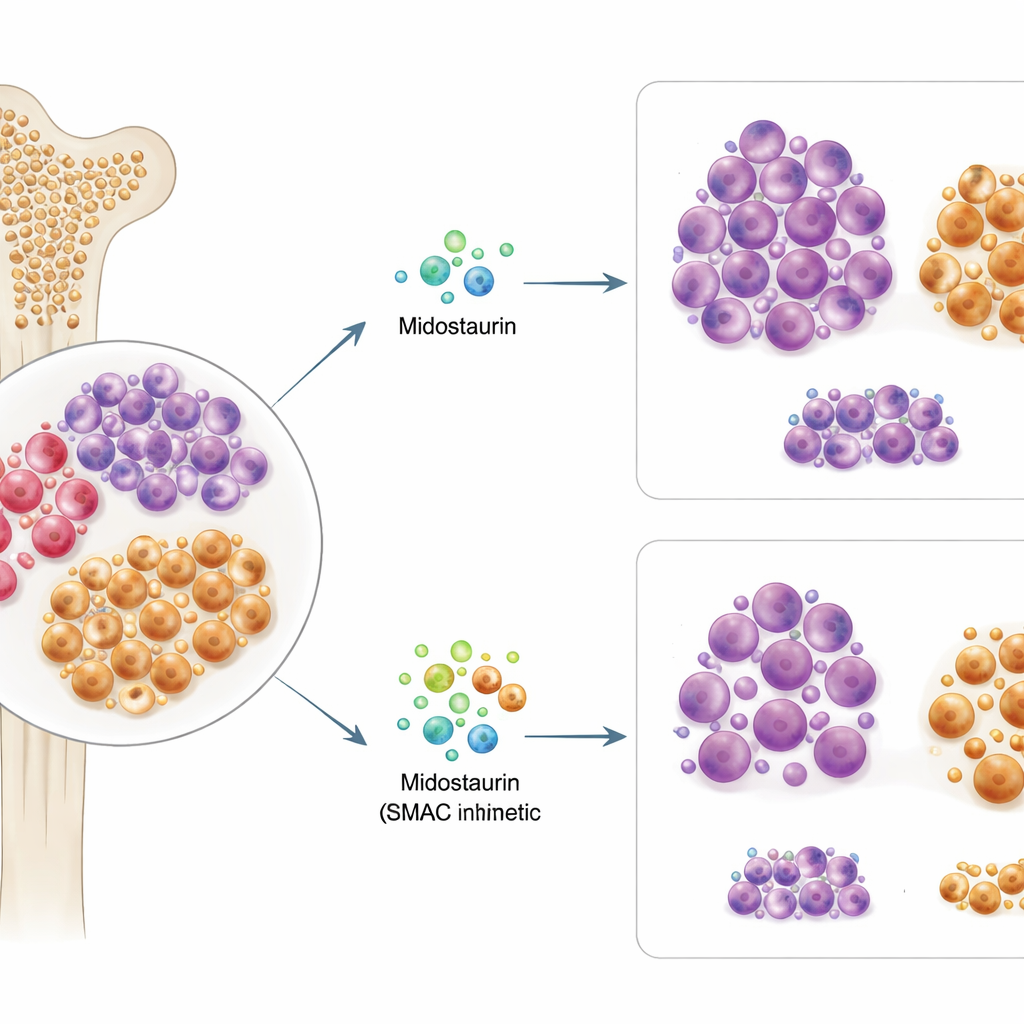
Olhando além da mutação principal
Cerca de um em cada três pacientes com LMA apresenta uma alteração no gene FLT3, que impulsiona o crescimento da leucemia e é a razão pela qual o midostaurin é prescrito. Os pesquisadores testaram amostras de medula óssea e sangue de 63 pacientes com LMA mutada em FLT3, expondo as células ao midostaurin e a mais de 500 outros fármacos contra o câncer em laboratório. Eles descobriram que a sensibilidade das células de um paciente ao midostaurin ex vivo correspondeu de perto à resposta subsequente desse paciente na clínica. Surpreendentemente, o tipo exato de mutação em FLT3 ou sua abundância não previram de forma confiável o sucesso do midostaurin, sugerindo que apenas a genética não explica quem se beneficia.
Um reservatório oculto de células “sementes” resistentes
Aprofundando, a equipe comparou os padrões gerais de proteínas e atividade gênica entre células sensíveis ao midostaurin e as que não eram. As amostras não respondedoras eram enriquecidas por características de células progenitoras imaturas, semelhantes a células‑tronco — células mais próximas da raiz da formação sanguínea e consideradas “sementes” capazes de reiniciar a leucemia. Em contraste, as amostras respondedoras se assemelhavam mais a células imunes e mieloides parcialmente maduras. Usando métodos avançados de célula única, os cientistas identificaram uma população específica de células leucêmicas marcada pelos marcadores de superfície CD38 e CD45RA que se comportava como essas sementes semelhantes a progenitores. Essas células apresentaram organização incomum de sua membrana externa, sugerindo que moléculas de sinalização importantes estavam dispostas de maneiras que favoreciam a sobrevivência.
Fiação de sobrevivência: uma mudança nas vias de sinalização
O midostaurin foi projetado para bloquear a sinalização de FLT3, que normalmente alimenta uma cadeia de sinais que inclui a molécula STAT5 e pode impulsionar o crescimento celular. Quando a equipe examinou a sinalização em linhagens celulares e amostras de pacientes após o tratamento com midostaurin, observaram dois padrões distintos. Nas células sensíveis ao midostaurin, a atividade de STAT5 caiu rapidamente, consistente com o desligamento eficaz do FLT3. Nas células resistentes, entretanto, outra via dominou: PI3K/AKT, uma rota clássica de sobrevivência que ajuda as células a resistir à morte. Essas células resistentes mantiveram ou até aumentaram a atividade de AKT após o tratamento, e apresentaram níveis mais altos de proteínas que bloqueiam a apoptose (morte celular programada). Em outras palavras, a fiação interna dessas células semelhantes a progenitor parecia redirecionada para favorecer a sobrevivência mesmo quando o FLT3 estava inibido.
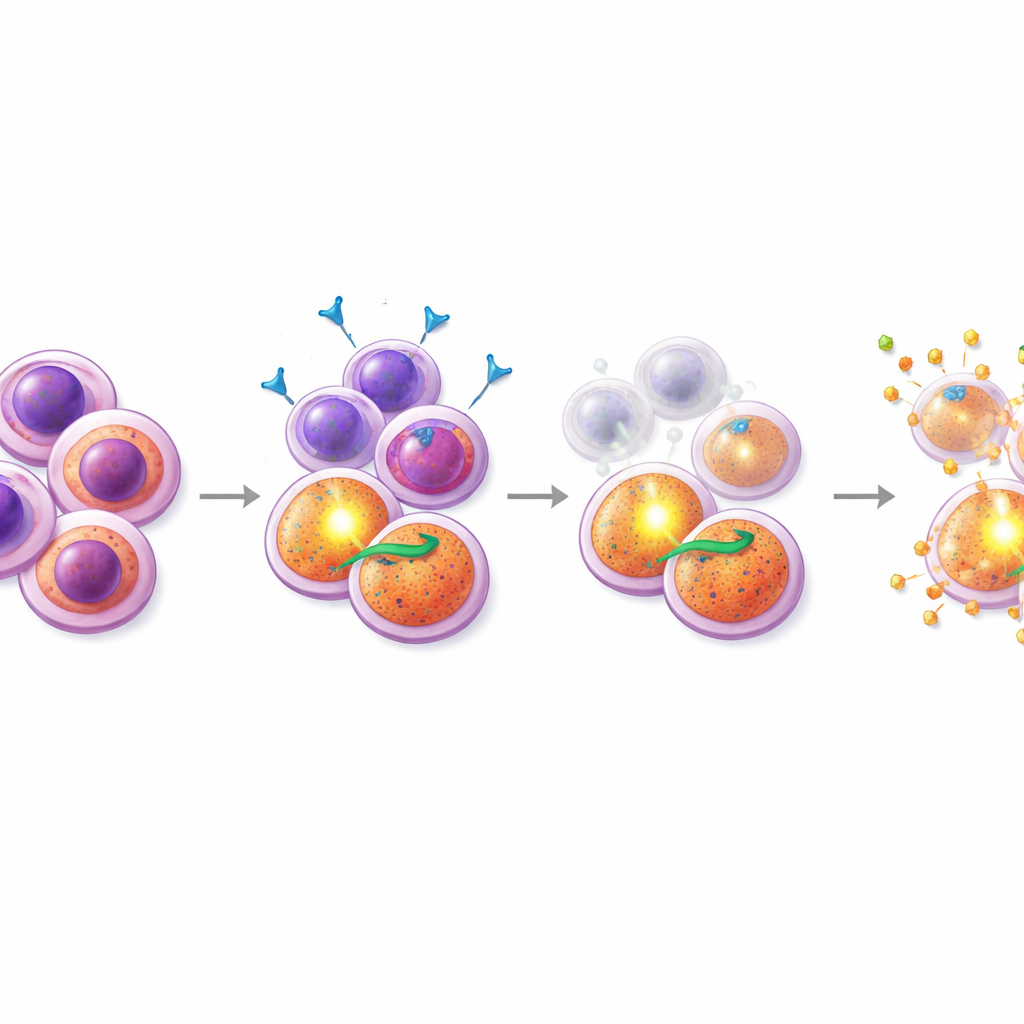
Encontrando um fármaco parceiro que atinja o ponto fraco
Munidos dessa percepção, os pesquisadores rastrearam combinações de midostaurin com centenas de outros compostos, concentrando‑se em drogas que influenciam a morte celular. Um grupo de destaque foi o dos miméticos de SMAC, fármacos que desativam as proteínas “inibidoras da apoptose” das quais as células impulsionadas por PI3K/AKT dependem. Em amostras de pacientes resistentes e em uma linhagem celular resistente mutada em FLT3, adicionar miméticos de SMAC como birinapant ao midostaurin produziu forte sinergia: juntos, os fármacos mataram muito mais células do que cada um isoladamente. Crucialmente, experimentos detalhados de citometria de fluxo mostraram que a combinação midostaurin–mimético de SMAC esgotou seletivamente a população semelhante a progenitor CD38+CD45RA+ e reduziu seus níveis característicos de marcadores de superfície, sugerindo que essa terapia atinge especificamente as sementes difíceis de eliminar. Em contraste, combinações com o inibidor aprovado de BCL‑2, venetoclax, foram mais eficazes contra um subconjunto diferente, com alto CD34, e não demonstraram o mesmo efeito focalizado nas células resistentes.
O que isso significa para os pacientes
Este trabalho sugere que a resistência ao midostaurin não se deve apenas à mutação em FLT3, mas também ao “estado” das células leucêmicas — seu nível de maturidade, organização da membrana e vias de sobrevivência preferidas. Um subconjunto semelhante a progenitor CD38+CD45RA+ parece ser um reservatório chave de resistência, deslocando sua sinalização da via habitual STAT5 para um programa de sobrevivência via PI3K/AKT. Ao combinar midostaurin com miméticos de SMAC, os pesquisadores conseguiram resensibilizar essas células e induzi‑las à morte em laboratório. Embora estudos clínicos maiores ainda sejam necessários, os achados apontam para um futuro em que os médicos podem usar testes funcionais e perfilamento do estado celular, não apenas sequenciamento de DNA, para escolher combinações direcionadas a FLT3 que atinjam tanto a população leucêmica em massa quanto suas sementes mais resilientes.
Citação: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Palavras-chave: leucemia mieloide aguda, inibidores de FLT3, resistência a medicamentos, células‑tronco leucêmicas, miméticos de SMAC