Clear Sky Science · pt
Fibroblastos associados ao câncer com alto COL3A1 orquestram microambientes metabólicos e imunes para conferir quimiorresistência no câncer de mama
Por que alguns tumores de mama resistem à quimioterapia
A quimioterapia pode salvar vidas no câncer de mama, porém muitos pacientes observam que seus tumores deixam de responder ou nunca respondem bem desde o início. Este estudo olha além das próprias células cancerosas para o bairro onde elas vivem e pergunta: quais células próximas ajudam os tumores a sobreviver ao tratamento, e como fazem isso? A resposta se concentra em um grupo especial de células de suporte que reprogramam tanto a nutrição do tumor quanto a imunidade local para proteger as células cancerosas da quimioterapia.
Os ajudantes ocultos ao redor do tumor
Os tumores de mama são mais do que apenas células cancerosas; são comunidades mistas que incluem vasos sanguíneos, células imunes e células do tecido conjuntivo chamadas fibroblastos. Quando fibroblastos vivem no tumor, são conhecidos como fibroblastos associados ao câncer, ou CAFs, e podem tanto restringir quanto promover o câncer. Ao combinar vários métodos poderosos de perfil genético em amostras de pacientes—análises de célula única, espaciais e em massa—além de experimentos em laboratório e animais, os pesquisadores identificaram um subgrupo de CAFs que produz altos níveis de uma molécula chamada COL3A1, um componente da matriz tecidual. Pacientes cujos tumores continham mais desses CAFs com alto COL3A1 tinham maior probabilidade de apresentar respostas ruins à quimioterapia e pior sobrevida.
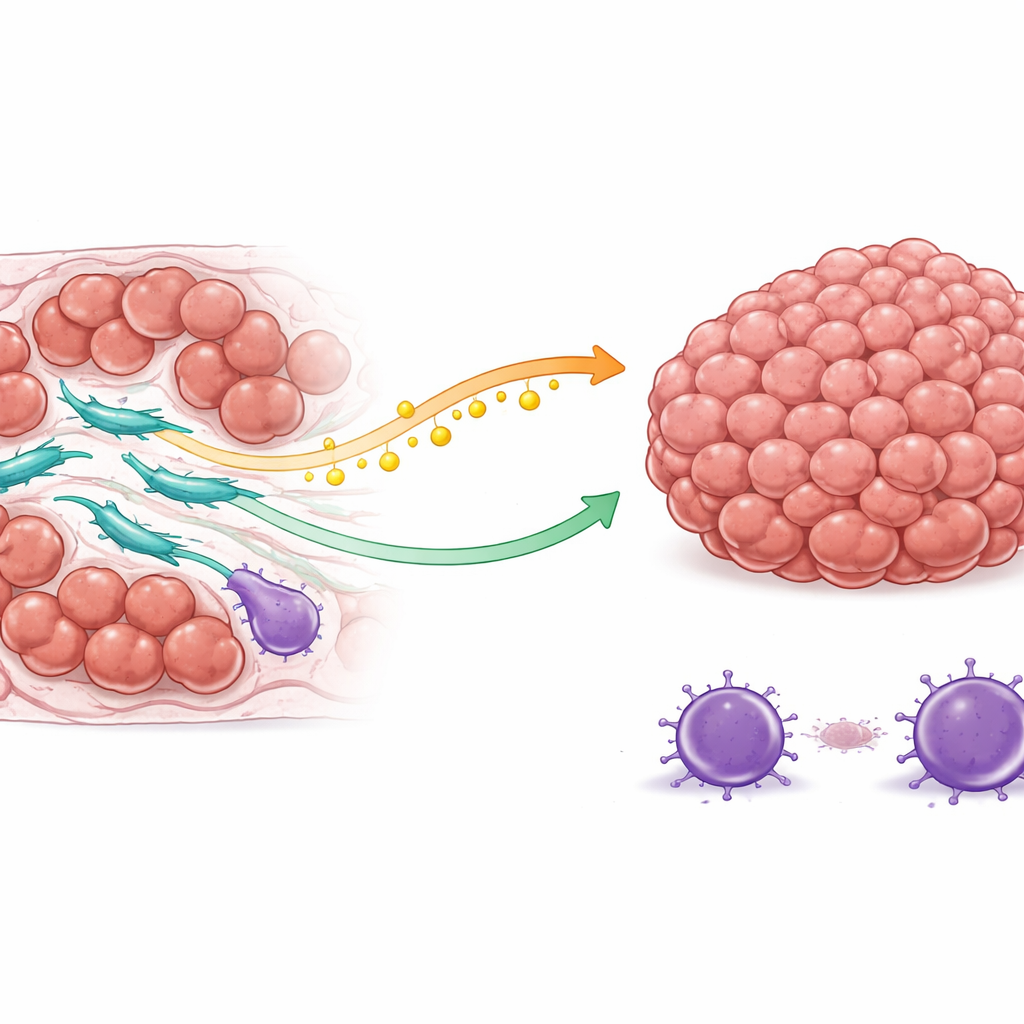
Um escudo duplo: combustível e proteção
A equipe descobriu que os CAFs com alto COL3A1 protegem as células cancerosas de duas maneiras principais. Primeiro, eles alteram como lidam com os lipídios. Esses fibroblastos aumentam a atividade de uma enzima que produz ácido oleico, um tipo de gordura. Em vez de reter esse combustível, eles o liberam no entorno do tumor. As células cancerosas captam esse ácido oleico por meio de uma proteína de superfície e, em resposta, ativam uma via interna de sobrevivência conhecida por ajudar as células a resistir a sinais de morte. Como resultado, quando a quimioterapia tenta desencadear programas de autodestruição nas células cancerosas, essas células estão mais bem equipadas para resistir e continuar se dividindo.
Moldando um entorno imune menos favorável
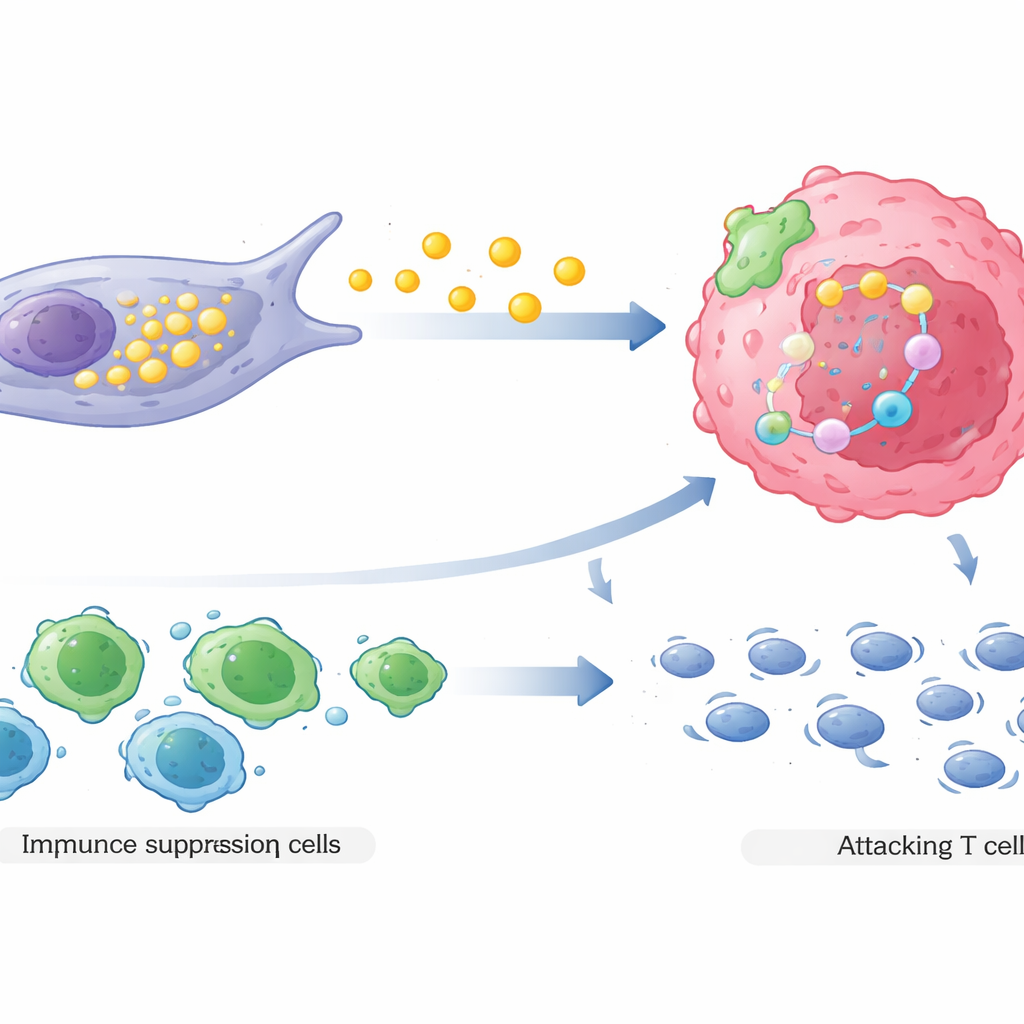
Segundo, os CAFs com alto COL3A1 remodelam a paisagem imune local a favor do tumor. Por meio de interações complexas de sinalização, eles atraem células T reguladoras, um tipo de célula imune que atenua ataques imunes, e ao mesmo tempo desencorajam ou enfraquecem as células T citotóxicas que normalmente atacariam o câncer. Mapeamentos espaciais de tumores reais de pacientes mostraram que esses fibroblastos tendem a ficar próximos tanto de células cancerosas resistentes a drogas quanto de células imunes supressoras, enquanto as células T citotóxicas eficazes são empurradas para mais longe. Esse arranjo cria uma zona protegida onde as células cancerosas enfrentam menos ameaças imunes justamente quando também se tornam mais difíceis de eliminar com medicamentos.
Prova a partir de células, camundongos e pacientes
Para testar causa e efeito, os pesquisadores reduziram COL3A1 em CAFs cultivados no laboratório. Quando células de câncer de mama foram cultivadas ao lado desses fibroblastos alterados, formaram menos estruturas invasivas, foram mais facilmente mortas pelo fármaco quimioterápico paclitaxel e mostraram mais sinais de morte celular programada. Em camundongos implantados com misturas de células de câncer de mama e CAFs, bloquear COL3A1 nos fibroblastos retardou o crescimento tumoral durante a quimioterapia e reduziu os níveis da enzima de produção de gordura e do receptor na célula cancerosa ligado ao ácido oleico. Em um grupo de 72 pacientes tratados com quimioterapia antes da cirurgia, níveis mais altos de COL3A1 e de seus parceiros no metabolismo lipídico corresponderam fortemente a piores respostas ao tratamento e menor tempo até a recidiva do câncer.
O que isso significa para tratamentos futuros
Em termos simples, o estudo mostra que um conjunto particular de células de suporte nos tumores de mama age como uma unidade de guarda-costas: alimentam as células cancerosas com uma dieta protetora à base de gordura e recrutam aliados imunes que atenuam as defesas do organismo. Juntas, essas ações tornam a quimioterapia menos eficaz. Medir a abundância de fibroblastos com alto COL3A1 melhora a capacidade dos médicos de prever quem responderá ou não ao tratamento, e as vias que eles usam—produção de gordura, sinalização de sobrevivência dentro das células cancerosas e supressão imune—oferecem novos alvos para medicamentos. No futuro, terapias que desarmem ou reprogramem esses fibroblastos poderiam ser combinadas com a quimioterapia padrão para impedir que os tumores desenvolvam resistência.
Citação: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
Palavras-chave: câncer de mama, quimiorresistência, microambiente tumoral, fibroblastos associados ao câncer, metabolismo lipídico