Clear Sky Science · pt
Integrando biópsia líquida e assinaturas mutacionais para avançar a oncologia de precisão
Por que um exame de sangue para a “impressão digital” do câncer importa
O câncer costuma ser descrito como uma doença do DNA, mas o tumor de cada pessoa é geneticamente diferente e pode mudar ao longo do tempo. Isso dificulta a escolha do tratamento correto e a detecção de quando um câncer está recorrendo ou se tornando resistente a medicamentos. Este artigo explica uma abordagem promissora que combina um exame de sangue simples, chamado biópsia líquida, com padrões detalhados de dano ao DNA conhecidos como assinaturas mutacionais. Juntos, eles poderiam permitir que médicos acompanhassem como um tumor se comporta ao longo da doença do paciente e ajustassem as terapias com mais precisão do que nunca. 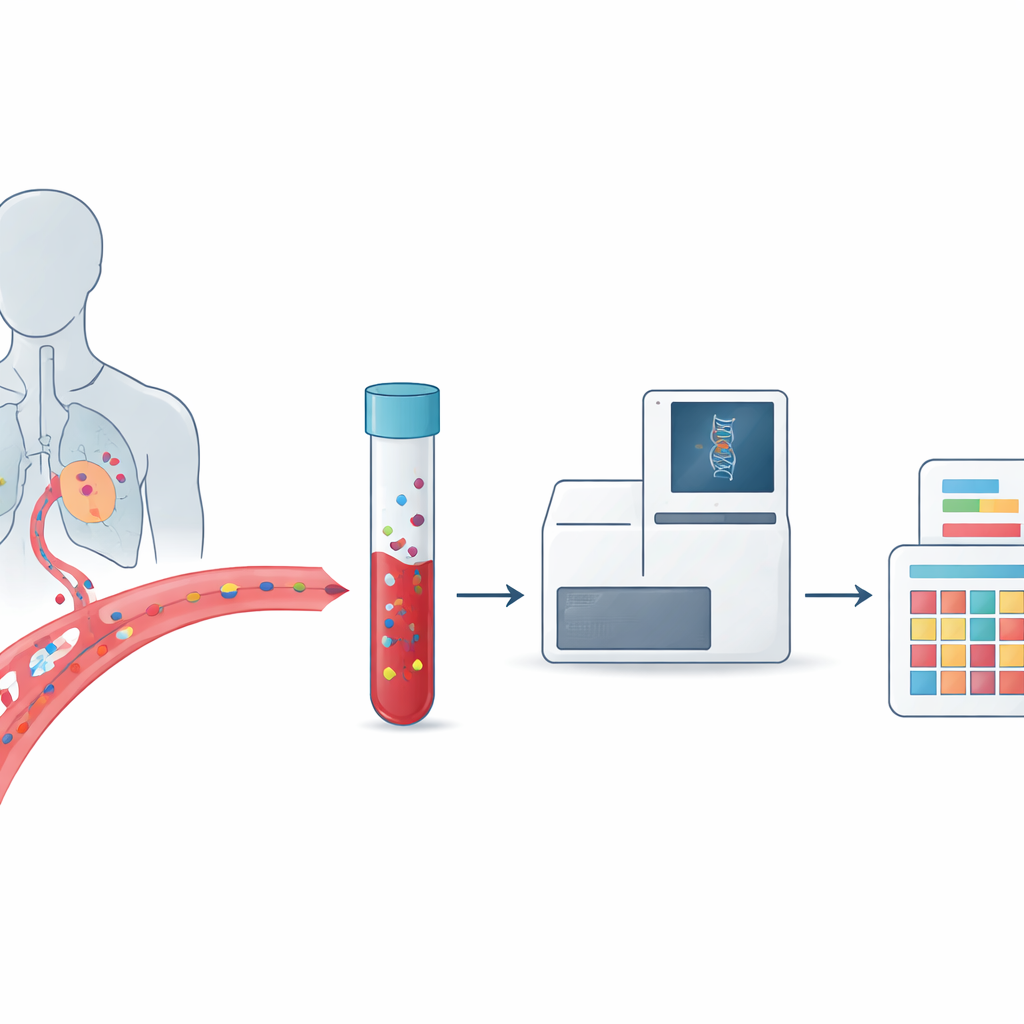
Procurando pistas de câncer em um tubo de sangue
Biopsias tradicionais de câncer exigem a remoção de um pedaço do tecido tumoral por cirurgia ou agulha, o que pode ser doloroso, arriscado e difícil de repetir. A biópsia líquida segue outro caminho: busca vestígios de câncer que os tumores liberam na corrente sanguínea e em outros fluidos corporais. Esses vestígios incluem células tumorais inteiras e fragmentos curtos de DNA liberados quando células cancerosas morrem. Como amostras de sangue podem ser colhidas regularmente e capturar material de múltiplos sítios tumorais, a biópsia líquida oferece uma imagem em movimento de como um câncer cresce, se espalha e responde ao tratamento, em vez de uma única fotografia no tempo.
Das mutações individuais aos padrões gerais de dano
A maioria dos testes atuais de biópsia líquida foca em detectar mutações específicas em uma lista curta de genes que orientam o uso de medicamentos direcionados. No entanto, nem todos os tumores carregam alterações “alvo” desse tipo, e cânceres com muitas mutações diferentes podem facilmente escapar de painéis genéticos fixos. Na última década, ferramentas poderosas de sequenciamento de DNA revelaram que as mutações no genoma de um câncer não são aleatórias: elas formam padrões reconhecíveis moldados por fatores como fumaça do tabaco, luz ultravioleta, reparo de DNA defeituoso ou a própria quimioterapia. Esses padrões recorrentes, chamados assinaturas mutacionais, atuam como impressões digitais dos processos que danificaram o DNA ao longo da vida do tumor.
Lendo a história e as fragilidades do tumor
Assinaturas mutacionais podem revelar onde um câncer pode ter começado e quais sistemas internos de reparo estão quebrados. Por exemplo, cânceres de pulmão em fumantes frequentemente mostram um padrão ligado à exposição ao tabaco, enquanto alguns cânceres de cólon apresentam assinaturas de falha no mismatch repair, um defeito que também os torna altamente sensíveis a certas imunoterapias. Outras assinaturas apontam para problemas em uma via de reparo do DNA chamada recombinação homóloga, que pode tornar tumores especialmente vulneráveis a medicamentos à base de platina e inibidores de PARP. Estudos experimentais em células e modelos animais confirmaram que muitos químicos ambientais e tratamentos contra o câncer deixam pegadas mutacionais distintas que correspondem às observadas em pacientes, fortalecendo a ligação entre assinatura e causa. 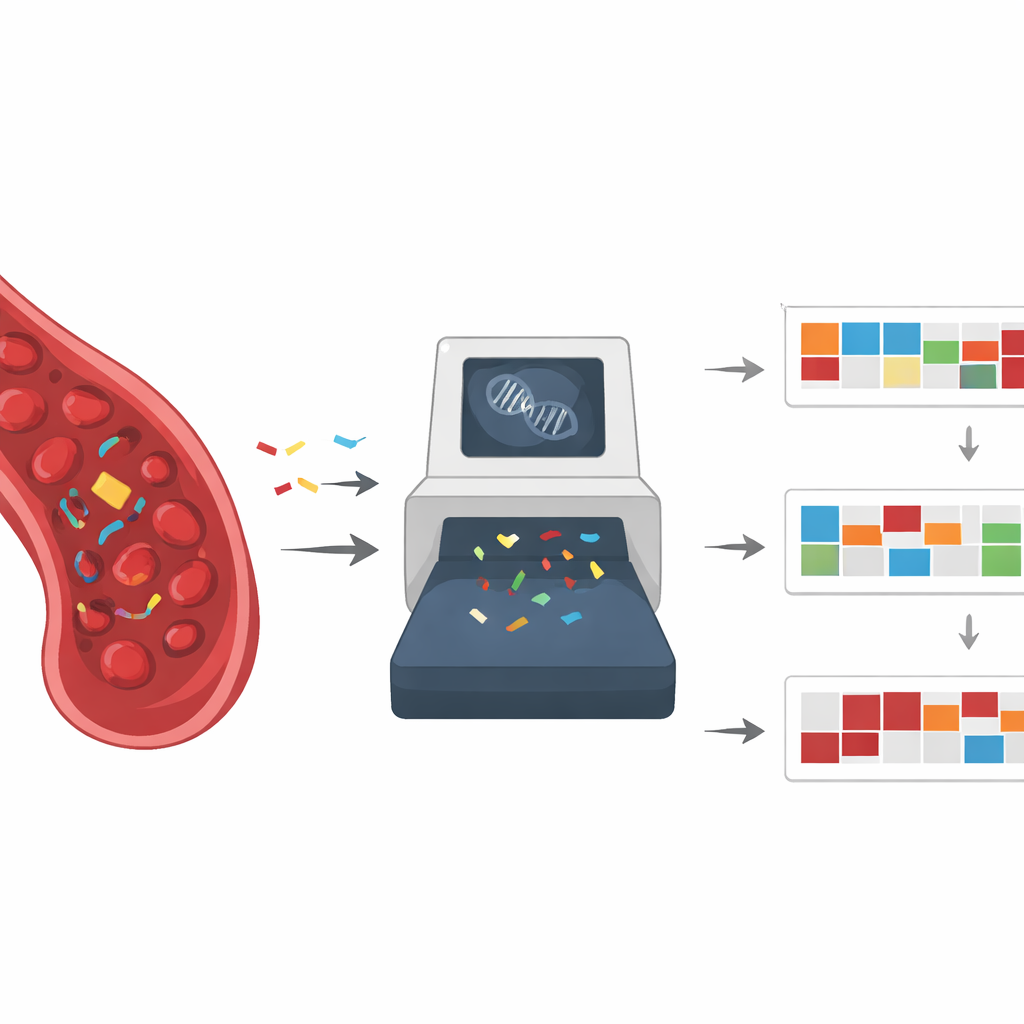
Combinando monitoramento por sangue com impressões digitais do DNA
A ideia central do artigo é fundir biópsia líquida com assinaturas mutacionais em um único quadro conceitual. Ao usar sequenciamento amplo em escala genômica dos fragmentos de DNA tumoral no sangue, os médicos poderiam identificar simultaneamente mutações individuais e os padrões gerais de dano que as produziram. Isso poderia melhorar a detecção precoce do câncer, ajudar a localizar o tecido de origem em casos enigmáticos e refinar escolhas terapêuticas mesmo quando as mutações clássicas dirigidas estão ausentes. Coletas de sangue repetidas ao longo de meses ou anos poderiam mostrar quando um tumor muda para um novo processo mutacional, como um induzido pela exposição contínua a um fármaco, sinalizando resistência emergente ou o risco de um segundo câncer relacionado à terapia.
Obstáculos no caminho para o uso cotidiano
Apesar de seu potencial, essa abordagem enfrenta desafios práticos. Alguns tumores liberam muito pouco DNA na corrente sanguínea, tornando seus sinais difíceis de detectar. Muitas assinaturas conhecidas ainda carecem de uma explicação biológica clara, e alguns padrões podem ser parcialmente moldados por peculiaridades técnicas de diferentes plataformas de sequenciamento. Alterações relacionadas à idade nas células formadoras de sangue podem introduzir suas próprias mutações no DNA sanguíneo, confundindo ainda mais o quadro. Métodos atuais para extrair assinaturas do plasma muitas vezes dependem de ferramentas complexas de aprendizado de máquina que requerem grandes conjuntos de treinamento e têm sido testadas principalmente em estudos de pesquisa retrospectivos, em vez de ensaios clínicos prospectivos.
O que isso pode significar para o cuidado futuro do câncer
Os autores concluem que integrar biópsia líquida com assinaturas mutacionais poderia, eventualmente, transformar o cuidado do câncer de uma série de decisões pontuais em um processo continuamente atualizado. Em vez de depender apenas de uma biópsia tecidual realizada no diagnóstico, os clínicos poderiam um dia usar exames de sangue de rotina para acompanhar a “caligrafia” evolutiva do dano ao DNA no tumor de um paciente. Isso poderia aguçar o rastreamento, melhorar o diagnóstico, orientar a seleção e a sequência de terapias e detectar resistência antes que ela se torne visível em exames de imagem. Realizar essa visão exigirá métodos padronizados, validação rigorosa e modelos computacionais mais inteligentes, mas o conceito aponta para um futuro em que o tratamento do câncer não é apenas dirigido às mutações atuais do tumor, mas também informado pelas forças que as criaram.
Citação: Carrasco, R., Dreij, K. Integrating liquid biopsy and mutational signatures to advance precision oncology. npj Precis. Onc. 10, 114 (2026). https://doi.org/10.1038/s41698-026-01337-w
Palavras-chave: biópsia líquida, assinaturas mutacionais, DNA livre de células, oncologia de precisão, evolução do câncer