Clear Sky Science · pt
Predizendo deficiência de recombinação homóloga e respostas ao tratamento usando um modelo fundacional baseado em tomografia computadorizada: um estudo pré-clínico
Por que isso importa para pacientes e médicos
Tratamentos contra o câncer que danificam o DNA, como certas quimioterapias e novas drogas direcionadas, podem ser notavelmente eficazes em tumores cujos sistemas de reparo já estão comprometidos. O desafio é descobrir quais tumores têm essas fraquezas ocultas sem depender de biópsias invasivas repetidas. Este estudo investiga se exames de imagem de rotina em camundongos, analisados por um poderoso modelo de inteligência artificial, podem revelar quão vulnerável é um tumor e quão bem ele responderá a uma nova droga experimental.
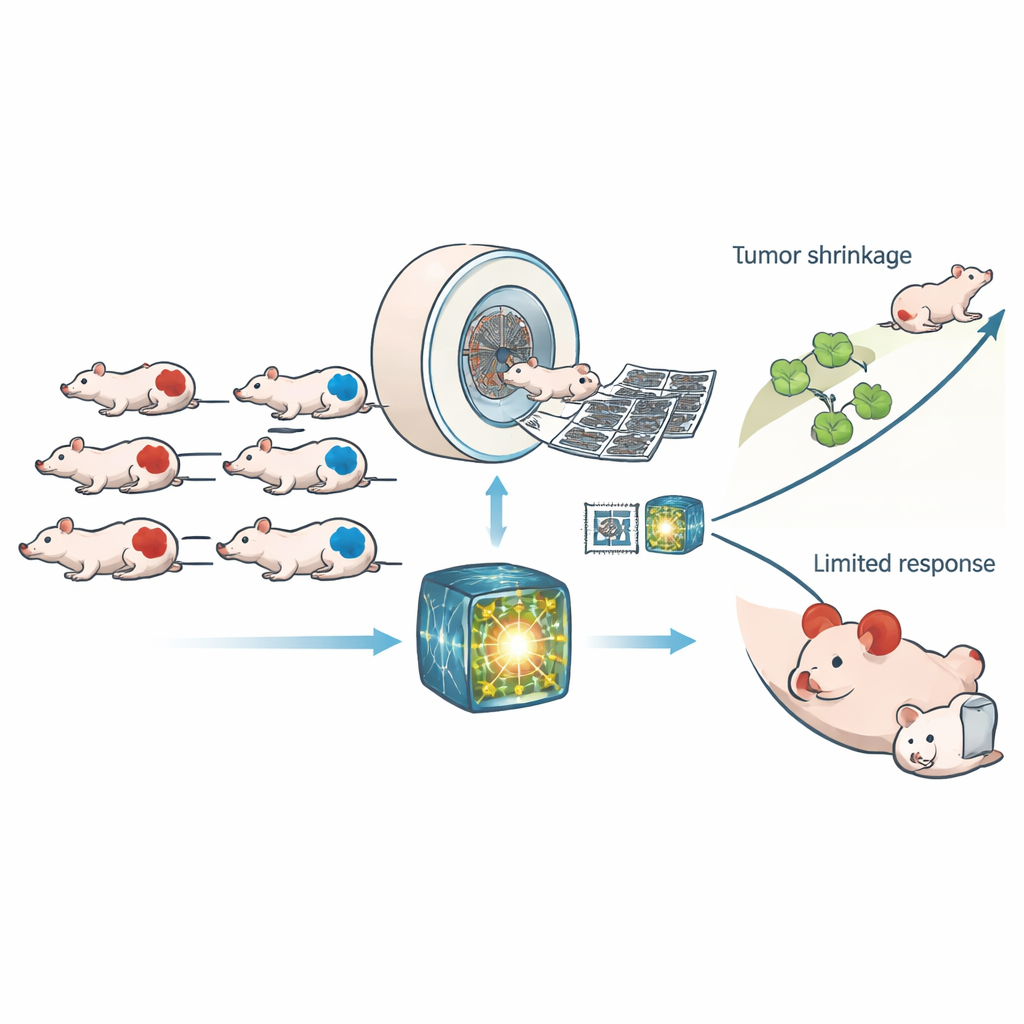
Um ponto fraco oculto nas células cancerosas
Muitos tumores apresentam defeitos em uma via chave de reparo do DNA chamada recombinação homóloga. Quando essa via falha, as células acumulam danos em seu material genético, uma condição conhecida como deficiência de recombinação homóloga, ou HRD. A HRD pode aumentar a probabilidade de surgimento de certos cânceres, mas também se transforma em um calcanhar de Aquiles: drogas que danificam ainda mais o DNA podem levar essas células já estressadas além do limite, matando-as de forma mais eficaz do que as células saudáveis. Hoje, identificar HRD costuma depender de testes genéticos ou ensaios laboratoriais especializados que são caros, demorados e frequentemente exigem amostras do tumor. Os autores perguntaram se a imagem — o mesmo tipo de tomografia tridimensional amplamente usada em clínicas — poderia oferecer uma janela rápida e não invasiva para detectar HRD.
Usando exames inteligentes em vez de mais biópsias
Os pesquisadores trabalharam com 307 camundongos portando enxertos tumorais humanos que eram ou HRD ou normais quanto à capacidade de reparo. Todos os animais foram submetidos a tomografias computadorizadas (TC) de alta resolução antes e depois de receberem um tratamento controle ou CP‑506, uma droga experimental que se torna ativa em regiões hipóxicas do tumor e entrecruza as fitas de DNA. Em vez de depender de um punhado de medidas de imagem feitas manualmente, a equipe usou um “modelo fundacional” moderno treinado em grandes conjuntos de dados humanos de TC para extrair milhares de padrões sutis de cada exame. Um classificador simples foi então treinado sobre esses padrões para decidir se um tumor era HRD, e as mesmas características aprendidas foram reutilizadas para prever quanto dano ao DNA e atraso de crescimento o CP‑506 causaria.
Desempenho do modelo de imagem
O modelo fundacional claramente superou tanto a radiômica tradicional quanto uma rede profunda padrão treinada do zero. Em exames de teste novos, ele distinguiu tumores HRD de não‑HRD com uma área sob a curva de aproximadamente 0,88, um nível de precisão que se manteve em diferentes configurações de energia da TC. Quando ambas as abordagens de IA concordaram sobre o tipo de tumor, o desempenho aumentou ainda mais. A pontuação de HRD baseada em imagem do modelo alinhou‑se de perto com o estado genético real em várias linhagens tumorais de próstata e colorretal, embora uma linhagem com comportamento de reparo incomum tenha permanecido mais difícil de classificar. Importante, as características de TC associadas à HRD não foram apenas artefatos estatísticos: elas também previram quanto dano persistente ao DNA o CP‑506 produziu 48 horas após o tratamento e quanto tempo levou para os tumores crescerem até quatro vezes seu tamanho em um experimento paralelo.
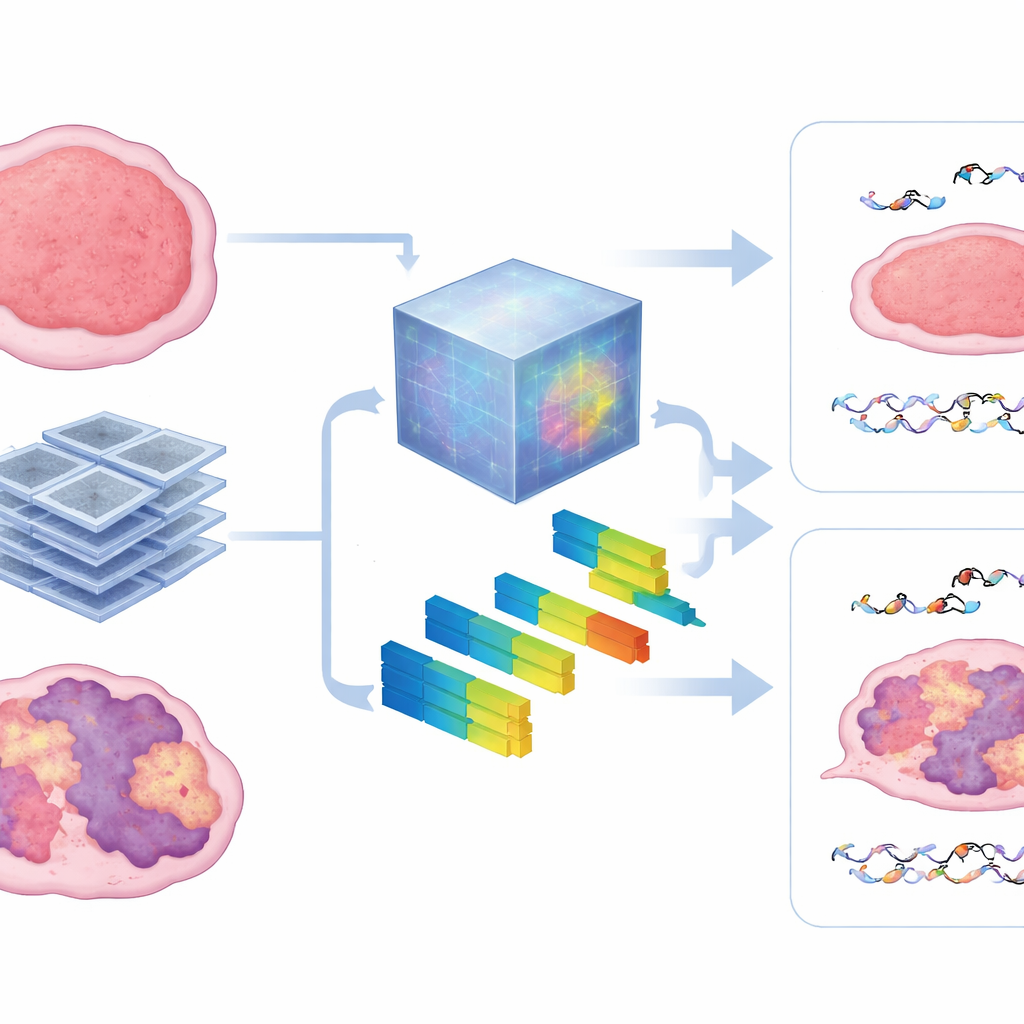
O que os exames revelam dentro do tumor
Para espiar dentro da caixa‑preta, os autores compararam os padrões aprendidos pelo modelo fundacional com características radiômicas padrão que descrevem textura e intensidade da imagem. Eles descobriram que o modelo se apoiou fortemente em medidas de heterogeneidade — quão irregular, áspero ou fragmentado o tumor parecia na TC. Tumores com assinaturas de HRD mais fortes tenderam a mostrar texturas mais desorganizadas, e essas mesmas características ajudaram a prever tanto o dano microscópico ao DNA quanto o controle macroscópico do tumor. A abordagem manteve‑se robusta quando havia menos dados de treinamento disponíveis, sugerindo que tais modelos pré‑treinados podem superar um grande obstáculo em estudos com animais, onde coletar grandes conjuntos de imagens é difícil.
Dos experimentos em camundongos ao futuro cuidado de pacientes
Este trabalho pré‑clínico mostra que uma única TC, interpretada por uma IA poderosa e pré‑treinada, pode captar sinais de reparo defeituoso do DNA e antecipar quão fortemente um tumor responderá a uma droga que danifica o DNA. Para um leigo, a conclusão é que exames com aparência padrão em breve podem ter dupla função — localizar o tumor e revelar quão frágil ele é — sem procedimentos extras. Antes que isso faça parte da prática clínica rotineira, o método precisa ser testado e validado em pacientes humanos. Se esses esforços tiverem sucesso, impressões digitais de HRD baseadas em TC podem ajudar médicos a combinar pessoas com tratamentos como CP‑506 e terapias relacionadas de forma mais precisa, melhorando os resultados e poupando outros de drogas tóxicas e ineficazes.
Citação: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Palavras-chave: deficiência de recombinação homóloga, imagemologia do câncer, radiômica, modelos fundacionais, terapia que danifica o DNA