Clear Sky Science · pt
Análise em larga escala de célula única e perturbação in silico revelam a evolução dinâmica do CHC: da iniciação ao direcionamento terapêutico
Por que a vida interior do câncer de fígado importa
O carcinoma hepatocelular, a forma mais comum de câncer de fígado, é notoriamente difícil de tratar. Muitos pacientes não respondem bem às drogas atuais, e os tumores frequentemente reaparecem ou se espalham. Uma razão importante é que cada tumor é uma mistura caótica de células diferentes que evoluem ao longo do tempo e se comunicam constantemente com seu entorno. Este estudo usa poderosas tecnologias de leitura gênica em célula única e espaciais para observar essa evolução em andamento, célula a célula, desde o crescimento tumoral inicial até a doença avançada e resistente a tratamentos, e para identificar pontos fracos que novas terapias possam explorar.
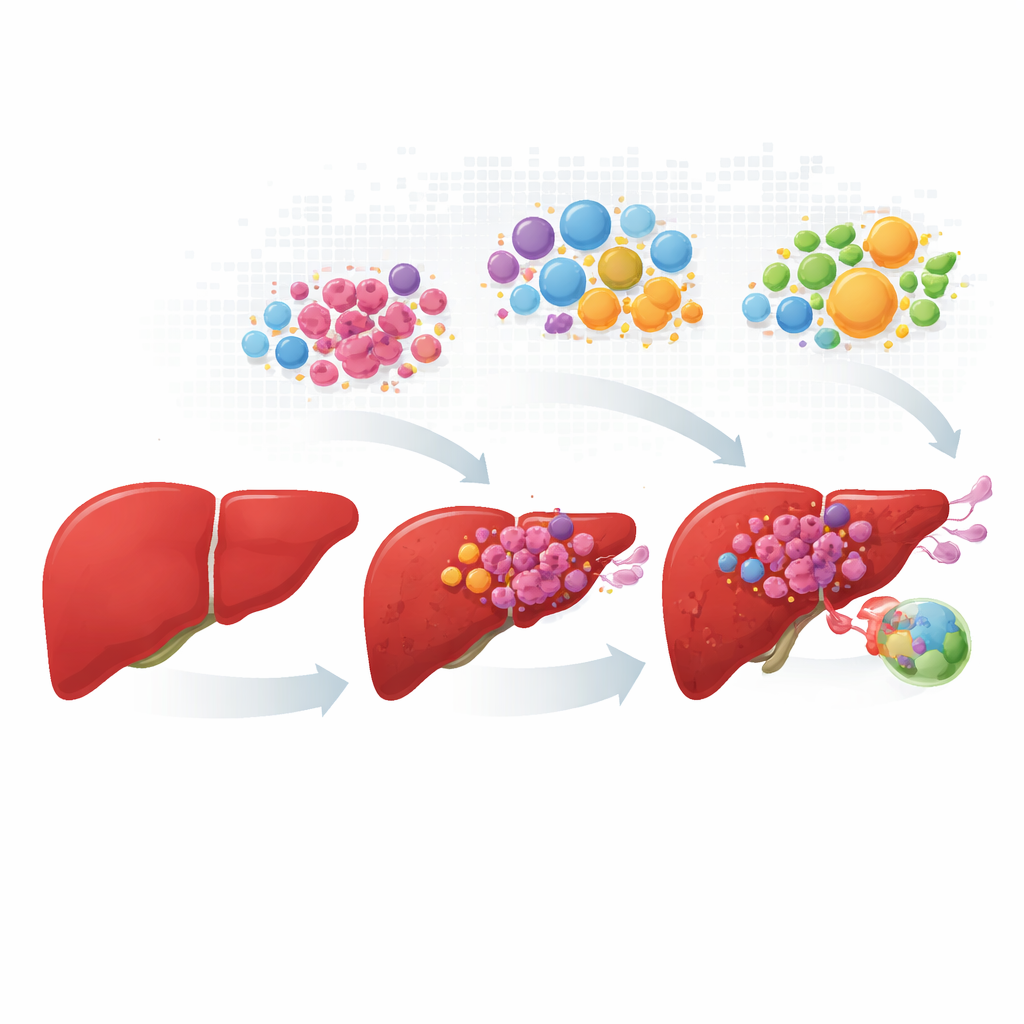
Seguindo as células cancerosas desde a alteração inicial até a disseminação
Os pesquisadores reuniram e harmonizaram dados de mais de cem pacientes, cobrindo fígado normal, tumores primários, crescimentos em vasos sanguíneos e metástases em linfonodos. Em vez de tratar cada tumor como uma massa uniforme, eles perfilaram centenas de milhares de células individuais e depois mapearam onde essas células se localizam em lâminas de tecido reais. As células hepáticas cancerosas se dividiram em quatro “personalidades” recorrentes. Um grupo manteve muitas funções normais do fígado e tarefas metabólicas; os outros três exibiram crescimento induzido por estresse, alta atividade da via de crescimento MYC ou comportamento invasivo associado à inflamação. Esses quatro estados apareceram em proporções diferentes conforme a doença avançou, com células de crescimento rápido e invasivas dominando em lesões vasculares e em linfonodos.
Quatro personalidades tumorais com futuros distintos
Os quatro estados das células cancerosas não eram apenas categorias acadêmicas; eles se correlacionaram com o desfecho dos pacientes. Tumores ricos no estado semelhante ao fígado, metabolicamente ativo, associaram‑se a melhores taxas de sobrevida, enquanto tumores dominados pelos outros três estados agressivos tendiam a ter piores prognósticos. Ainda assim, mesmo o estado “favorável” teve uma nuance: estava fortemente enriquecido em pacientes que não se beneficiaram do fármaco para câncer de fígado sorafenibe, provavelmente porque essas células preservam maquinário de desintoxicação capaz de inativar medicamentos. Ao reproduzir como as células se movem ao longo de trajetórias de desenvolvimento, a equipe mostrou que células invasivas e inflamatórias podem ramificar‑se em direção a estados mais diferenciados ou mais altamente proliferativos, sugerindo que as células tumorais podem mudar de identidade e potencialmente escapar de terapias dirigidas a um único estado.
O elenco de apoio: cúmplices imunes e estromais
As células cancerosas não atuam sozinhas. O estudo revelou células imunes especializadas e células de suporte que ou combatem os tumores ou os ajudam discretamente. Entre os macrófagos, os coletores de resíduos e sentinelas do tecido, alguns tipos produziram sinais inflamatórios que podem auxiliar a imunidade antitumoral, enquanto outros foram metabolicamente reprogramados, suprimiram sinais benéficos e promoveram o crescimento vascular e a invasão. Esses macrófagos “agentes nocivos” se expandiram em amostras avançadas. Do mesmo modo, certos endotélios que revestem os vasos sanguíneos e fibroblastos que constroem o tecido conectivo formaram subconjuntos distintos vinculados a mau prognóstico. Na doença avançada, um subtipo endotelial particular e dois tipos de fibroblastos criaram hubs fortemente conectados que remodelaram o arcabouço extracelular, alimentaram a formação de novos vasos sanguíneos e se correlacionaram com os estados celulares cancerosos mais agressivos.
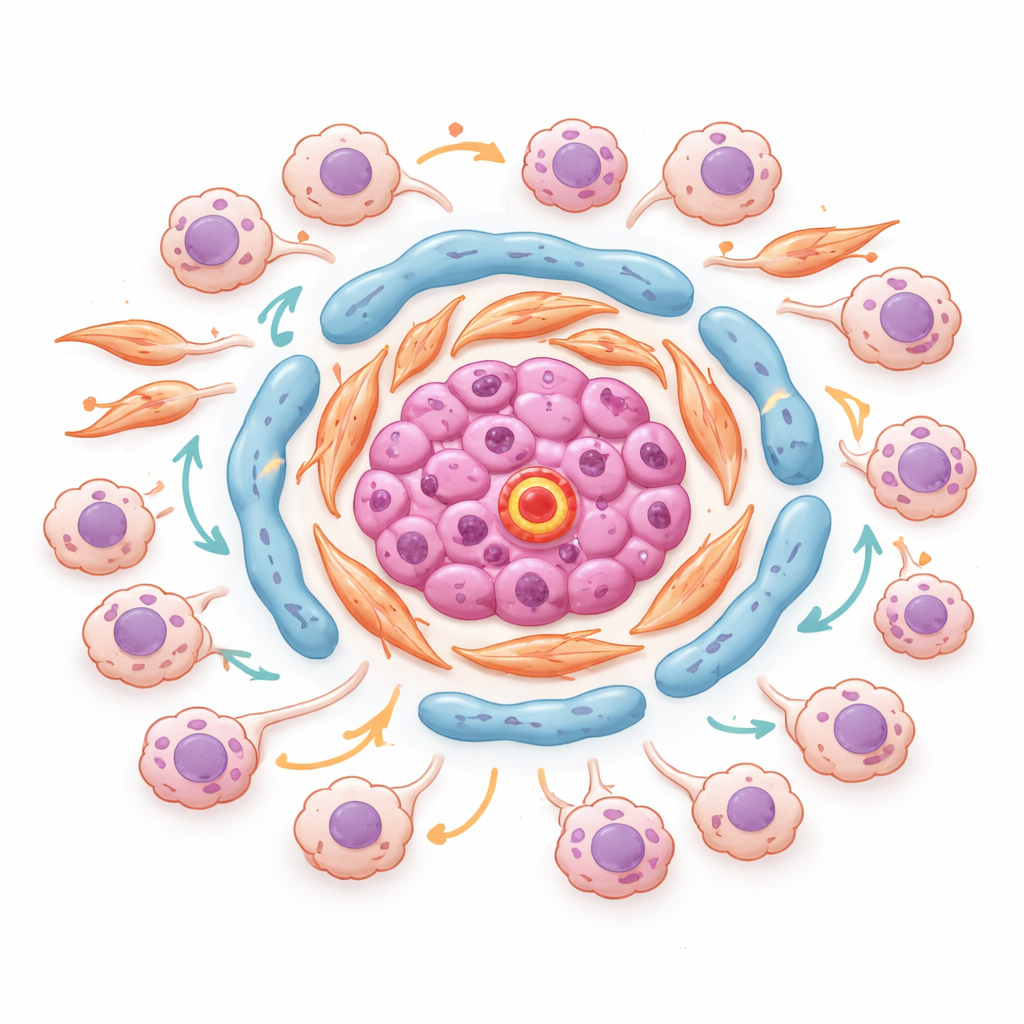
Vendo bairros perigosos dentro dos tumores
Usando transcriptômica espacial, que mede a atividade gênica sem perder o mapa de onde cada ponto se localiza no tecido, os autores identificaram “bairros” organizados dentro dos tumores. Em um tumor representativo, células endoteliais ricas em uma molécula chamada ESM1 se agruparam com fibroblastos produtores de matriz e ávidos por lipídios no núcleo de ilhas estromais. Ao redor desses núcleos acumularam‑se células cancerosas dirigidas por estresse e invasivas, em regiões com sinais fortes de TGF‑beta e baixa oxigenação. Fatores de transcrição chave que controlam como as células respondem ao estresse e à inflamação foram compartilhados entre esses estados cancerosos e estavam mais ativos exatamente onde as células tumorais tocavam esses hubs estromais. Isso sugere que micro‑nichos específicos nas fronteiras tumor–estroma estimulam ativamente as células cancerosas a mudar de estado, tornarem‑se mais agressivas e resistentes à terapia.
Encontrando um ponto fraco comum para novos tratamentos
Para avançar da descrição para a intervenção, a equipe usou um modelo de aprendizado de máquina treinado em milhões de células para simular “nocaute virtual” de genes e prever quais alterações poderiam empurrar células nocivas de volta a estados mais saudáveis. Comparando macrófagos, células endoteliais e células cancerosas, eles encontraram um pequeno conjunto de genes cuja remoção ajudava a normalizar os três tipos. Entre eles, HSP90B1 se destacou: linhagens celulares cancerosas dependem fortemente dele, ele é superexpresso em tumores hepáticos — especialmente naqueles que resistem a drogas dirigidas e à imunoterapia — e altos níveis predizem pior sobrevida. HSP90B1 codifica uma chaperona de manejo de estresse na fábrica de dobramento proteico da célula que sustenta muitos receptores de superfície e vias de sinalização. Como já existem fármacos seletivos contra essa chaperona que também podem remodelar o ambiente imune, o estudo propõe HSP90B1 como um alvo promissor para superar resistência, especialmente quando combinado com tratamentos correntes para câncer de fígado.
O que isso significa para pacientes e terapias
Em conjunto, este trabalho mostra que o câncer de fígado não é uma única doença, mas um ecossistema dinâmico de estados celulares e nichos que mudam à medida que o tumor cresce e se espalha. Ao conectar personalidades específicas de células cancerosas, células de suporte e bairros espaciais ao desfecho do paciente e à resposta a medicamentos, o estudo oferece um roteiro para tratamentos mais precisos: combinar terapias aos estados celulares dominantes, desmantelar hubs estromais que cultivam comportamentos agressivos e direcionar dependências compartilhadas como HSP90B1 das quais muitas células tumorais e do microambiente dependem. Embora sejam necessários mais testes laboratoriais e clínicos, o atlas que essa equipe construiu fornece um plano detalhado para transformar a complexidade interna do tumor de um obstáculo em uma oportunidade para terapias hepáticas mais inteligentes e duradouras.
Citação: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Palavras-chave: carcinoma hepatocelular, análise de célula única, microambiente tumoral, transcriptômica espacial, HSP90B1