Clear Sky Science · pt
Perda do microRNA-29b promove a redução do STING mediada por DNMT3b para atenuar a imunidade antitumoral induzida por radioterapia em câncer colorretal com mutação em KRAS
Por que esta pesquisa é importante
Para muitas pessoas com câncer retal e de cólon, a radioterapia é parte fundamental do tratamento antes da cirurgia. Ainda assim, alguns tumores mal encolhem, e o câncer frequentemente retorna ou se espalha. Este estudo investiga um dos defeitos genéticos comuns no câncer colorretal — a mutação em KRAS — para explicar por que esses tumores costumam resistir à radioterapia e às novas imunoterapias, e propõe uma estratégia para reativar o próprio sistema imune do organismo contra eles.
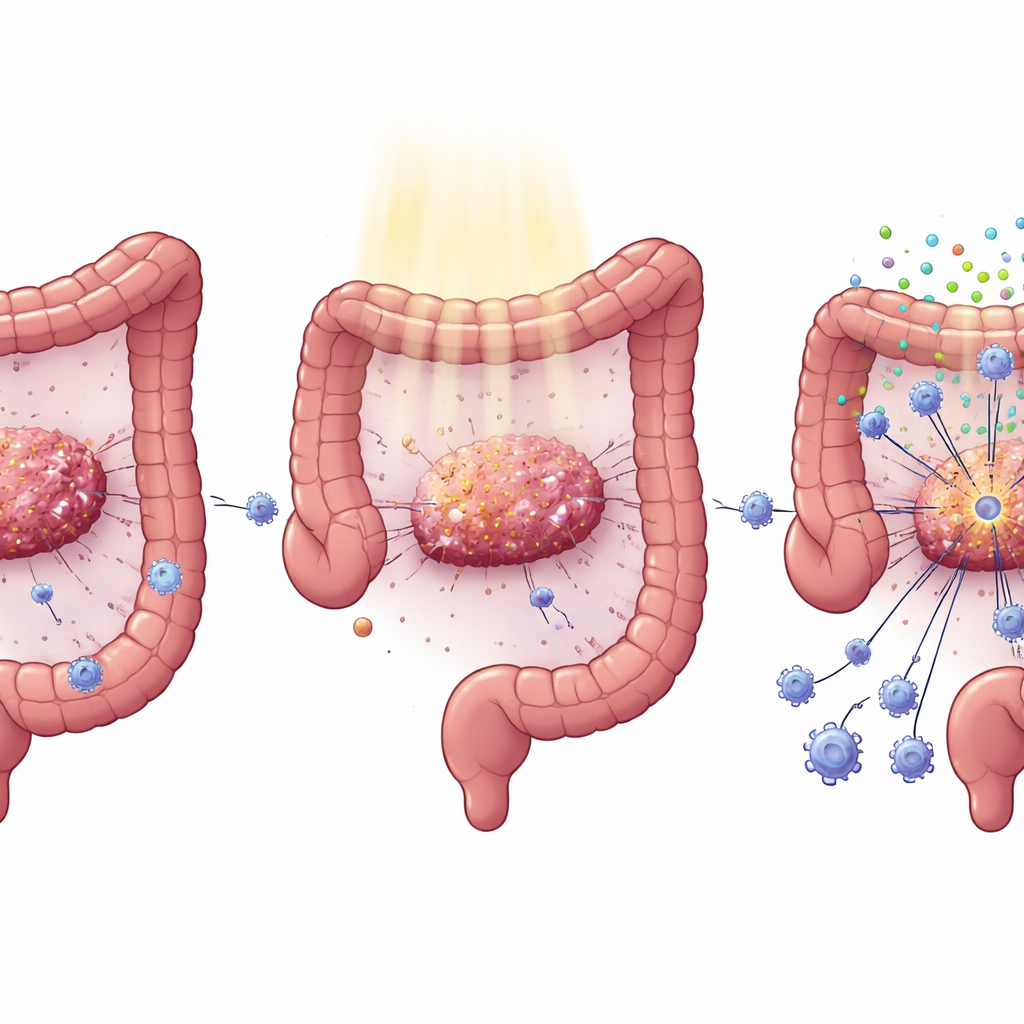
Uma mutação comum que esconde os tumores do ataque imune
O câncer colorretal frequentemente apresenta mutações no gene KRAS, um importante indutor do crescimento e da disseminação tumoral. Clínicos já haviam observado que tumores com mutação em KRAS tendem a responder mal tanto a drogas direcionadas quanto à radioterapia. Ao minerar grandes bancos de dados oncológicos e examinar amostras de pacientes, os autores descobriram que tumores com KRAS mutante apresentam menos células T CD8 citotóxicas e menor atividade dos sinais de interferon que potencializam a resposta imune. Em pacientes submetidos ao tratamento padrão com quimiorradioterapia antes da cirurgia para câncer retal, aqueles com KRAS normal ganharam muito mais células T CD8 dentro de seus tumores após o tratamento do que os com mutações em KRAS, o que ajuda a explicar seus melhores desfechos.
O sistema de alarme interno ausente nas células tumorais
A radioterapia não apenas danifica o DNA tumoral; ela também pode agir como um sinalizador, fazendo com que células cancerosas liberem fragmentos de DNA que disparam uma via de alarme interna chamada cGAS–STING. Quando o STING está ativo, as células produzem interferons do tipo I e outros sinais que atraem e ativam células imunes, incluindo células T e células dendríticas. Os pesquisadores demonstraram que, em células de câncer colorretal geneticamente modificadas para carregar KRAS mutante, esse sistema de alarme fica comprometido: após a radiação, essas células produziram muito menos interferon e moléculas relacionadas. Em camundongos, silenciar o KRAS nos tumores restaurou os níveis de STING, reforçou os sinais de interferon e levou a mais células T CD4 e CD8, menos células T reguladoras e melhor controle tumoral — não apenas nos tumores irradiados, mas também em tumores distantes não irradiados (efeito abscopal).
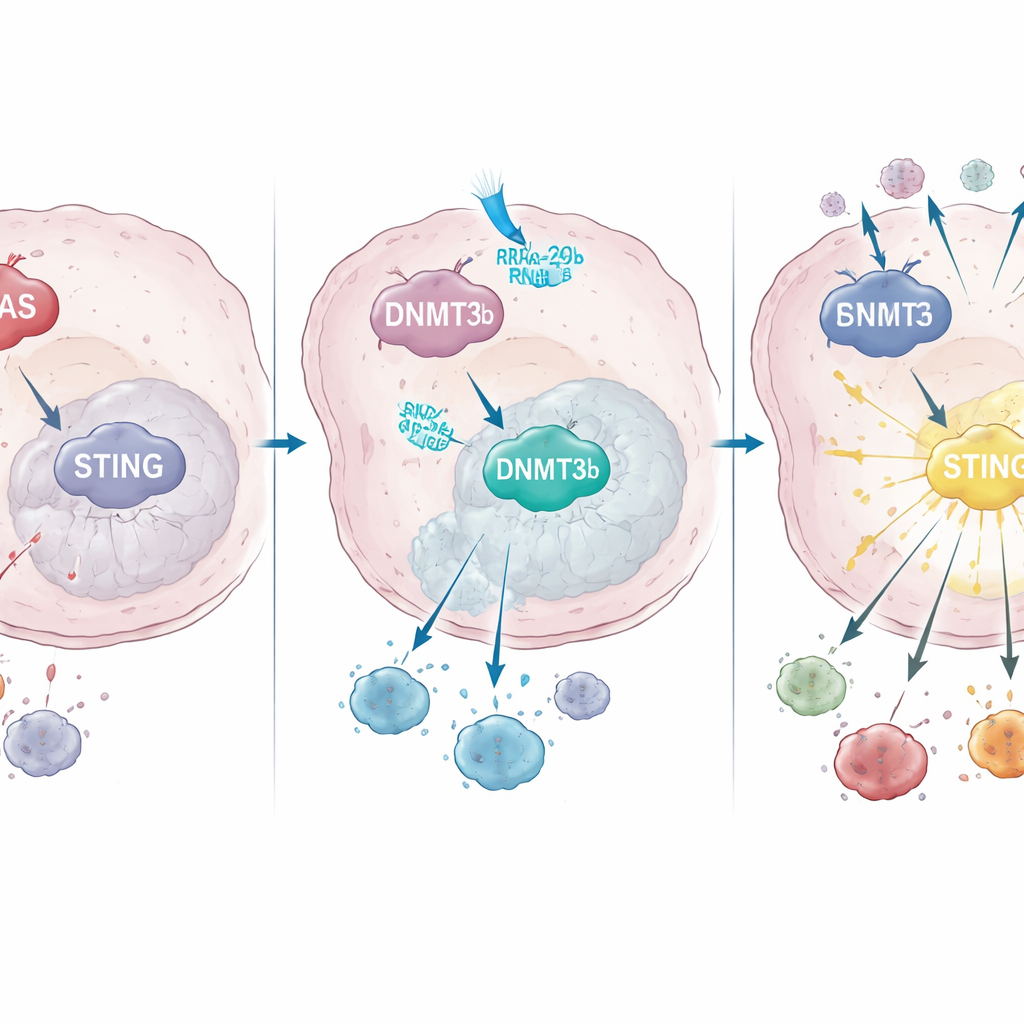
Como o KRAS reprograma o controle gênico para desligar o STING
Aprofundando-se, a equipe descobriu que o KRAS mutante aumenta a atividade de uma enzima modificadora do DNA chamada DNMT3b, que adiciona grupos metil a certas regiões do DNA e silencia genes próximos. Em linhas celulares tumorais e em amostras de pacientes, altos níveis de DNMT3b estavam associados a baixos níveis de STING. Um trecho importante do promotor de STING — a região “liga/desliga” do DNA — estava fortemente metilado em tumores com KRAS mutante, mas não naqueles com KRAS normal. Pacientes cujos tumores ainda conseguiam aumentar a expressão de STING após quimiorradioterapia tiveram maior infiltração de células T CD8 e sobrevivência melhor, ressaltando a importância dessa via para o sucesso do tratamento.
Um pequeno RNA que pode reativar o alarme
Os autores então investigaram o que torna o DNMT3b tão abundante no câncer com KRAS mutante. Usando sequenciamento de microRNAs, identificaram um pequeno RNA regulador, o microRNA‑29b‑3p, que normalmente mantém o DNMT3b sob controle, mas é fortemente suprimido pelo KRAS mutante. Restaurar esse microRNA em células KRAS-mutantes cultivadas em laboratório reduziu o DNMT3b, reativou o STING e aumentou a produção de interferon após a radiação; bloqueá‑lo teve o efeito oposto. Em amostras tumorais, pacientes com KRAS mutante tendiam a apresentar baixo microRNA‑29b‑3p, DNMT3b alto e STING baixo, e aqueles com níveis mais altos de microRNA‑29b‑3p viveram mais, ligando essa cadeia molecular aos desfechos clínicos.
Uma abordagem de entrega gênica direcionada que potencializa radioterapia e imunoterapia
Para traduzir essas descobertas em um possível tratamento, a equipe projetou um vírus inofensivo (AAV) que entrega microRNA‑29b‑3p sob o controle de um promotor ativo principalmente em células de câncer colorretal. Em modelos murinos com tumores colorretais KRAS-mutantes, administrar esse AAV junto com radioterapia localizada reduziu drasticamente tanto os tumores irradiados quanto tumores distantes que não receberam radiação. Os tumores apresentaram menos DNMT3b, mais STING, sinais de interferon aumentados e intensa infiltração por células T e outras células imunes. Quando o mesmo tratamento com microRNA‑29b‑3p foi combinado com um inibidor de checkpoint imune dirigido ao PD‑1, a sobrevida melhorou ainda mais — e esse benefício dependia de células T CD8, confirmando que o sistema imune foi responsável pelo efeito.
O que isso pode significar para pacientes
Em termos simples, este estudo revela como cânceres colorretais com mutação em KRAS “cortam o fio” de um sistema de alarme interno que a radiação normalmente dispara, permitindo que escapem do ataque imune. Ao restaurar um único pequeno RNA, o microRNA‑29b‑3p, os pesquisadores conseguiram reduzir o DNMT3b, reativar o STING e transformar tumores imunologicamente “frios” em “quentes”, que respondem melhor tanto à radioterapia quanto ao bloqueio de checkpoints. Embora este trabalho ainda esteja em fase pré-clínica, aponta para tratamentos futuros que combinem radiação com terapia gênica direcionada ao tumor para superar a resistência em câncer colorretal com KRAS mutante, potencialmente tornando as terapias existentes eficazes para muito mais pacientes.
Citação: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Palavras-chave: Câncer colorretal com mutação em KRAS, resistência à radioterapia, via STING, microRNA-29b, imunologia tumoral