Clear Sky Science · pt
Análise comparativa de estratégias de monitoramento de ctDNA em NSCLC avançado com mutações de salto do éxon 14 de MET tratadas com ensartinibe
Por que um exame de sangue importa no câncer de pulmão
Para pessoas com câncer de pulmão avançado, uma das maiores questões é se um novo medicamento está realmente funcionando — e quão cedo os médicos podem saber. Este estudo explora uma abordagem baseada em sangue, usando pequenos fragmentos de DNA tumoral que circulam na corrente sanguínea, para avaliar rapidamente o quanto um fármaco direcionado chamado ensartinibe está ajudando pacientes cujos tumores compartilham uma falha genética específica. Os achados sugerem que um simples exame de sangue precoce pode indicar quais pacientes provavelmente terão benefício prolongado com o tratamento e quais podem precisar mudar de estratégia.
Colocando as impressões digitais do tumor em um tubo de sangue
Células cancerígenas liberam pedaços de seu material genético no sangue, conhecidos como DNA tumoral circulante. Neste ensaio, os pesquisadores se concentraram em pessoas com câncer de pulmão não pequenas células impulsionado por uma alteração no gene MET, especificamente um defeito conhecido como salto do éxon 14. Todos os pacientes receberam ensartinibe após falha de tratamentos prévios. Amostras de sangue foram coletadas pouco antes do início do medicamento e novamente quatro semanas depois. Usando um teste avançado de sequenciamento que analisa 229 genes relacionados ao câncer, a equipe agrupou as alterações detectadas em três categorias: mudanças no próprio MET, um conjunto de genes conhecidos por dirigir o câncer e um grupo amplo que engloba qualquer mutação detectável.
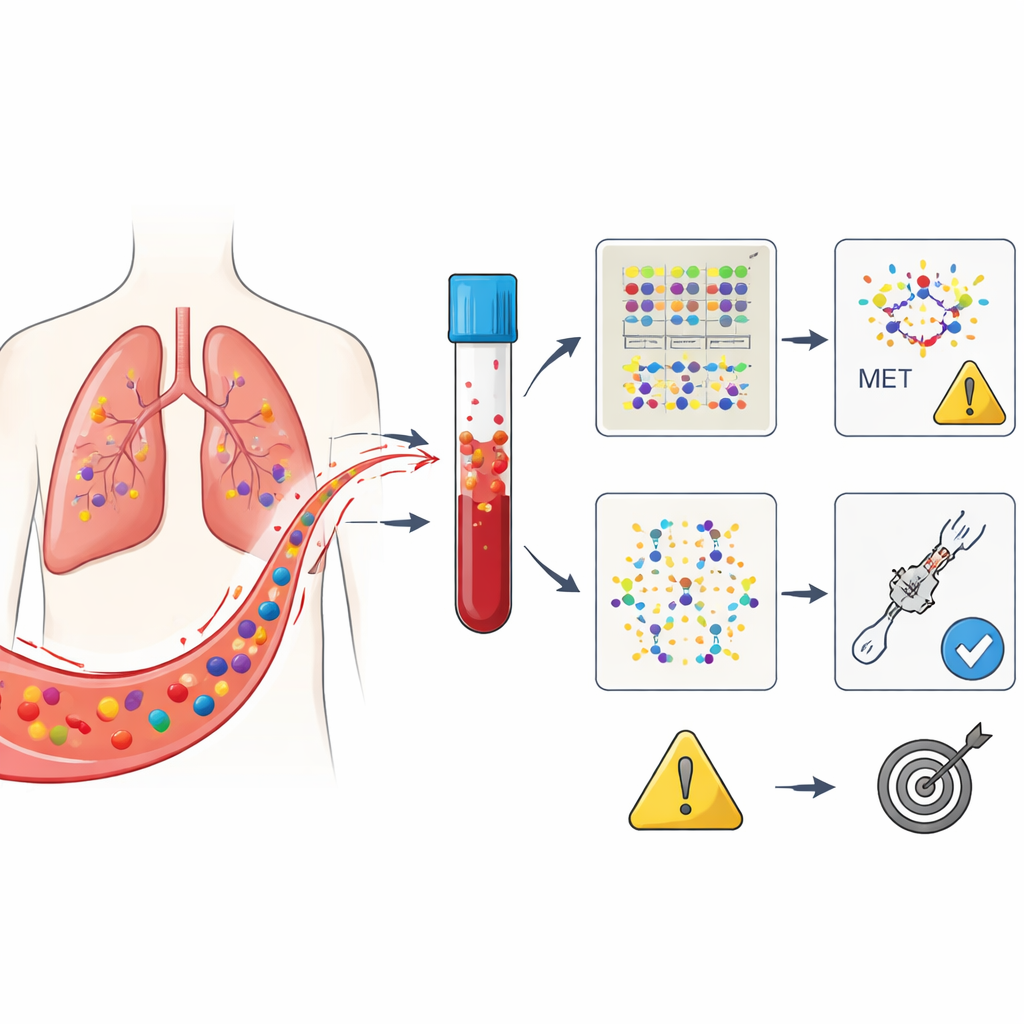
Três maneiras de ler o mesmo sinal sanguíneo
A questão central era qual dessas três “visões” sanguíneas melhor prevê quem responderá ao ensartinibe e por quanto tempo essa resposta vai durar. No início, nem todos os pacientes tinham DNA tumoral detectável no sangue, apesar de seus tumores apresentarem o defeito em MET; isso reflete o quanto os tumores liberam DNA de forma desigual. Logo no início, simplesmente ser positivo ou negativo para DNA tumoral na linha de base não previu fortemente o desfecho. No entanto, aos quatro semanas surgiu um padrão claro: pacientes cujo sangue não mostrou mais alterações relacionadas ao MET tenderam a permanecer sem piora da doença por muito mais tempo do que aqueles em que esses sinais persistiram. Isso foi observado mesmo quando as tomografias do tumor naquele momento podiam ainda ser ambíguas.
Quando os sinais de MET desaparecem, os resultados melhoram
Ao analisar mais de perto como os resultados do sangue mudaram ao longo do tempo, a equipe encontrou três trajetórias. Alguns pacientes nunca tiveram DNA de MET detectável no sangue, alguns iniciaram positivos e tornaram-se negativos, e outros permaneceram positivos ou desenvolveram novas alterações em MET. Aqueles que eliminaram os sinais de MET na quarta semana desfrutaram do maior intervalo antes da progressão da doença, cerca de nove meses em média, e tiveram a maior taxa de redução mensurável do tumor. Pacientes que permaneceram positivos para DNA de MET tiveram desempenho muito pior, com progressão da doença em pouco mais de dois meses, em média. Monitorar conjuntos mais amplos de mutações também forneceu informações úteis, mas foi menos preciso porque muitas alterações de baixo nível ou não relacionadas podem confundir a interpretação.
Equilibrando simplicidade e insights mais profundos
Usar apenas o DNA relacionado ao MET como guia ofereceu a visão mais nítida e simples sobre se o ensartinibe estava funcionando. Essa abordagem focalizada teve alta especificidade, o que significa que quando os sinais de MET desapareciam havia forte probabilidade de o paciente evoluir bem. Isso a torna atraente como ferramenta prática: testes de gene único são mais baratos, mais rápidos e mais fáceis de interpretar do que painéis genômicos amplos. Ao mesmo tempo, escanear mais genes ainda tem valor, pois pode revelar novas mutações que expliquem por que um tumor deixou de responder e apontar opções terapêuticas futuras. O estudo sugere que combinar uma visão estreita, centrada em MET, para decisões precoces de tratamento com uma visão mais ampla para monitorar resistência pode oferecer o melhor dos dois mundos.
O que isso significa para os pacientes
Para um leigo, a mensagem principal é que um exame de sangue realizado apenas um mês após o início do ensartinibe já pode indicar o retorno a longo prazo do medicamento. Se o DNA tumoral relacionado ao MET desaparecer da corrente sanguínea, as chances de um benefício significativo e duradouro são altas; se persistir, os médicos podem precisar acompanhar mais de perto ou considerar outras opções. Embora este tenha sido um estudo relativamente pequeno, de braço único, que precisa ser confirmado em grupos maiores, ele reforça a ideia de que “biópsias líquidas” podem funcionar como uma avaliação precoce de tratamentos direcionados. No futuro, esse monitoramento pode ajudar a personalizar o cuidado, poupando pacientes de continuar em drogas ineficazes e orientando-os mais rapidamente para terapias que funcionam.
Citação: Zhou, M., Zhu, Y., Sun, X. et al. Comparative analysis of ctDNA monitoring strategies in advanced NSCLC with MET exon 14 skipping mutations treated with ensartinib. npj Precis. Onc. 10, 110 (2026). https://doi.org/10.1038/s41698-026-01284-6
Palavras-chave: DNA tumoral circulante, salto do éxon 14 de MET, ensartinibe, câncer de pulmão não pequenas células, monitoramento por biópsia líquida