Clear Sky Science · pt
Superexpressão da subunidade NDUFS4 do complexo I mitocondrial impulsiona a progressão de glioma ao regular a função mitocondrial e COX5B
Por que tumores cerebrais com alta demanda energética são importantes
Os gliomas estão entre os cânceres cerebrais mais agressivos, frequentemente retornando mesmo após cirurgia, radiação e quimioterapia. Este estudo examina em detalhe as células de glioma para responder a uma pergunta simples, mas de grande alcance: esses tumores dependem de uma parte específica de suas “usinas” internas para crescer e se espalhar? Ao acompanhar uma pequena proteína mitocondrial chamada NDUFS4, os pesquisadores revelam um ponto fraco metabólico que parece alimentar a progressão tumoral enquanto afeta muito menos as células cerebrais saudáveis.
Um interruptor oculto nas usinas de energia dos tumores cerebrais
Dentro de cada célula, as mitocôndrias funcionam como pequenos geradores, convertendo nutrientes em energia utilizável. Nas células de glioma, esses geradores são levados a funcionamento acelerado. A equipe analisou grandes conjuntos de dados públicos sobre câncer e dados de sequenciamento de célula única e descobriu que a proteína NDUFS4, um componente de um dos principais complexos produtores de energia nas mitocôndrias, está consistentemente elevada em tecido de glioma em comparação com o cérebro normal. Níveis mais altos de NDUFS4 correlacionaram-se com graus tumorais mais avançados e com pacientes que morreram mais precocemente em decorrência da doença. A análise em resolução de célula única mostrou que esse excesso de NDUFS4 se concentra especificamente nas células tumorais, e não nas células não cancerosas circundantes do cérebro.
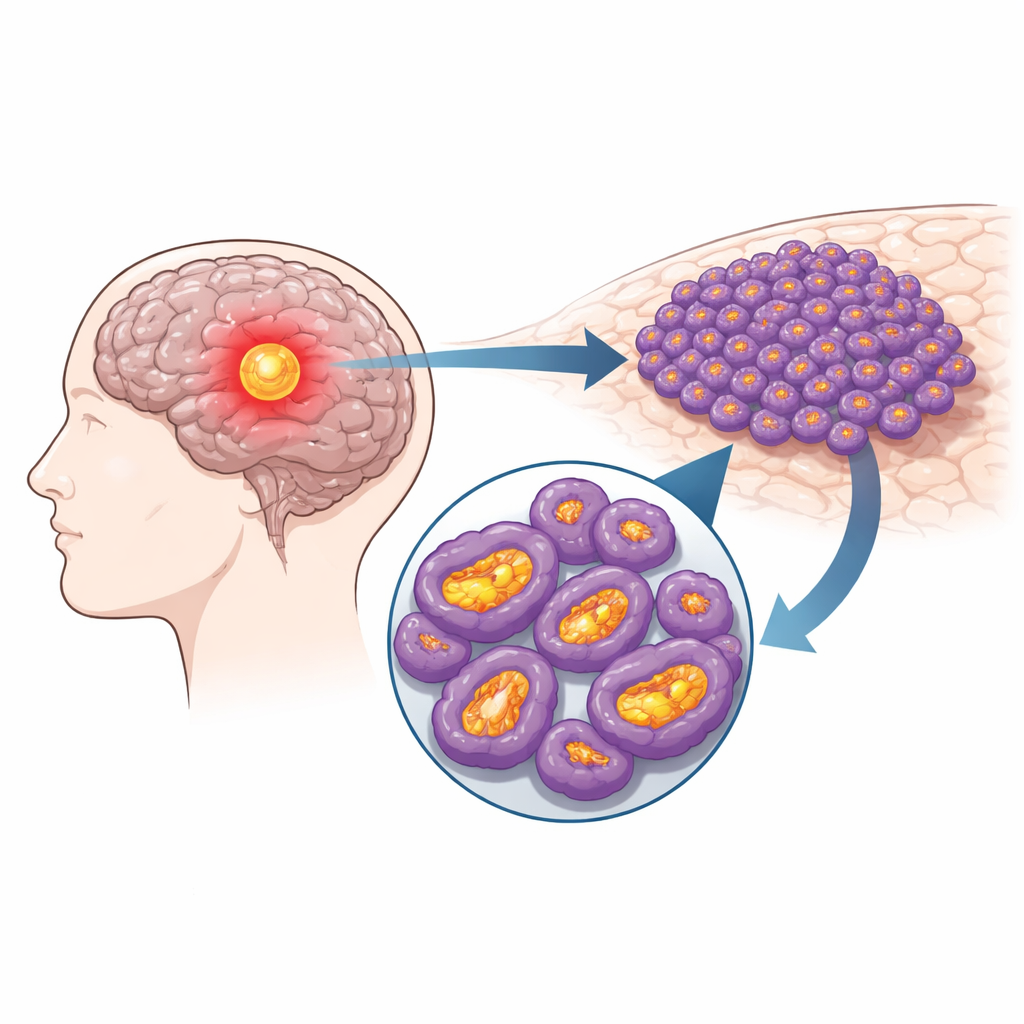
Reduzir o dial de energia para frear o câncer
Para testar se NDUFS4 é apenas um marcador ou um verdadeiro motor, os pesquisadores reduziram ou eliminaram deliberadamente sua expressão em células de glioma derivadas de pacientes cultivadas em laboratório. Quando NDUFS4 foi silenciada ou nocauteada, as mitocôndrias das células enfraqueceram: o consumo de oxigênio caiu, uma etapa chave da produção de energia desacelerou e a quantidade de combustível celular (ATP) diminuiu. Ao mesmo tempo, subprodutos danosos conhecidos como espécies reativas de oxigênio aumentaram, e as membranas internas das células mostraram sinais de estresse e oxidação. Funcionalmente, essas células tumorais com falta de energia dividiram-se menos, formaram menos colônias, moveram-se e invadiram com menos eficácia e apresentaram mais sinais de morte celular programada. Notavelmente, o mesmo impacto genético em astrócitos não cancerosos — células de suporte do tecido cerebral normal — causou pouco ou nenhum dano, sugerindo que as células tumorais dependem de forma incomum desse interruptor mitocondrial.
Aumentar a potência torna os tumores mais agressivos
O experimento inverso desenhou um quadro igualmente claro. Quando os cientistas forçaram células de glioma a produzir NDUFS4 em excesso, suas mitocôndrias tornaram-se mais ativas: a produção de energia aumentou e o complexo respiratório chave trabalhou com maior intensidade. Essas células aprimoradas cresceram mais rápido, migraram com mais facilidade e invadiram barreiras com maior agressividade, tanto em células primárias de pacientes quanto em linhagens laboratoriais padrão. Em camundongos, células de glioma geneticamente alteradas para manter altos níveis de NDUFS4 formaram tumores intracranianos maiores, enquanto células com NDUFS4 reduzido cresceram muito mais lentamente no cérebro, apresentaram desempenho mitocondrial mais fraco, mais dano oxidativo, menos células em divisão e mais células morrendo. Juntos, esses experimentos estabelecem NDUFS4 não apenas como um acompanhante, mas como um motor da progressão do glioma.
Uma proteína parceira liga o controle energético ao comportamento tumoral
Aprofundando a investigação, a equipe perguntou como NDUFS4 exerce efeitos tão amplos. Ao cruzar dados de expressão gênica de tumores em conjunto, de células únicas e mapas de proteínas de células cancerosas, eles identificaram outra proteína mitocondrial, COX5B, como parceira chave. COX5B ajuda a operar a etapa final da principal cadeia de energia da célula. Ela apresentou forte correlação com os níveis de NDUFS4 em gliomas e já é conhecida por estar elevada em outros cânceres. Quando os pesquisadores reduziram COX5B em células de glioma, observaram o mesmo padrão visto com a perda de NDUFS4: desempenho mitocondrial enfraquecido, mais estresse oxidativo, crescimento e migração mais lentos e aumento da morte celular. Crucialmente, quando restauraram COX5B em células com NDUFS4 depletada, grande parte do dano mitocondrial e do efeito antitumoral foi revertida. Eles também descobriram que NDUFS4 influencia a força com que um fator de transcrição (Sp1) se liga à região de controle do gene COX5B, ajudando a ajustar quanto COX5B a célula produz.
O que isso significa para tratamentos futuros do câncer cerebral
Para um não especialista, a mensagem central é que muitos gliomas parecem depender de um sistema energético supercarregado centrado em NDUFS4 e seu parceiro downstream COX5B. Reduzir a atividade desse sistema priva as células tumorais do combustível e do equilíbrio necessários para crescer e invadir, ao passo que deixa as células de suporte cerebrais normais relativamente intactas. Como essa vulnerabilidade aparece de forma consistente em amostras de pacientes, células isoladas e tumores cerebrais de camundongo, NDUFS4 — e seu controle sobre COX5B — despontam como um alvo promissor para novas drogas. Terapias que perturbem seletivamente esse “circuito de energia” mitocondrial podem complementar os tratamentos existentes, potencialmente retardando o crescimento tumoral e prolongando a sobrevida sem prejudicar severamente o tecido cerebral saudável.
Citação: Wu, J., Li, J., Xu, L. et al. Mitochondrial complex I subunit NDUFS4 overexpression drives glioma progression by regulating mitochondrial function and COX5B. npj Precis. Onc. 10, 99 (2026). https://doi.org/10.1038/s41698-026-01281-9
Palavras-chave: glioma, mitocôndrias, NDUFS4, COX5B, metabolismo do câncer cerebral