Clear Sky Science · pt
Neoadjuvância com sintilimabe, paclitaxel ligado à albumina e carboplatina para carcinoma escamoso do esôfago localmente avançado e ressecável: estudo clínico e exploração mecanística
Virando a Maré Contra um Letal Câncer de Garganta
O câncer esofágico está entre os mais letais no mundo, frequentemente detectado apenas depois de progredir profundamente no tórax. Muitos pacientes ainda são candidatos à cirurgia, mas mesmo com a melhor quimioterapia e radioterapia atuais, o risco de recidiva é alto. Este estudo testa uma nova estratégia para reforçar as defesas do próprio corpo antes da cirurgia e investiga sob o microscópio como os tumores e as células ao redor mudam em resposta. Os achados apontam para tratamentos mais eficazes e um caminho rumo a cuidados verdadeiramente personalizados.
Um Novo Plano de Três Fármacos Antes da Cirurgia
Os pesquisadores inscreveram 24 pessoas na China com uma forma comum e agressiva de câncer esofágico chamada carcinoma escamoso. Todos apresentavam tumores avançados, mas ainda ressecáveis. Antes da operação, cada paciente recebeu três ciclos de um tratamento combinado: sintilimabe, um anticorpo que ativa o sistema imune e ajuda os linfócitos T a reconhecer o câncer; além de dois quimioterápicos padrão, paclitaxel ligado à albumina e carboplatina. Após essa fase “neoadjuvante”, os pacientes foram submetidos à cirurgia para remover o tumor do esôfago, e a maioria continuou com sintilimabe depois da cirurgia.
Redução Tumoral Mais Profunda e Sobrevida Animadora
Quando cirurgiões e patologistas examinaram os tumores removidos, observaram que esse regime pré-operatório produziu retração profunda em muitos pacientes. Cerca de 42% apresentaram o que os médicos chamam de resposta patológica major, significando que apenas uma pequena fração de células tumorais viáveis permaneceu. Um em cada três pacientes não apresentou células cancerosas detectáveis na área principal do tumor. Em imagens e acompanhamento clínico, os resultados também foram promissores: três anos após o tratamento, aproximadamente três em cada quatro pacientes estavam vivos sem sinais de recidiva, e quase quatro em cada cinco ainda estavam vivos. Importante, os efeitos colaterais desse plano intensificado foram manejáveis, sem mortes relacionadas ao tratamento e com a ressecção cirúrgica permanecendo segura e viável.
Como o Vizinhança do Tumor Molda a Resposta
Nem todos os pacientes se beneficiaram da mesma forma, então a equipe investigou por quê. Eles focaram no microambiente tumoral — o complexo conjunto de células cancerosas, células imunes e moléculas sinalizadoras. Usando medições proteicas direcionadas em amostras tumorais cuidadosamente dissecadas, compararam quem respondeu bem com quem não respondeu. Antes do tratamento, identificaram 14 proteínas que diferiam entre esses dois grupos. Uma proteína de superfície, CD44, destacou-se: tumores com níveis mais altos de CD44 tendiam a responder melhor à terapia à base de sintilimabe. Após o tratamento, muitas proteínas envolvidas na atividade imune e no reparo de DNA estavam reduzidas nos respondedores, sugerindo que a terapia combinada desestabilizou com sucesso os sistemas de suporte do câncer e remodelou a paisagem imune local.
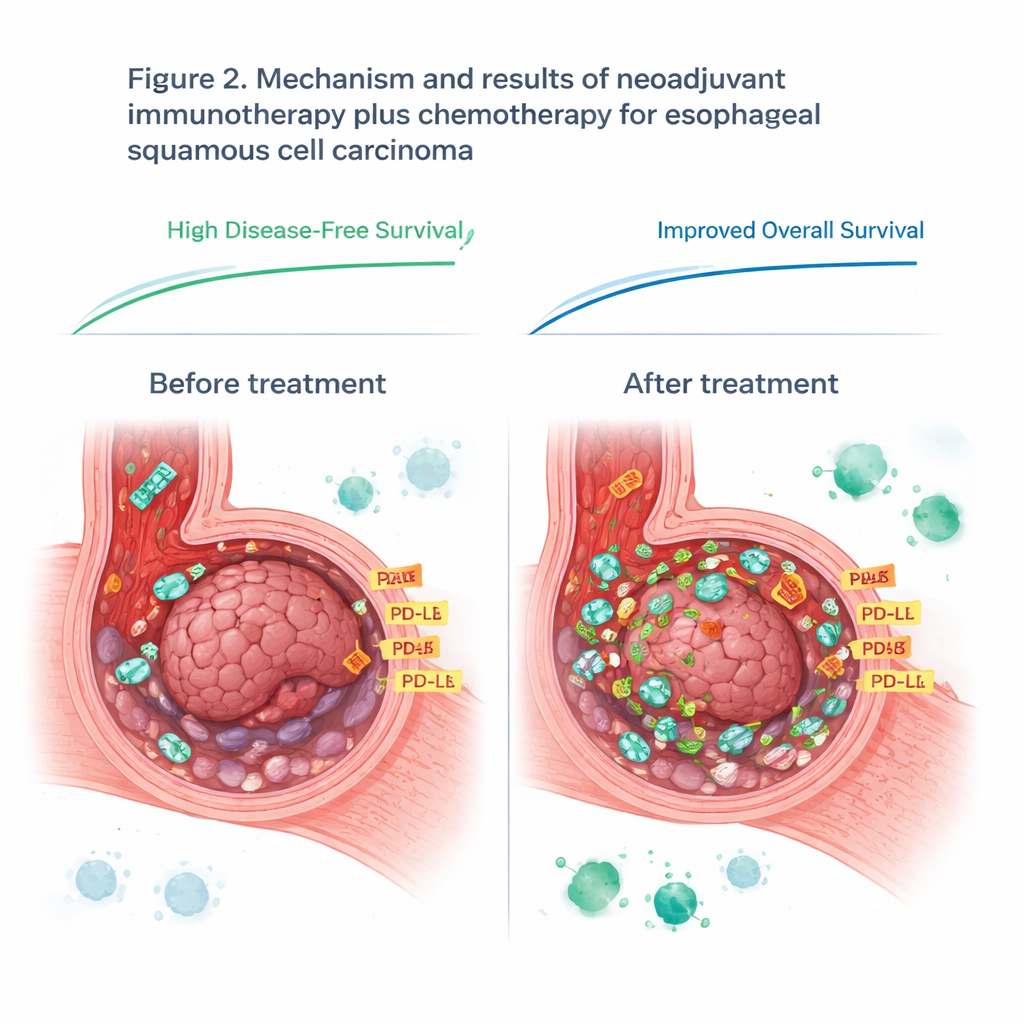
Repensando um Marcador Imune Popular
O estudo também examinou o PD-L1, uma proteína frequentemente usada como bússola para decidir quem pode se beneficiar de drogas que bloqueiam pontos de checagem imune. Antes do tratamento, os níveis de PD-L1 nas amostras tumorais não previram quem teria bom desfecho, desafiando a prática corrente nesse tipo de câncer. Entretanto, os níveis de PD-L1 aumentaram em todos os pacientes durante o tratamento, provavelmente porque o sistema imune ativado inundou o tumor com sinais inflamatórios. Após a terapia, níveis mais altos de PD-L1 no tecido tumoral remanescente estiveram mais relacionados ao desempenho da imunoterapia. Isso sugere que o timing importa: uma única medida de PD-L1 antes do tratamento pode perder mudanças cruciais que ocorrem quando o sistema imune é ativado.
O Que Isso Significa para Pacientes e para o Futuro
Para pessoas prestes a ser operadas por câncer esofágico avançado, este estudo traz duas mensagens esperançadoras. Primeiro, combinar sintilimabe com quimioterapia antes da cirurgia parece reduzir os tumores de forma mais profunda e pode aumentar as chances de sobrevida a longo prazo, sem adicionar efeitos adversos perigosos. Segundo, o trabalho mostra que o tumor e seu microambiente não são estáticos; são remodelados pelo tratamento em modos que podem ser monitorados por proteínas como PD-L1 e CD44. No futuro, essas assinaturas moleculares poderão ajudar os médicos a selecionar e ajustar terapias em tempo real, convertendo mais tumores “frios” que ignoram o sistema imune em tumores “quentes” que atraem um ataque imune poderoso e duradouro.
Citação: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Palavras-chave: câncer esofágico, imunoterapia, terapia neoadjuvante, inibidores de PD-1, microambiente tumoral