Clear Sky Science · pt
Transcriptômica espacial revela heterogeneidade molecular e alvos terapêuticos específicos por subtipo no câncer de pulmão de pequenas células
Por que este estudo sobre câncer de pulmão é importante
O câncer de pulmão de pequenas células é uma das formas mais letais de câncer, acometendo principalmente pessoas com histórico de tabagismo e frequentemente retornando rapidamente após quimioterapia. Os médicos sabem que nem todos os tumores desse tipo se comportam da mesma forma, mas faltavam ferramentas para visualizar como diferentes tipos de células tumorais e células imunes estão organizadas dentro de cada tumor. Este estudo utilizou uma tecnologia nova que lê a atividade gênica em milhares de pontos minúsculos ao longo de uma lâmina tumoral, criando um “mapa molecular” de cada amostra. Ao combinar isso com análises computacionais personalizadas, os pesquisadores descobriram padrões ocultos que podem apontar para tratamentos mais precisos e específicos por subtipo.
Mapeando os tumores no local
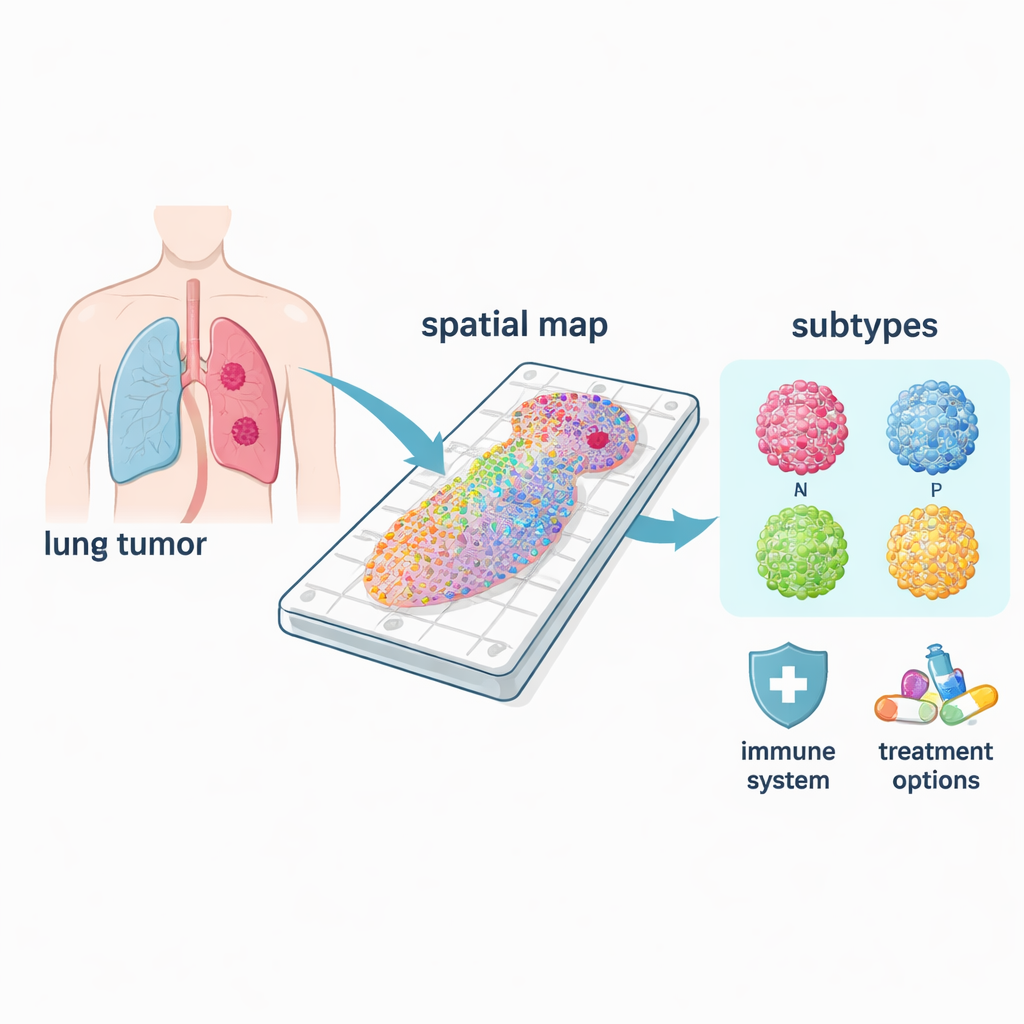
A equipe analisou amostras tumorais de 21 pacientes com câncer de pulmão de pequenas células em estágio limitado que foram submetidos à cirurgia antes de receber qualquer medicação. Em vez de triturar o tecido e perder toda a informação espacial, eles aplicaram transcriptômica espacial: uma técnica que mede quais genes estão ativados em muitos pontos definidos ao longo de uma seção de tecido. Cada ponto permanece em sua posição original, permitindo aos cientistas vincular a atividade gênica ao local físico onde residem células tumorais, células normais e células imunes. Eles acrescentaram duas ferramentas-chave: um novo escore “Edgeindex” para quantificar o quão profundamente as células tumorais infiltram o tecido vizinho, e uma rede neural artificial — uma forma de aprendizado de máquina — para marcar automaticamente quais pontos são tumorais e quais não são.
Diferentes tipos de câncer em uma mesma doença
O câncer de pulmão de pequenas células não é uma única doença, mas inclui pelo menos quatro subtipos moleculares principais, frequentemente chamados de ASCL1, NEUROD1, POU2F3 e YAP1, em referência a genes regulatórios que os definem. Usando seus mapas espaciais, os pesquisadores puderam ver onde cada subtipo predominava dentro dos tumores e como suas biologias diferiam. As formas comuns ASCL1 e NEUROD1 foram fortemente associadas a programas de divisão celular, compatíveis com sua reputação de alta proliferação. Em contraste, as regiões POU2F3 estavam ligadas a vias relacionadas ao sistema imune, enquanto áreas YAP1 exibiram sinais relacionados ao metabolismo e remodelação tecidual, características que podem se conectar à disseminação e resistência ao tratamento. Como esses padrões são resolvidos espacialmente, o método pode identificar o verdadeiro subtipo “motor” dentro de um tumor misto — algo que testes em massa frequentemente não detectam.
A borda invasora e a mudança imune
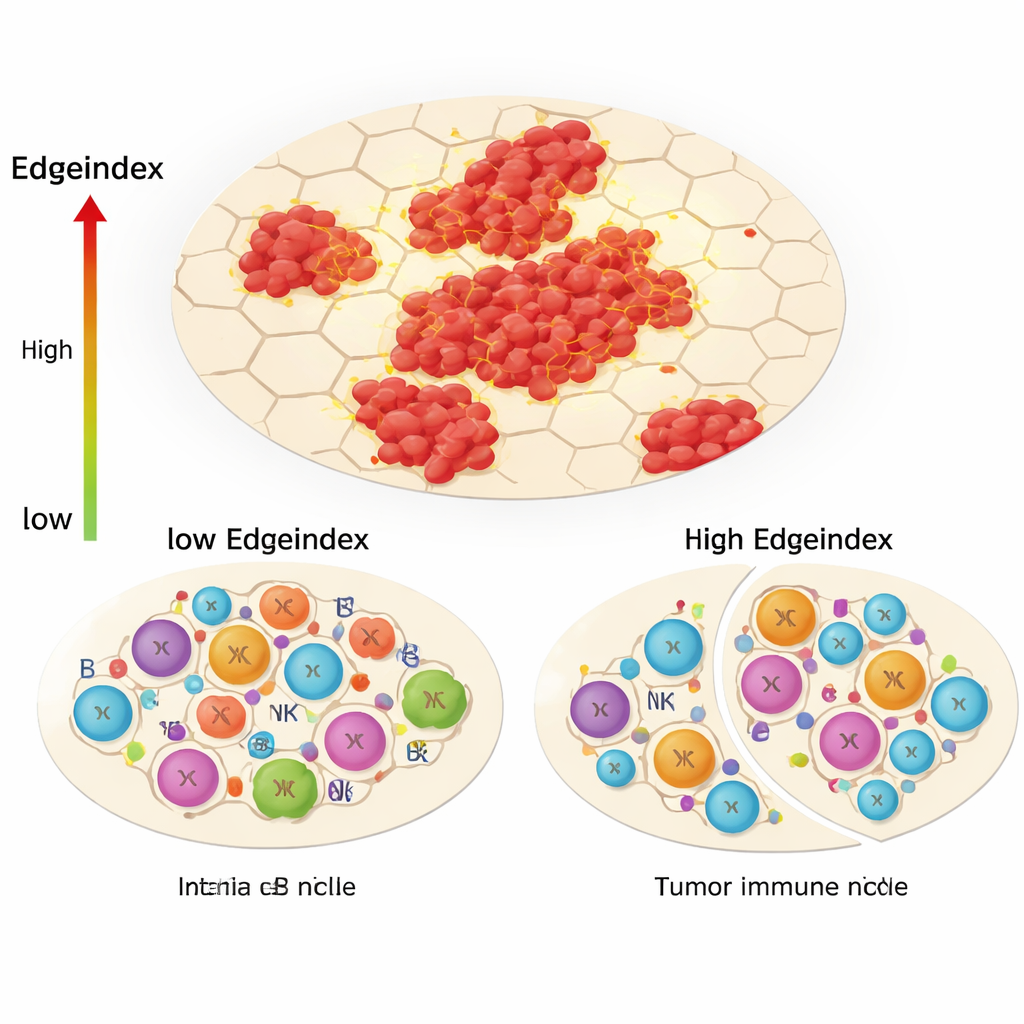
Uma das inovações centrais do estudo, o Edgeindex, captura o quanto as células tumorais se misturam com o tecido não tumoral ao redor. Escores baixos refletem tumores compactos e bem delimitados, enquanto escores altos indicam ilhas dispersas e bordas irregulares e invasivas. Tumores com Edgeindex alto foram enriquecidos em programas gênicos relacionados à matriz extracelular, metástase e morte celular. Eles também exibiram um panorama imune fortemente alterado: menos células T auxiliares e outros componentes da resposta imune adaptativa, mas mais células inatas como certos linfócitos natural killer e monócitos. Os autores interpretam isso como um “remodelamento do nicho imunológico”, no qual o tumor afasta respostas imunes precisas e direcionadas, deixando um componente mais ineficaz e largamente inato que não consegue controlar plenamente o câncer.
Diversidade oculta dentro e ao redor dos tumores
Além dos padrões de subtipo e invasão, os dados espaciais revelaram que tanto as populações de células tumorais quanto seus microambientes circundantes eram internamente diversos. Ao agrupar pontos dentro de cada tumor, a equipe contou quantos bairros de expressão gênica distintos existiam nas regiões tumorais e no tecido não tumoral próximo. Maior diversidade dentro do tumor se relacionou a vias associadas ao sistema imune, enquanto certos padrões no tecido adjacente se ligaram à atividade do ciclo celular e à regulação genética. Os pesquisadores também examinaram quão intensamente diferentes regiões “se comunicavam” usando moléculas de sinalização conhecidas. Tumores com comunicação mais intensa entre regiões tendiam a mostrar sinais imunes mais fortes, reforçando a ideia de que a atividade imune e o crescimento tumoral estão fortemente interligados no espaço.
Acompanhando o desenvolvimento do tumor ao longo do tempo
Para aproximar como as células tumorais mudam conforme a doença progride, a equipe realizou uma análise de “pseudotempo” que ordena as células ao longo de um trajeto de desenvolvimento com base em sua atividade gênica. Entre as amostras, eles identificaram repetidamente um gene, UCHL1, como central nessas trajetórias. Níveis elevados de UCHL1 coincidiram com forte atividade do ciclo celular em pontos tumorais, enquanto níveis mais baixos se alinharam com vias imunes e de morte celular. Como UCHL1 é uma proteína de tipo neural anteriormente associada a cânceres de pulmão agressivos, esses achados reforçam a possibilidade de que ela seja um alvo terapêutico útil, particularmente para as células de caráter neuroendócrino que impulsionam o câncer de pulmão de pequenas células.
O que isso significa para os pacientes
Em termos práticos, este estudo transforma lâminas de microscópio planas de câncer de pulmão de pequenas células em mapas ricos e em camadas que mostram onde cada subtipo de tumor está localizado, quão agressivamente invade, como se comunica com o entorno e como o sistema imune responde ou falha. O novo escore Edgeindex e a abordagem de mapeamento destacam quais tumores são especialmente infiltrativos e quais células imunes estão presentes ou ausentes na borda. Ao vincular esses padrões espaciais a vulnerabilidades específicas por subtipo — como medicamentos que têm alvos em DLL3, BCL‑2, AURKA, IGF‑1R/PARP ou pontos de verificação imunes — o trabalho aproxima o campo de combinar cada paciente com uma estratégia terapêutica personalizada. Embora essas ferramentas ainda precisem ser testadas em estudos maiores, elas oferecem um roteiro para terapias mais precisas e potencialmente mais eficazes em um tipo de câncer que necessita urgentemente de melhores opções.
Citação: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Palavras-chave: câncer de pulmão de pequenas células, transcriptômica espacial, heterogeneidade tumoral, microambiente imune tumoral, oncologia de precisão