Clear Sky Science · pt
Métodos para avaliação randomizada, cega e controlada de intervenções putativas em redes multilaboratoriais de avaliação pré-clínica
Por que isso importa para a saúde cotidiana
Muitas terapias médicas promissoras parecem eficazes em estudos com animais, mas falham depois em grandes e caros ensaios clínicos. Este artigo mostra, em detalhes concretos, como os cientistas podem redesenhar esses testes iniciais em animais para que seus resultados sejam mais confiáveis e mais capazes de prever o que acontecerá em pacientes reais — usando o acidente vascular cerebral como caso-teste. 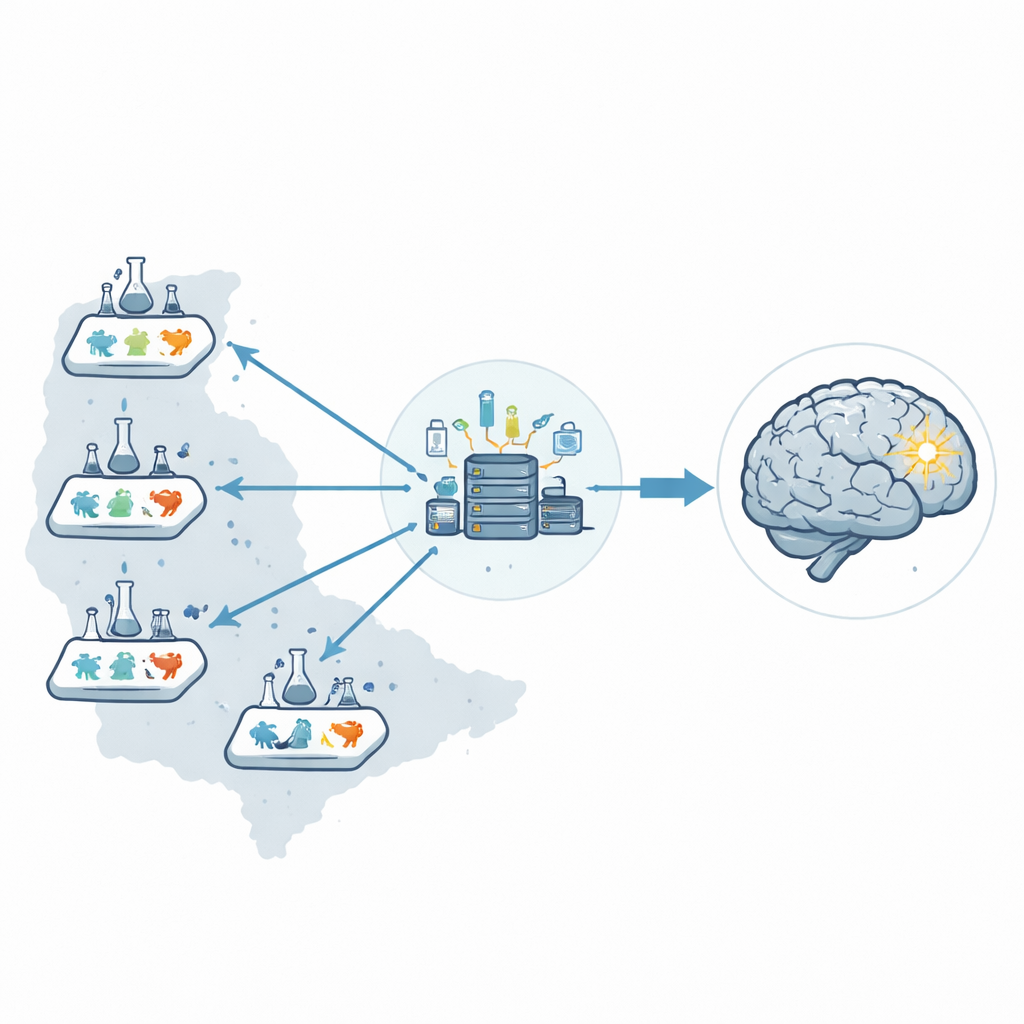
Construindo uma rede em vez de um único laboratório
Em vez de depender de um único laboratório, os pesquisadores criaram uma rede pré-clínica de seis laboratórios nos Estados Unidos, chamada Stroke Preclinical Assessment Network. Um centro coordenador central gerenciou toda a operação: envio de frascos codificados com drogas, atribuição aleatória dos tratamentos, recebimento de todos os dados e execução das estatísticas. Ao separar essas funções das pessoas que realizavam as cirurgias ou avaliavam os desfechos, reduziram a chance de que expectativas humanas influenciassem sutilmente os resultados.
Implementando imparcialidade e ocultamento
Para imitar as regras de um bom ensaio clínico, todo animal foi registrado, identificado e acompanhado desde o momento em que chegou a um laboratório. Os tratamentos foram ocultados em frascos idênticos para que os cirurgiões não pudessem distinguir drogas reais de placebos durante a indução do AVC e a administração da terapia. Um plano de randomização estruturado garantiu que machos e fêmeas, diferentes modelos de AVC e os seis locais contribuíssem de forma equilibrada para cada grupo de tratamento. Mesmo que um animal morresse ou um procedimento falhasse, ele permaneceu no registro para que as perdas não fossem silenciosamente ignoradas, ajudando a evitar vieses ocultos.
Testando tratamentos em modelos de AVC realistas
A rede utilizou cinco modelos diferentes de roedores que, em conjunto, capturaram aspectos importantes do AVC humano, incluindo idade, hipertensão e obesidade induzida por dieta. O AVC foi produzido da mesma maneira entre os locais, bloqueando brevemente uma artéria cerebral principal e então restaurando o fluxo sanguíneo — semelhante aos procedimentos modernos de remoção de coágulos em pessoas. Os animais receberam um dos seis tratamentos candidatos com potencial protetor ou um controle correspondente. A equipe os acompanhou com testes simples de movimento, como como giravam em uma esquina ou caminhavam sobre uma grade, e com exames cerebrais para medir o tamanho da lesão ao longo de 30 dias.
Escore cego, dados compartilhados e estatísticas inteligentes
Para manter os julgamentos imparciais, os testes comportamentais foram gravados em vídeo e enviados a um arquivo central. Esses vídeos, desprovidos de qualquer informação identificadora, foram enviados a avaliadores treinados em outros laboratórios, que os pontuaram sem saber qual tratamento o animal havia recebido ou onde foi testado. As imagens de ressonância magnética passaram por um fluxo de análise automatizado que segmentou o cérebro e a área lesionada com mínima intervenção humana. Todos os resultados alimentaram um desenho estatístico multi-braço e multiestágio que permitiu testar vários tratamentos em paralelo: candidatos fracos ou claramente ineficazes podiam ser descartados cedo, enquanto os promissores avançavam para estágios posteriores. 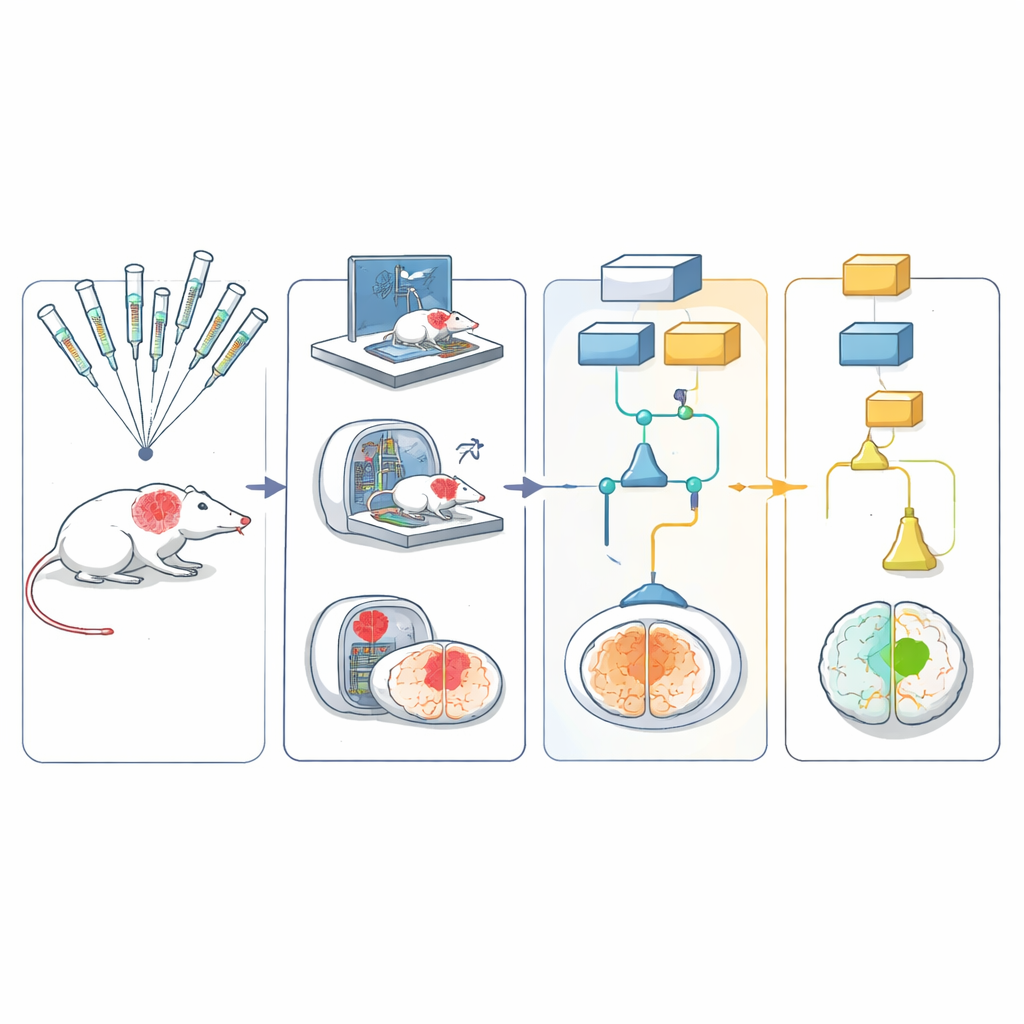
O que os resultados mostraram sobre terapias para AVC
Ao longo de quatro estágios e 2.615 animais, o sistema mostrou-se viável mesmo durante as interrupções da pandemia de COVID-19. Os métodos mantiveram consistentemente os grupos de tratamento balanceados, minimizaram erros na dosagem e mostraram melhoria na qualidade dos dados à medida que os locais progrediam na curva de aprendizado. No fim, cinco dos seis tratamentos foram descartados, enquanto um — ácido úrico, um captador de radicais livres — atingiu o limiar pré-planejado de benefício. Ao mesmo tempo, o trabalho revelou limitações de alguns modelos populares, como taxas de mortalidade muito altas em camundongos idosos, sugerindo que eles podem não ser práticos ou realistas para estudos futuros.
Visão geral: um modelo para ciência pré-clínica mais confiável
Para o leitor leigo, a mensagem principal é que a forma como testamos tratamentos em animais é tão importante quanto o que testamos. Ao importar as salvaguardas dos ensaios clínicos modernos — randomização, cegamento, registro completo de cada sujeito e estatísticas cuidadosas — para a pesquisa animal, esta rede demonstra que estudos iniciais podem ser ao mesmo tempo mais rigorosos e mais eficientes. O manual detalhado que eles fornecem pode ser adaptado a outras doenças, oferecendo um caminho para descobertas de laboratório que resistam à replicação e deem a médicos, pacientes e financiadores mais confiança de que uma terapia realmente tem chance de funcionar na clínica.
Citação: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Palavras-chave: acidente vascular cerebral, ensaios pré-clínicos, modelos animais, rigor da pesquisa, estudos multicêntricos