Clear Sky Science · pt
Transgênese mediada por PiggyBac e knockout por CRISPR–Cas9 na traça maior da cera, Galleria mellonella
Uma pequenina lagarta com grande potencial médico
Imagine testar novos antibióticos ou estudar infecções perigosas sem usar camundongos ou outros mamíferos. As larvas da traça maior da cera, Galleria mellonella, estão surgindo como um substituto de baixo custo e eticamente atraente para esses experimentos. Este estudo mostra como cientistas deram um passo importante ao fornecer a essas lagartas o mesmo tipo de ferramentas genéticas que tornaram a mosca-das-frutas e o zebrafish tão poderosos para a pesquisa biomédica.
Por que este inseto importa para a saúde humana
As larvas de Galleria mellonella imitam surpreendentemente bem como o corpo humano responde a microrganismos. Elas podem ser mantidas a 37 °C — a nossa temperatura corporal — e podem ser infectadas por uma ampla gama de bactérias e fungos de importância médica. Quando adoecem, seus corpos escurecem por um processo chamado melanização, fornecendo aos pesquisadores um indicador visível de saúde. Por serem invertebrados, evitam muitos dos obstáculos legais e éticos associados ao trabalho com vertebrados, além de serem baratos de criar em grande número. As larvas também foram encontradas capazes de degradar plásticos comuns, sugerindo usos em pesquisa ambiental.
O kit genético que faltava
Apesar dessas vantagens, as larvas da traça da cera careciam dos artifícios genéticos sofisticados disponíveis em animais clássicos de laboratório. Na última década, várias equipes decodificaram o genoma da traça e catalogaram seus genes e proteínas ativos, mas os pesquisadores ainda não podiam ligar ou desligar genes facilmente nem adicionar marcadores úteis. Essa lacuna limitava o que era possível com o modelo — por exemplo, criar animais que acendem quando infectados ou deletar genes específicos para testar como afetam a imunidade. O artigo atual enfrenta esse problema de frente, adaptando dois sistemas poderosos de engenharia genética, conhecidos como PiggyBac e CRISPR–Cas9, para uso em Galleria mellonella.
Construindo larvas repórter que brilham no escuro
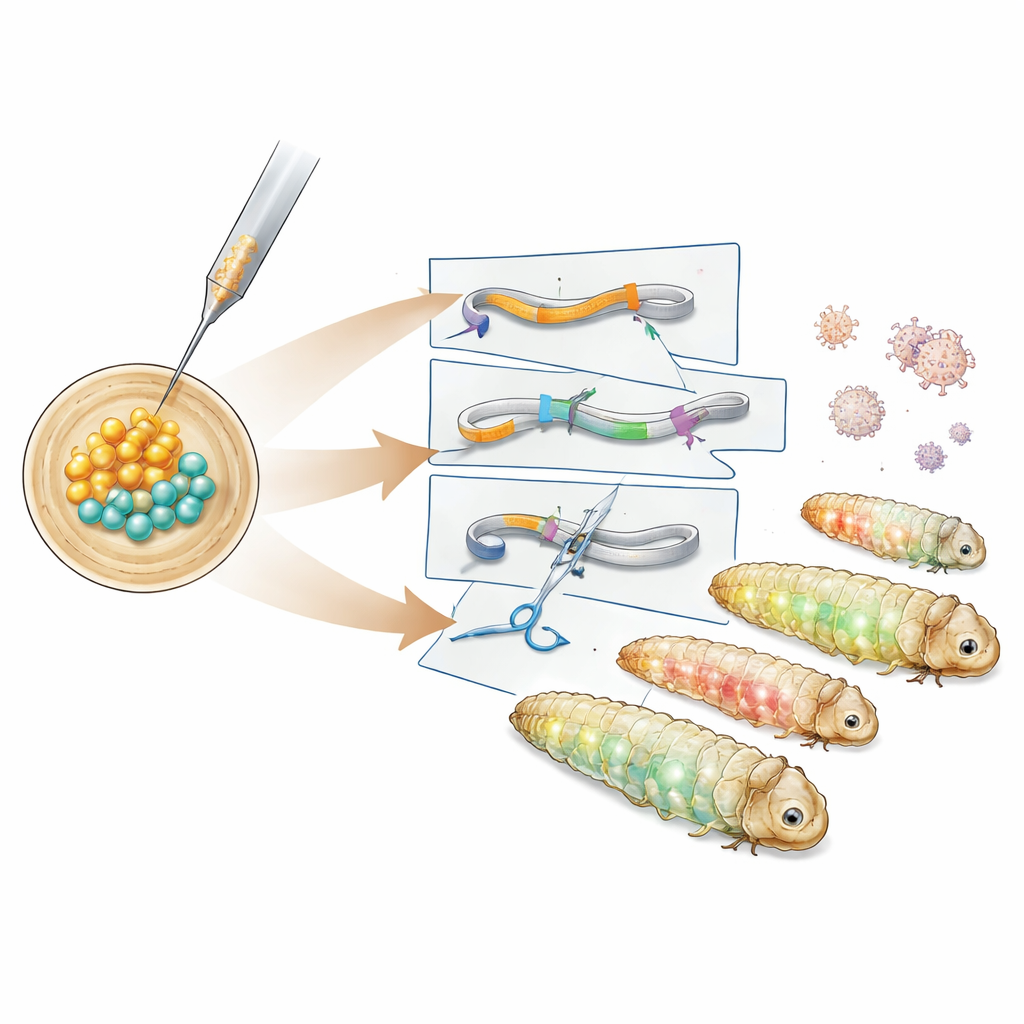
A equipe primeiro estudou o tempo do desenvolvimento embrionário inicial e identificou uma janela de aproximadamente seis horas após a postura dos ovos, quando todos os núcleos em divisão ainda compartilham um interior comum. Injetar DNA durante esse período permite que o material genético novo seja levado a todos os tecidos posteriores, incluindo futuros espermatozoides e óvulos. Usando essa janela, os pesquisadores introduziram construções de DNA baseadas no transposon PiggyBac, um elemento “cortar-e-colar” que insere grandes trechos de DNA no genoma. Após testar diferentes plasmídeos auxiliares, identificaram uma versão que carrega uma enzima PiggyBac hiperativa que produziu linhas transgênicas com sucesso. Essas larvas expressaram proteínas fluorescentes verdes e vermelhas em tecidos corporais distintos, e a análise de DNA mostrou que o cassete genético se alojou em um trecho inócuo entre genes nativos.
Observando células e anulando genes
Em seguida, os autores criaram linhas repórteres mais especializadas. Uma construção marcou uma proteína estrutural chamada tubulina com fluorescência verde para destacar o esqueleto interno da célula, enquanto outra fundiu um marcador vermelho a uma histona que envolve o DNA no núcleo. Essas linhas brilharam em padrões característicos pelo intestino, tecido adiposo, glândulas sericígenas e outros tecidos, permitindo aos pesquisadores visualizar estruturas celulares em larvas vivas ou fixadas. Para ir além de adicionar genes e realmente desativá‑los, a equipe recorreu ao CRISPR–Cas9. Eles injetaram complexos pré-montados de proteína–RNA do CRISPR visando o marcador fluorescente verde em embriões que já carregavam o cassete repórter. Muitos descendentes apresentaram perda parcial ou completa do sinal verde enquanto mantinham a fluorescência vermelha nos olhos, e o sequenciamento de DNA confirmou pequenas inserções e deleções no local de corte previsto pelo CRISPR.
Do avanço técnico ao impacto prático
Embora a eficiência tanto do PiggyBac quanto do CRISPR nessas traças ainda seja modesta em comparação com alguns outros insetos, os autores delineiam caminhos claros para melhoria por meio do ajuste de promotores, variantes enzimáticas e estratégias de injeção. Mesmo em sua forma atual, o kit de ferramentas é poderoso o suficiente para gerar linhas estáveis que visualizam componentes celulares-chave ou carregam knockouts gênicos direcionados. Para não especialistas, a visão geral é que Galleria mellonella agora pode ser manipulada quase tão flexivelmente quanto animais de laboratório mais conhecidos. Isso significa que pesquisadores podem criar lagartas que reportam infecções, modelam aspectos de doenças humanas ou testam novos medicamentos de maneiras mais rápidas, baratas e humanas, potencialmente reduzindo a dependência de modelos mamíferos em biologia de infecções e áreas relacionadas.
Citação: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Palavras-chave: Galleria mellonella, modelo de infecção invertebrado, engenharia genética, transgênese PiggyBac, knockouts por CRISPR