Clear Sky Science · pt
Formação multifásica aprimorada de nitrato e sulfato particulado impulsionada por NO2 em condições de alta umidade
Por que o ar úmido ainda pode estar poluído
Muitas pessoas imaginam que o clima úmido e enevoado ajuda a limpar o ar, lavando a poluição do céu. Mas no sul da China, o oposto frequentemente acontece: quando o ar oceânico quente e úmido encontra o ar continental mais frio, forma-se uma névoa densa mesmo que os processos atmosféricos tradicionais de limpeza estejam fracos. Este estudo explica o porquê, revelando como um poluente de tráfego comum, o dióxido de nitrogênio, alimenta de forma discreta a formação rápida de partículas finas nocivas quando o ar está muito úmido.
Ar pegajoso sobre uma cidade costeira
Os pesquisadores concentraram-se em Xiamen, uma cidade costeira no sul da China, durante duas semanas no início da primavera de 2024. Nessa época do ano, o ar oceânico quente e úmido frequentemente colide com ar continental mais frio e seco e fica estagnado, criando frentes meteorológicas quase estacionárias. Durante esses eventos de alta umidade, o ar se torna estagnado, as velocidades do vento caem e uma camada rasante de ar se instala sobre a cidade. Medições de uma estação de monitoramento no telhado mostraram que os níveis de partículas finas (PM2,5) aumentaram, a visibilidade piorou e o nevoeiro frequentemente se formou à medida que a umidade subia. Dentro desses períodos nebulosos, a composição química das partículas mudou em duas fases claras: primeiro o nitrato dominou, depois o sulfato cresceu rapidamente.
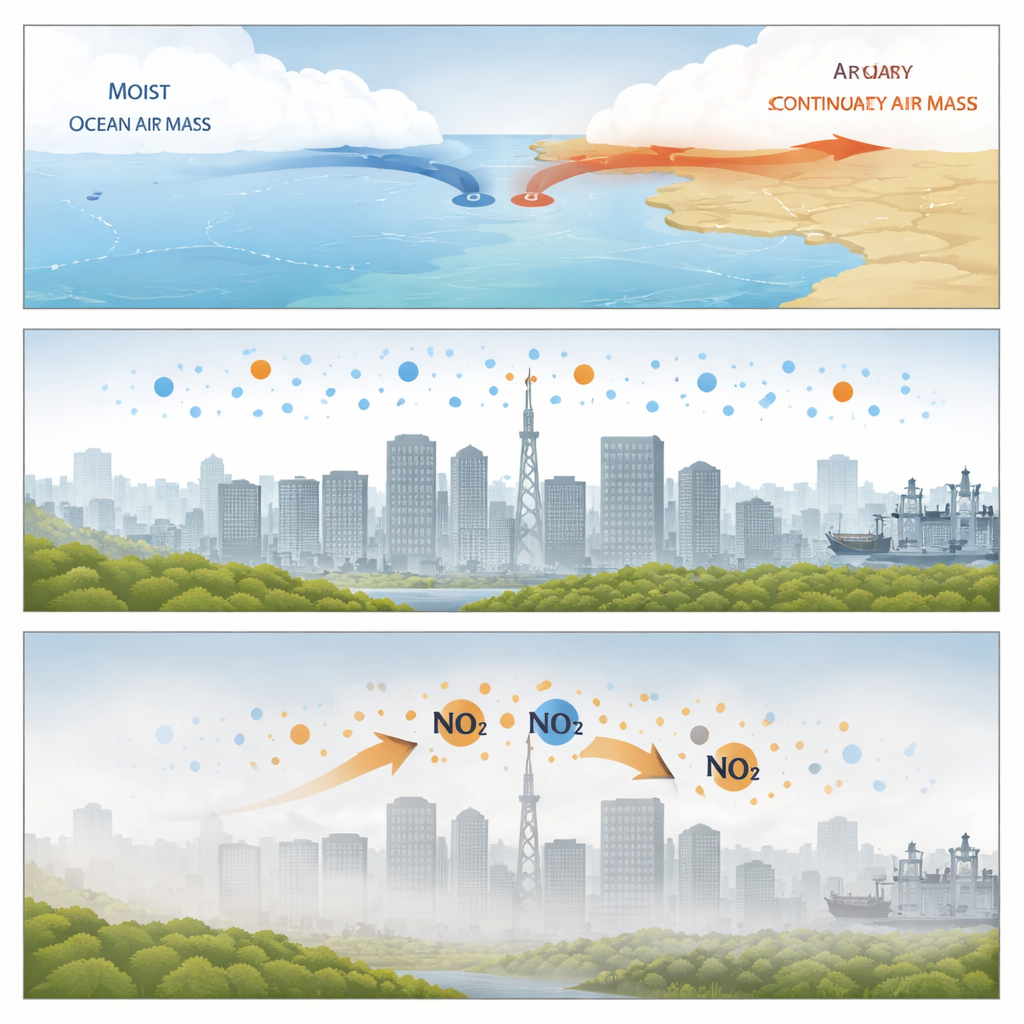
Duas fases de química oculta
Nas primeiras horas muito úmidas desses eventos, as partículas ficaram ricas em nitrato, embora a química usual induzida pela luz solar estivesse fraca e os níveis de ozônio baixos. A equipe constatou que a melhor explicação era que o dióxido de nitrogênio de fontes como o tráfego estava sendo absorvido diretamente pelas superfícies úmidas das partículas e por películas finas de água no solo. Nessas gotículas concentradas, o dióxido de nitrogênio reage mais rapidamente do que em água comum, produzindo tanto nitrato quanto outra forma reativa de nitrogênio que pode escapar de volta para o ar. A forte ligação entre dióxido de nitrogênio, água em aerossóis, área de superfície das partículas e aumento do nitrato sugeriu que esses processos de superfície dominavam a produção de nitrato durante a noite.
Quando o nevoeiro transforma nitrogênio em partículas de enxofre
À medida que a umidade aumentava ainda mais e o nevoeiro se formava, a química mudou. O sulfato, formado a partir do dióxido de enxofre, começou a crescer rapidamente e podia até superar o nitrato. Novamente o dióxido de nitrogênio desempenhou um papel central, mas de maneira diferente. Dentro de gotas de nevoeiro e gotas maiores, o dióxido de nitrogênio e seus produtos de reação oxidavam o enxofre dissolvido em uma série de reações aquosas. Um intermediário-chave, uma espécie reativa de nitrogênio que mantém um equilíbrio com o ácido nitroso, foi encontrado com tempo de permanência maior dentro de gotas maiores e menos ácidas do que em partículas minúsculas e mais ácidas. Esse tempo de residência mais longo permitiu que atacasse repetidamente o enxofre dissolvido, impulsionando a rápida produção de sulfato precisamente quando nevoeiro denso e névoa estavam presentes.
Colocando números no invisível
Para testar essas ideias, os autores construíram um “modelo caixa” computacional detalhado que combinou química em fase gasosa, reações em água líquida e trocas entre ar e partículas. Quando permitiram a captura de dióxido de nitrogênio por partículas úmidas e gotas de nevoeiro, o modelo reproduziu de perto os aumentos observados de nitrato e sulfato. Durante os eventos úmidos, a captura direta de dióxido de nitrogênio respondeu por quase metade de todo o nitrato formado, e os oxidantes à base de nitrogênio (dióxido de nitrogênio mais seus produtos aquosos) produziram quase dois terços do sulfato. À noite, a via do dióxido de nitrogênio superou amplamente a rota mais familiar envolvendo outro oxidante noturno, o pentóxido de dinitrogênio. O modelo também mostrou que gotas de nevoeiro, com seu tamanho maior e pH mais alto, são reatores especialmente favoráveis para a química nitrogênio–enxofre que gera sulfato.
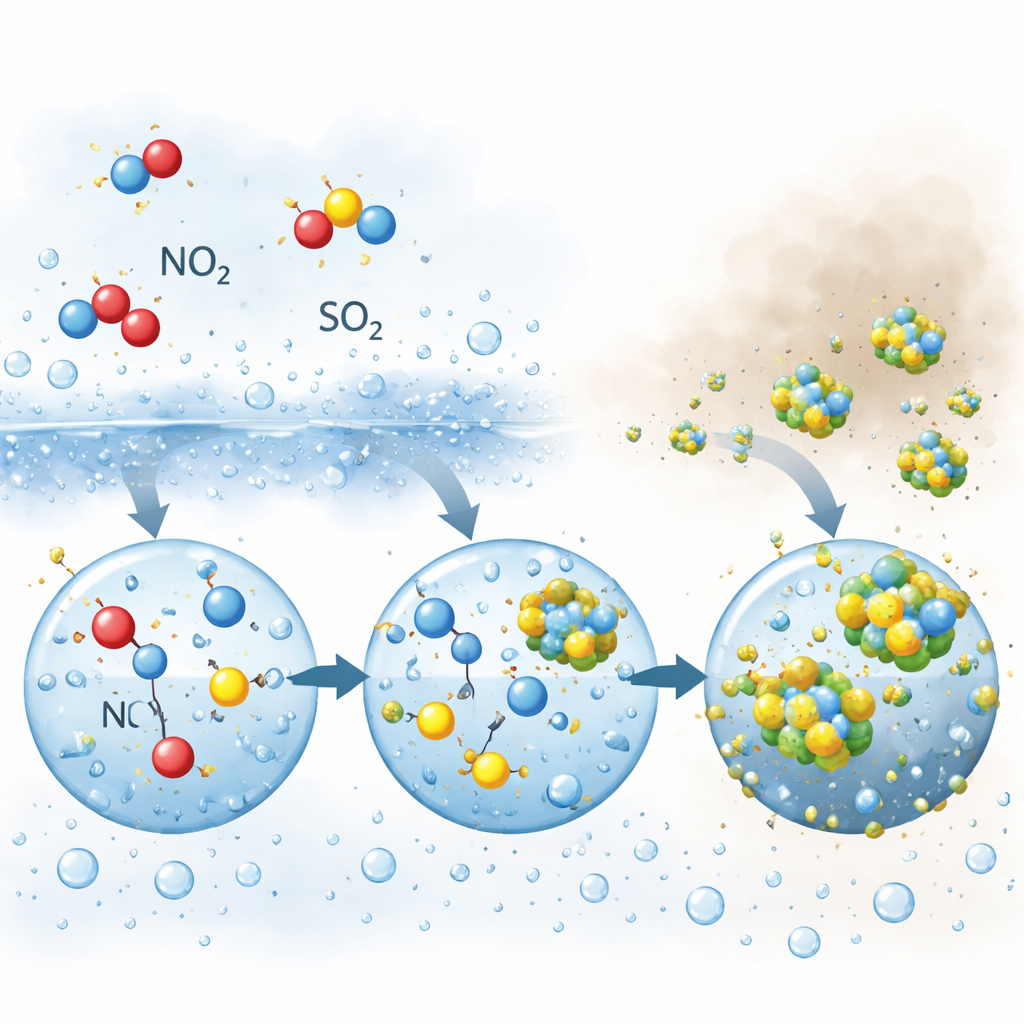
O que isso significa para um ar mais limpo
O estudo conclui que o dióxido de nitrogênio faz muito mais do que servir como um gás indicador da poluição do tráfego: sob condições muito úmidas e estagnadas, ele se torna um motor poderoso da formação de partículas finas. Ao acelerar a conversão de nitrogênio e enxofre gasosos em partículas de nitrato e sulfato, essas reações ocultas em água ajudam a explicar por que os níveis de partículas não caíram tão rapidamente quanto as emissões de gases de nitrogênio e enxofre na China. As descobertas sugerem que o controle eficaz da névoa fotoquímica em regiões costeiras e úmidas deve considerar não apenas quanto dióxido de nitrogênio é emitido, mas também com que frequência a atmosfera entra nesses estados pegajosos e enevoados que o transformam em uma fábrica química microscópica.
Citação: Lin, Z., Ji, X., Xu, L. et al. Enhanced NO2-driven multiphase formation of particulate nitrate and sulfate under high-humidity conditions. npj Clim Atmos Sci 9, 76 (2026). https://doi.org/10.1038/s41612-026-01352-5
Palavras-chave: poluição do ar, dióxido de nitrogênio, partículas finas, alta umidade, química do nevoeiro