Clear Sky Science · pt
Percepções estruturais e mecanísticas sobre o direcionamento dos integrinas α2β1 e α5β1 por vesículas extracelulares bioengenheiradas originárias de células de câncer de pulmão
Mensageiros Ocultos do Câncer
O câncer de pulmão frequentemente é detectado tardiamente, quando as opções de tratamento são limitadas. Uma abordagem promissora para combatê‑lo é entregar medicamentos apenas às células tumorais, poupando o tecido saudável. Este estudo explora um minúsculo sistema natural de transporte — vesículas extracelulares, ou VEs — que as próprias células cancerosas já usam para enviar mensagens. Ao reengenheirar essas vesículas com uma pequena etiqueta de direcionamento, os pesquisadores mostram como elas podem se ligar a alvos específicos nas células tumorais, estabelecendo as bases para terapias contra o câncer mais precisas e menos tóxicas.
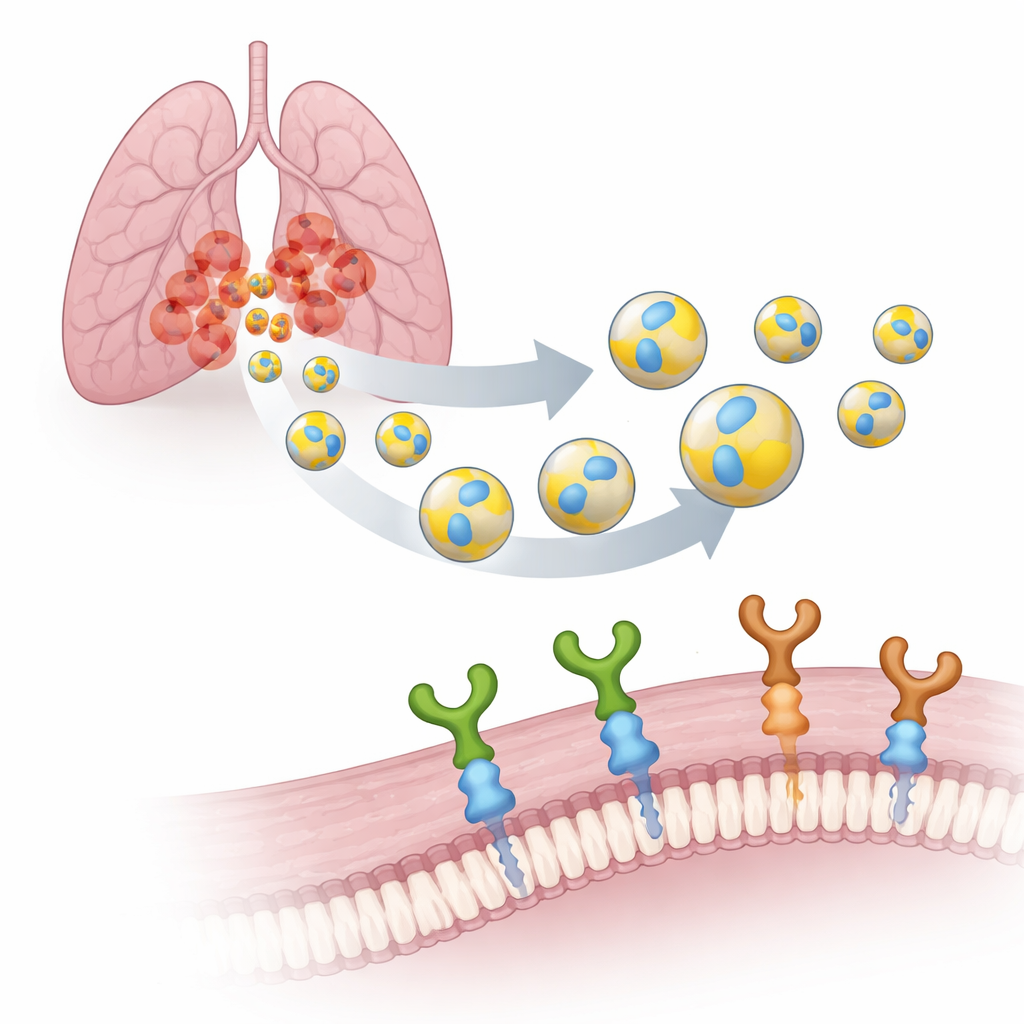
Transformando Pacotes Naturais em Mensageiros Inteligentes
Cada célula do nosso corpo libera VEs: bolsas em escala nanométrica envoltas por uma membrana, um pouco como bolhas de sabão microscópicas. Por serem produzidas por nossas próprias células, as VEs são biodegradáveis, atravessam barreiras biológicas com facilidade e têm menor probabilidade de provocar efeitos colaterais que transportadores sintéticos. A equipe se concentrou em VEs produzidas por células humanas de câncer de pulmão (A549) e decorou sua superfície com uma pequena etiqueta de sete blocos de construção chamada PTHTRWA. Experimentos anteriores mostraram que essa etiqueta direciona VEs para células de câncer de pulmão em camundongos, ligando‑se muito mais fortemente às células tumorais do que às células pulmonares normais, ao mesmo tempo em que apresenta toxicidade reduzida.
Encontrando os Portos de Ancoragem Certos nas Células Tumorais
Para transformar essas vesículas etiquetadas em ferramentas verdadeiramente direcionadas, os pesquisadores precisavam identificar quais “portos” nas células cancerosas elas reconhecem. Eles investigaram dois receptores de superfície relacionados, as integrinas α2β1 e α5β1. Essas são ganchos moleculares que ajudam as células a aderir ao seu entorno e a transmitir sinais para o interior. Em tumores pulmonares, α5β1 está fortemente associada a comportamento agressivo, disseminação e pior sobrevida, enquanto α2β1 tem sido ligada à resistência à quimioterapia. Utilizando uma técnica sensível chamada ressonância de plasmônica de superfície, a equipe comparou quão fortemente VEs decoradas com PTHTRWA se ligam a ambas as integrinas. Eles descobriram que vesículas sem a etiqueta mal interagiam, ao passo que VEs etiquetadas formavam complexos estáveis e apertados com ambos os receptores em condições próximas às fisiológicas.
Ampliando o Abraço Molecular
Para entender o que ocorre átomo a átomo quando a etiqueta encontra as integrinas, os pesquisadores recorreram a simulações computacionais. Construíram modelos tridimensionais da etiqueta ligada a regiões-chave das integrinas e deixaram esses sistemas evoluírem em água virtual por centenas de nanossegundos. Os cálculos mostraram que PTHTRWA se encaixa confortavelmente em um sulco raso no receptor α2β1, formando uma rede de ligações de hidrogênio e contatos hidrofóbicos que estabilizam o complexo. De forma crucial, a ligação favoreceu uma conformação mais “aberta” do receptor — sua forma de alta afinidade, pronta para sinalizar — em detrimento do estado “fechado” de repouso. Ao testar versões levemente modificadas da etiqueta, observaram que pequenas alterações químicas em uma extremidade podem remodelar sutilmente como o peptídeo se acomoda no sulco e quão fortemente ele prefere uma integrina em relação à outra.
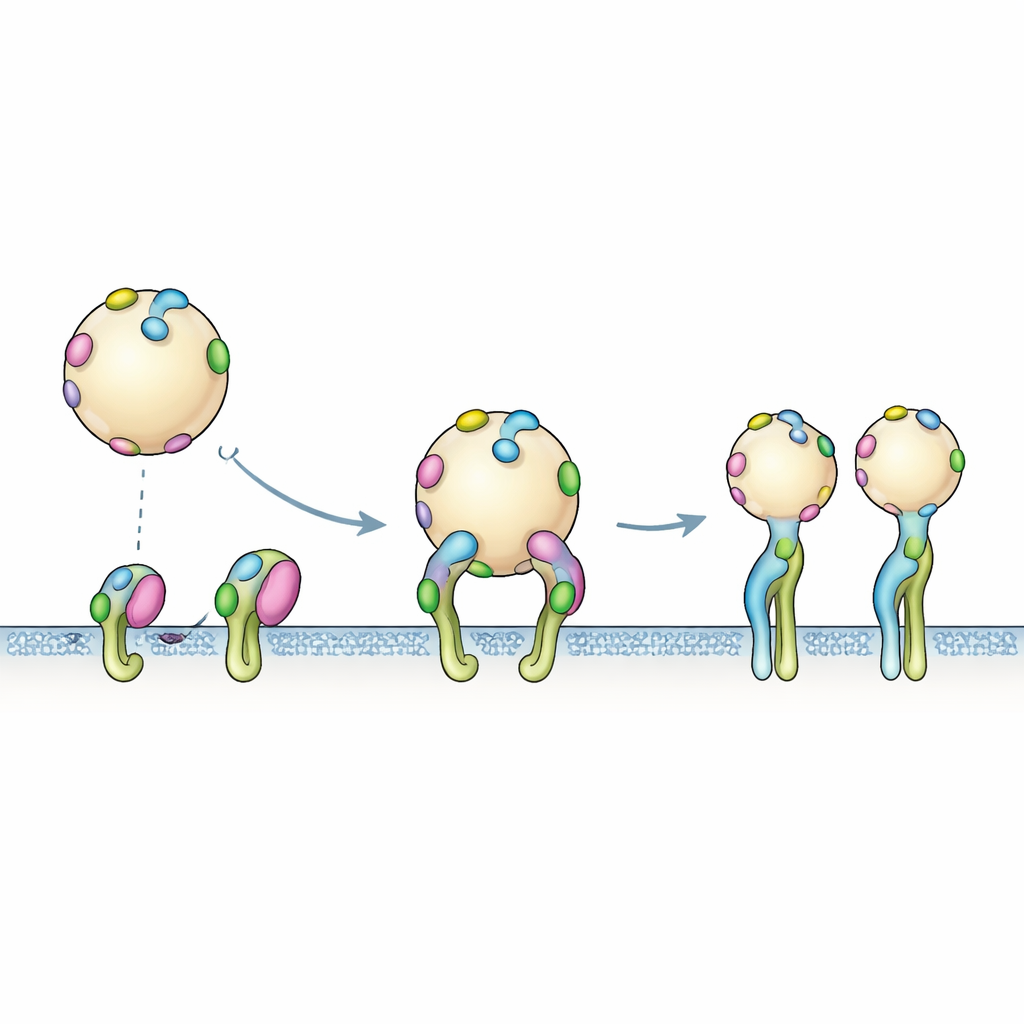
De Etiquetas Únicas a Agarres Multivalentes
Modelos computacionais capturam uma etiqueta tocando um receptor por vez, mas a superfície real das VEs ostenta muitas cópias de PTHTRWA. Os experimentos de ligação refletiram essa realidade multivalente: uma vez que uma vesícula etiquetada se aproxima de um aglomerado de integrinas, várias etiquetas podem se engajar simultaneamente. Os dados do sensor ajustaram‑se melhor a um processo em duas etapas. Primeiro, a vesícula anexa‑se brevemente por encontros rápidos e reversíveis. Em seguida, ocorre um rearranjo mais lento no qual as integrinas mudam para sua forma aberta e o aperto global se reforça. Esse fecho cooperativo, com muitas “mãos”, explica por que a força aparente de ligação de vesículas inteiras é maior do que a prevista a partir de uma única etiqueta isolada.
O Que Isso Pode Significar para Tratamentos Futuros
Em termos simples, o estudo demonstra que VEs armadas com a etiqueta PTHTRWA podem reconhecer seletivamente integrinas hiperativas no câncer de pulmão, e que fazem isso ao induzir esses receptores a uma forma aberta e fortemente ligada. Ao mapear essas interações em detalhe, os pesquisadores fornecem regras de projeto para a próxima geração de transportadores baseados em vesículas que poderiam entregar fármacos, agentes de imagem ou outras cargas diretamente às células malignas, ignorando em grande parte o tecido saudável. Embora mais trabalho em animais e humanos seja necessário, essa estratégia de direcionamento de integrinas aproxima a visão de uma medicina oncológica personalizada baseada em VEs de se tornar realidade.
Citação: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Palavras-chave: câncer de pulmão, vesículas extracelulares, integrinas, liberação direcionada de fármacos, simulações moleculares