Clear Sky Science · pt
Prova de conceito para extração de DNA livre de células do plasma baseada em sistema aquoso de duas fases para aplicações de biópsia líquida
Por que um exame de sangue importa para câncer e outras doenças
Muitos exames médicos modernos buscam fragmentos minúsculos de DNA que circulam livremente no sangue. Esses fragmentos, conhecidos como DNA livre de células, podem revelar se um tumor está liberando material genético, se um órgão transplantado está sendo rejeitado ou como está a evolução de uma gravidez. Mas, porque esses fragmentos são escassos, curtos e misturados com uma sopa de proteínas e outras moléculas, extraí‑los de forma limpa e rápida é surpreendentemente difícil. Este estudo apresenta uma nova forma mais simples de extrair esses fragmentos do plasma sanguíneo usando um método de separação à base de água e de baixa agressividade, possivelmente tornando testes avançados de “biópsia líquida” mais acessíveis e econômicos.
O desafio de pescar pedaços minúsculos de DNA
Médicos e pesquisadores usam biópsias líquidas para ler pistas genéticas a partir de uma simples coleta de sangue em vez de remover tecido. O problema é que o DNA livre de células no plasma normalmente existe em apenas algumas dezenas de nanogramas por mililitro e está fragmentado em pedaços curtos. Uma pequena fração desse material pode vir de um tumor ou de um órgão transplantado, então cada fragmento conta. Kits de extração padrão capturam DNA fazendo‑o aderir a superfícies de sílica na presença de sais fortes, seguidos por várias etapas de lavagem e centrifugação. Esses kits funcionam bem, mas demandam tempo, exigem equipamentos especiais e podem ser caros. Além disso, podem ter dificuldade para recuperar os fragmentos mais curtos e podem co‑extrair longos trechos de DNA genômico normal, que podem mascarar sinais raros relacionados a doenças.
Um truque de duas camadas de água para capturar DNA
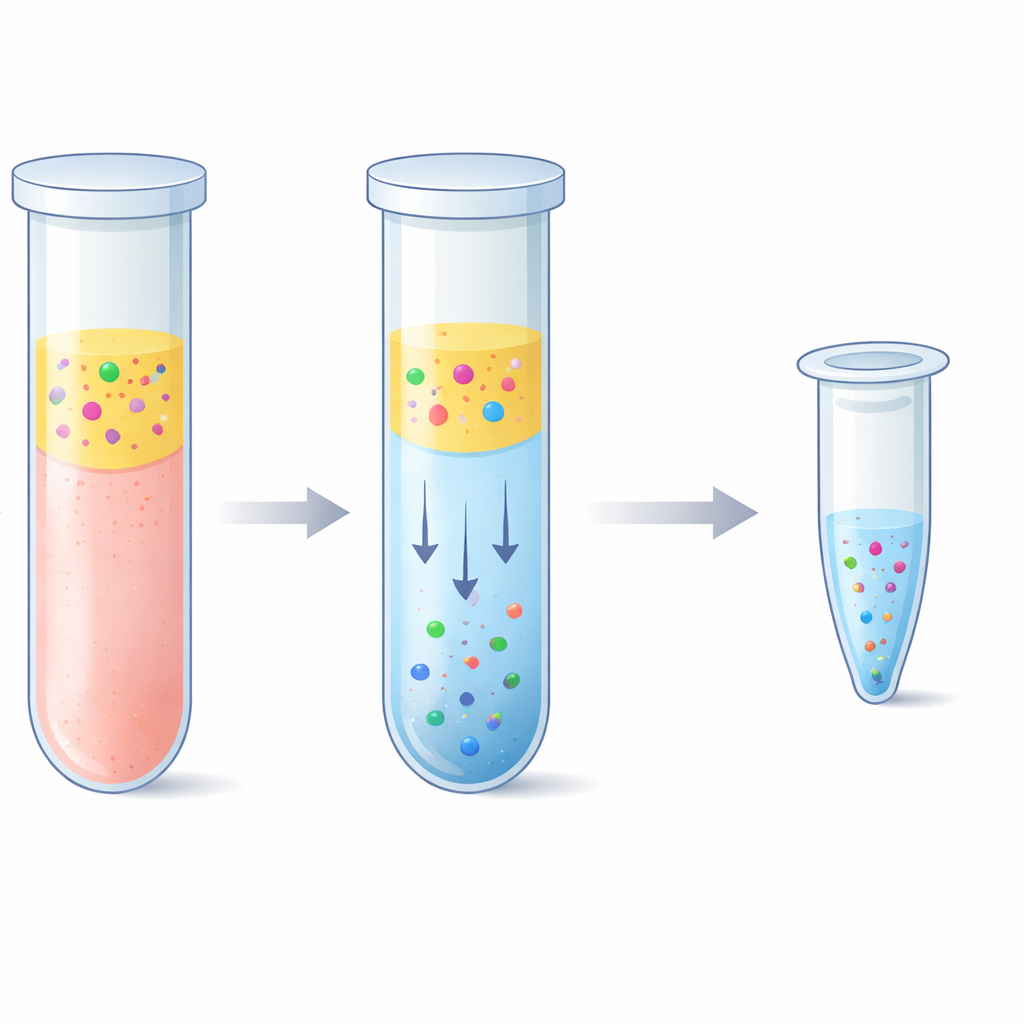
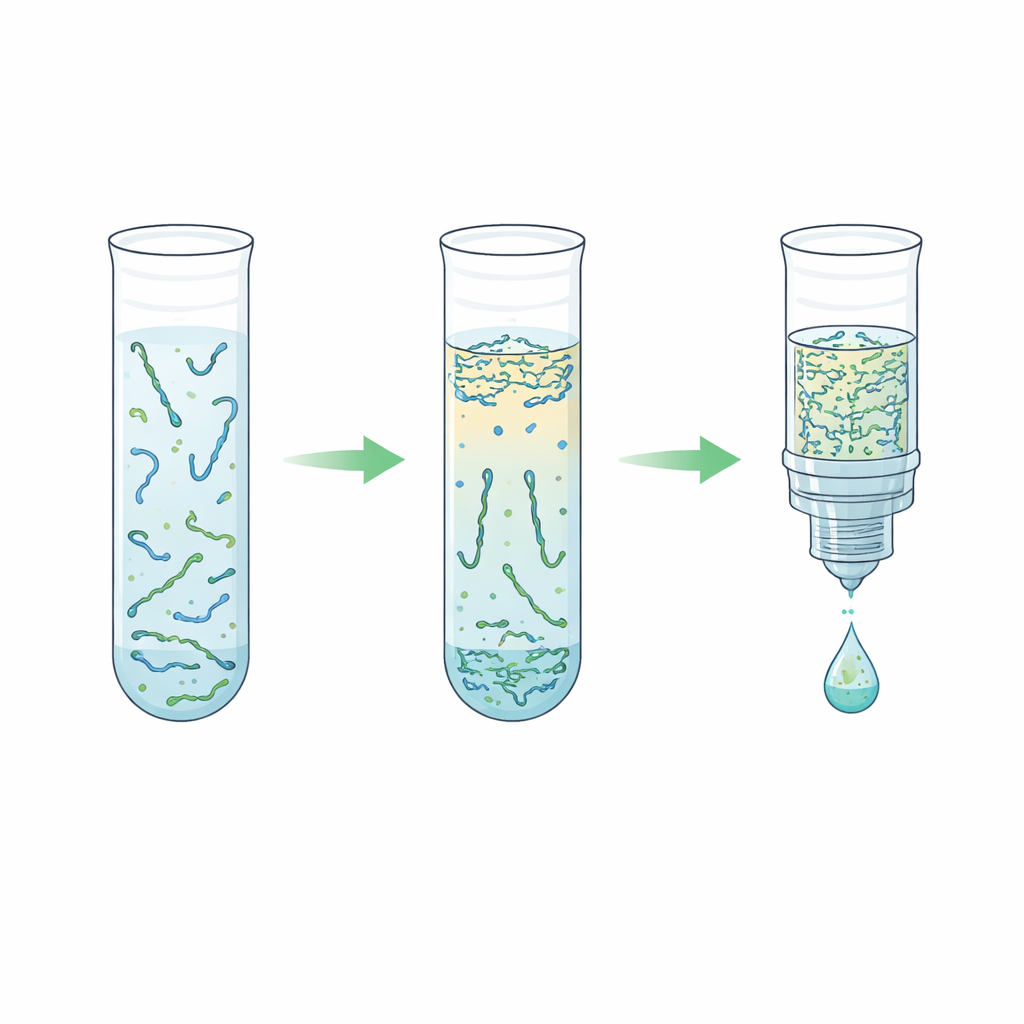
A equipe explorou uma alternativa baseada em um “sistema aquoso de duas fases” — em termos simples, dois líquidos ricos em água que não se misturam completamente, como óleo e vinagre, só que ambos feitos majoritariamente de água. Ao combinar o plasma com um polímero chamado polietilenoglicol e sais fosfato simples, a mistura se separou naturalmente em uma camada superior e outra inferior. Surpreendentemente, os fragmentos curtos de DNA preferiram fortemente a camada inferior rica em sal, enquanto a maioria das proteínas do sangue e as fitas longas de DNA permaneceram na camada superior ou na interface. Os pesquisadores ajustaram cuidadosamente a receita para que essa camada inferior permanecesse pequena o suficiente para concentrar o DNA, mas suave o bastante para não danificá‑lo. Em seguida, combinaram essa etapa com uma purificação por “elução reversa”, que empurra a camada inferior salgada através de uma matriz porosa para remover o sal e reduzir o volume final, resultando em uma solução de DNA mais limpa e concentrada.
Aprimorando o processo para uso no mundo real
Por meio de muitas rodadas de testes, os autores ajustaram o equilíbrio entre polímero e sal, velocidades de centrifugação, volumes e etapas opcionais de lise que rompem complexos proteína–DNA. Eles descobriram que aumentar o teor de polímero ao longo de certas linhas de composição duplicou a concentração de DNA sem prejudicar a recuperação, e que um condicionamento mais vigoroso na etapa de elução reversa aumentou a concentração em cerca de quatro vezes em comparação com trabalhos anteriores. Surpreendentemente, verificaram que pular a lise agressiva antes da separação em duas camadas frequentemente funcionava melhor; a lise tendia a perturbar as fases e reduzir o rendimento. Um fluxo de trabalho simplificado, em grande parte sem lise, removeu cerca de 99,7% das proteínas do plasma enquanto recuperava até aproximadamente dois terços do DNA curto de entrada em um volume quatro vezes menor, tudo em cerca de dez minutos de processamento total e apenas alguns minutos de trabalho manual.
Como o novo método se compara
Os pesquisadores compararam sua abordagem com um kit comercial de sílica amplamente usado. O kit padrão produziu rendimentos totais de DNA um pouco mais altos e maior concentração porque eluía em volumes muito pequenos. No entanto, o método de duas fases mostrou recuperações consistentes acima de 60% em uma variedade de entradas de DNA, mesmo começando com quantidades muito pequenas, e exigiu bem menos etapas manuais e menos equipamentos. Importante, o novo processo atuou como um filtro embutido para o tamanho dos fragmentos: enriqueceu DNA curto, semelhante ao DNA livre de células, enquanto excluía em grande parte as fitas longas que podem vir de células sanguíneas rompidas. Testes usando PCR quantitativa mostraram que os extratos limpos não inibiram a amplificação posterior. Quando a equipe usou uma amostra de referência comercial contendo mutações relacionadas ao câncer conhecidas, o DNA recuperado com seu método pôde ser convertido em bibliotecas de sequenciamento, rodado em um sequenciador de alto rendimento e usado para detectar todas as variantes esperadas nas frequências corretas.
O que isso pode significar para futuros exames de sangue
Em termos simples, este trabalho mostra que uma separação relativamente simples à base de água pode substituir uma química mais complexa de superfície sólida para preparar DNA livre de células a partir do plasma. Embora o novo método atualmente renda ligeiramente menos DNA do que kits comerciais de ponta, ele oferece processamento rápido, forte remoção de proteínas indesejadas e DNA longo, e compatibilidade pronta com PCR e sequenciamento de nova geração. Se for validado adicionalmente em amostras de pacientes reais e refinado para automação, essa abordagem poderia reduzir custos e simplificar fluxos de trabalho laboratoriais, ajudando a levar testes sanguíneos precisos baseados em genética para câncer, transplante e outras condições a um uso mais amplo e cotidiano.
Citação: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
Palavras-chave: biópsia líquida, DNA livre de células, teste sanguíneo para câncer, extração de DNA, sequenciamento de nova geração