Clear Sky Science · pt
Interferon-β e FTY720 melhoram a inflamação progressiva do SNC via sinalização de astrócitos associada à SOCS1
Por que esta pesquisa importa para pessoas com esclerose múltipla
Para muitas pessoas com esclerose múltipla (EM), o maior temor não são as recaídas iniciais, e sim a perda lenta e contínua de função que pode ocorrer depois. Nessa fase tardia e progressiva, o dano dentro do cérebro e da medula espinhal continua mesmo quando medicamentos padrão que atuam sobre o sistema imunológico no sangue estão conseguindo seu efeito. Este estudo explora uma forma de alcançar essa inflamação “oculta” ao combinar um comprimido já usado na EM com uma forma de medicamento de longa data administrada diretamente em direção ao cérebro.
Uma doença cerebral de longo prazo com poucas opções
A EM é uma doença autoimune em que as próprias células de defesa do corpo atacam o revestimento dos axônios, levando a problemas de visão, fraqueza e outros sintomas neurológicos. No início, os sintomas tendem a surgir e regredir. Com o tempo, muitos pacientes entram em uma fase progressiva marcada por deficiência gradual e muitas vezes irreversível. Durante esse estágio, a barreira hematoencefálica torna-se mais difícil de ser atravessada por medicamentos, e a atividade prejudicial de células residentes do cérebro chamadas glia — especialmente astrócitos e microglia — passa a ter um papel maior. Os tratamentos atuais, que atuam principalmente bloqueando células imunes no sangue, oferecem ajuda limitada uma vez que esse estágio está estabelecido.
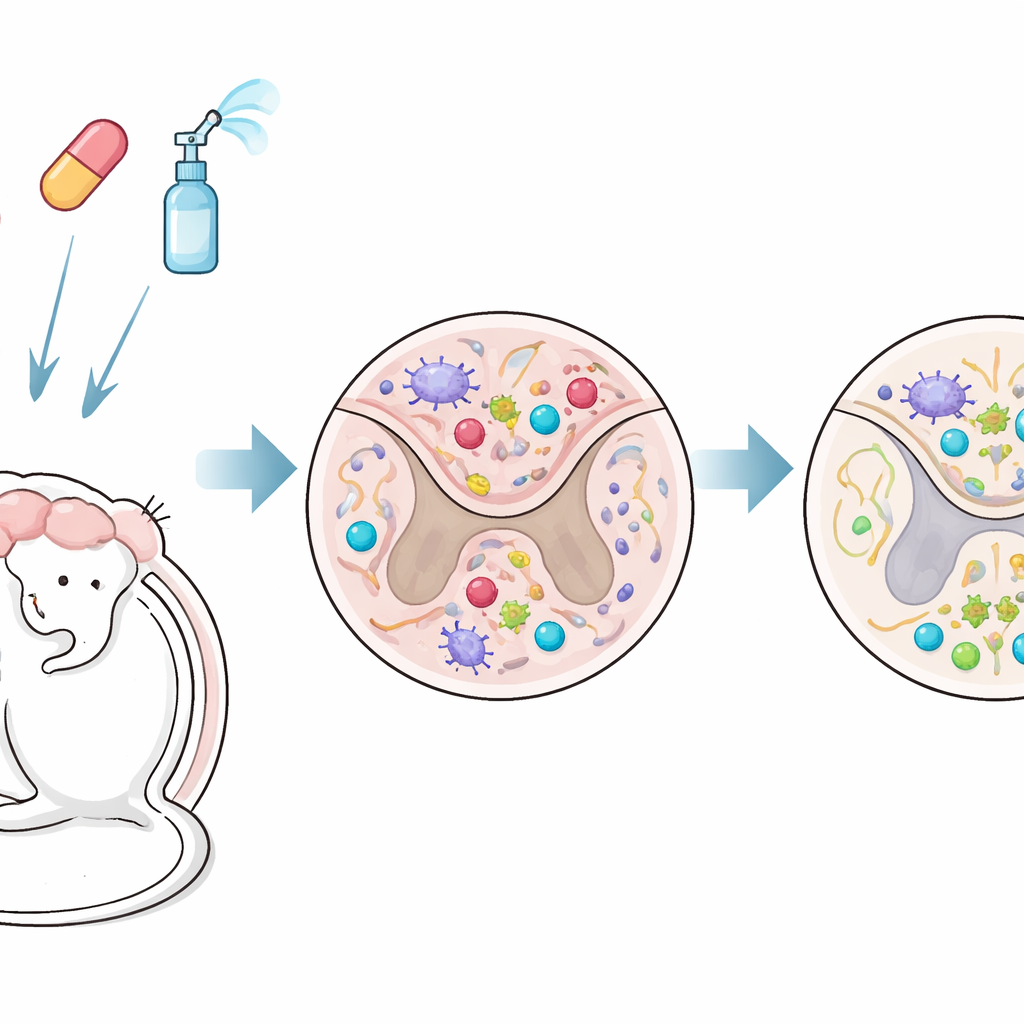
Combinar dois medicamentos para atingir sangue e cérebro
Os pesquisadores testaram um tratamento combinado em um modelo murino que reproduz de perto a EM progressiva. Um dos fármacos, o fingolimode (FTY720), é um comprimido que aprisiona células imunes nos linfonodos e também pode entrar no cérebro. O outro, interferon‑beta, é uma terapia antiga para EM que normalmente atua fora do cérebro porque não atravessa facilmente a barreira hematoencefálica. Neste estudo, o interferon‑beta foi administrado por via intranasal — através do nariz — para que pudesse contornar essa barreira e alcançar o sistema nervoso central de forma mais direta. O tratamento começou depois que os camundongos já haviam desenvolvido problemas neurológicos crônicos, refletindo um estágio em que o dano costuma ser mais difícil de reverter.
Menos dano e atividade imune mais calma
Os camundongos que receberam a combinação de fingolimode mais interferon‑beta intranasal se saíram melhor do que aqueles tratados apenas com fingolimode. Seus escores de doença melhoraram mais, e alguns déficits neurológicos existentes diminuíram. Ao examinar as medulas espinais, os cientistas encontraram mais mielina preservada, menos sinais de lesão axonal e menos células imunes infiltradas. Células T pró‑inflamatórias e monócitos foram reduzidos, e as T restantes produziram menos das moléculas mensageiras danosas interferon‑gama e IL‑17. Importante, a terapia combinada também atenuou sinais prejudiciais vindos de astrócitos e microglia, as células gliais que ajudam a moldar o ambiente local dentro do cérebro e da medula espinhal.
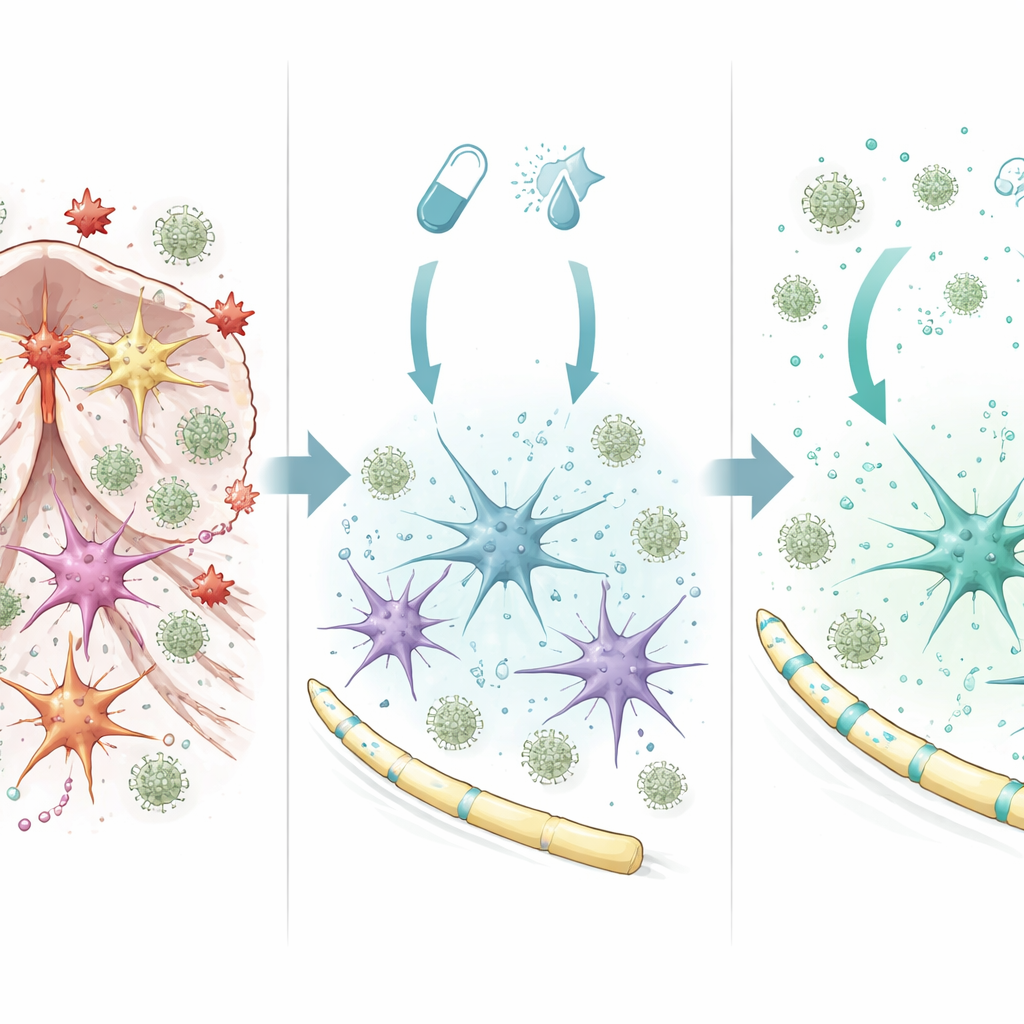
Astrócitos mudam de comportamento nocivo para protetor
Para entender como o tratamento combinado atua dentro do cérebro, a equipe estudou astrócitos purificados em cultura. Quando expostos a fingolimode mais interferon‑beta, os astrócitos ativaram um amplo conjunto de genes ligados à sobrevivência celular, redução da inflamação e manutenção saudável da bainha de mielina. Um componente-chave foi um regulador chamado SOCS1, que age como um freio na sinalização inflamatória. Bloquear a SOCS1 nos astrócitos apagou grande parte do padrão gênico protetor e levou essas células a liberar mais fatores inflamatórios que atraíam células imunes. Em contraste, quando a SOCS1 estava ativa, os astrócitos produziram mais sinais de crescimento e reparo e liberaram uma mistura de moléculas que reduziram a migração de monócitos inflamatórios. Mudanças protetoras semelhantes foram observadas em linhagens celulares humanas de astrócitos e microglia tratadas com a combinação de medicamentos, sugerindo que o mecanismo é relevante além dos camundongos.
O que isso pode significar para futuras terapias da EM
Este estudo mostra que combinar fingolimode com interferon‑beta administrado pelo nariz pode fazer mais do que bloquear células imunes no sangue. Também pode reprogramar astrócitos dentro do sistema nervoso central para um estado mais calmo e protetor, com a SOCS1 atuando como um nó central de controle. Embora o trabalho tenha sido feito em camundongos e em culturas celulares, e o interferon‑beta sozinho não tenha sido testado lado a lado em todos os experimentos, os resultados apontam para uma estratégia promissora: mirar simultaneamente o sistema imune periférico e as próprias células de suporte do cérebro. Se efeitos semelhantes puderem ser alcançados e comprovados seguros em humanos, abordagens combinadas com foco no cérebro podem ajudar a retardar ou parcialmente reverter o dano silencioso que impulsiona a EM progressiva.
Citação: Tsaktanis, T., Beyer, T., Nirschl, L. et al. Interferon-β and FTY720 ameliorate progressive CNS inflammation via SOCS1-associated astrocyte signaling. Sci Rep 16, 9851 (2026). https://doi.org/10.1038/s41598-026-45303-9
Palavras-chave: esclerose múltipla progressiva, fingolimode, interferon beta, astrócitos, neuroinflamação