Clear Sky Science · pt
Investigando as interações da proteína de imunidade Colicin E9 de Escherichia coli com a DNA girase de Pseudomonas aeruginosa: abordagem computacional avançada para desenvolver novas estratégias antimicrobianas
Transformando armas bacterianas em novos medicamentos
À medida que a resistência a antibióticos se espalha, os médicos ficam sem recursos para conter infecções perigosas. Alguns dos agentes mais persistentes, como Pseudomonas aeruginosa, conseguem resistir a muitos fármacos. Este estudo busca inspiração nas próprias bactérias, explorando como a proteína protetora de um microrganismo poderia ser reaproveitada para desativar uma enzima vital em outro microrganismo. Usando simulações computacionais avançadas, os pesquisadores mostram como uma pequena proteína de “imunidade” pode se ligar fortemente a uma enzima bacteriana chave, sugerindo uma nova via para futuros antimicrobianos.
Um pequeno escudo contra uma toxina letal
Certas linhagens de Escherichia coli produzem proteínas-tóxicas potentes chamadas colicinas, que podem matar bactérias vizinhas. Para evitar se envenenar, essas bactérias também fabricam proteínas de imunidade correspondentes. Uma dessas protetoras, conhecida como proteína de imunidade da Colicin E9 (frequentemente chamada Im9), prende-se ao domínio cortante da toxina e impede que ela danifique o DNA da bactéria hospedeira. Como essa parceria é tão específica e forte, os cientistas há muito suspeitam que entendê-la em detalhe poderia revelar novas maneiras de controlar bactérias nocivas. Neste trabalho, os autores investigam se a Im9 também poderia se ligar à DNA girase, uma enzima essencial em Pseudomonas aeruginosa que gerencia como seu DNA é enrolado e replicado.
Alvejar uma enzima vulnerável em um microrganismo de difícil tratamento
Pseudomonas aeruginosa é um importante patógeno hospitalar, capaz de sobreviver em ambientes adversos e resistente a muitos medicamentos. A DNA girase é uma de suas enzimas mais importantes, responsável por manter as longas fitas de DNA da bactéria adequadamente torcidas para que possam ser replicadas. Como bloquear essa enzima pode interromper o crescimento bacteriano, ela já é um alvo comprovado de alguns antibióticos. Os autores usaram uma ferramenta de aprendizado profundo para analisar a estrutura tridimensional da DNA girase de Pseudomonas e identificar prováveis “pontos quentes” — aglomerados de aminoácidos na superfície que são mais importantes para a ligação de parceiros. Essas regiões formam o bolso ativo da enzima, onde ocorre o processamento normal do DNA e onde um inibidor potencial idealmente se prenderia.
Simulando um aperto molecular
Para verificar se a Im9 poderia segurar esses pontos quentes, os pesquisadores recorreram a programas de docking molecular que virtualmente “encaixam” proteínas como quebra-cabeças 3D. Primeiro, eles limparam e completaram as estruturas disponíveis de Im9 e da DNA girase, reparando um loop ausente na enzima e executando simulações curtas para aliviar regiões tensionadas. Em seguida, usaram duas ferramentas de docking complementares, ClusPro e LightDock, para gerar muitos complexos candidatos. A partir desses, selecionaram os arranjos mais promissores e os submeteram a longas simulações de dinâmica molecular, abrangendo centenas de nanossegundos. Esses filmes temporais permitiram observar como as duas proteínas se ajustavam, flexionavam e se assentavam em formas mais estáveis quando ligadas.
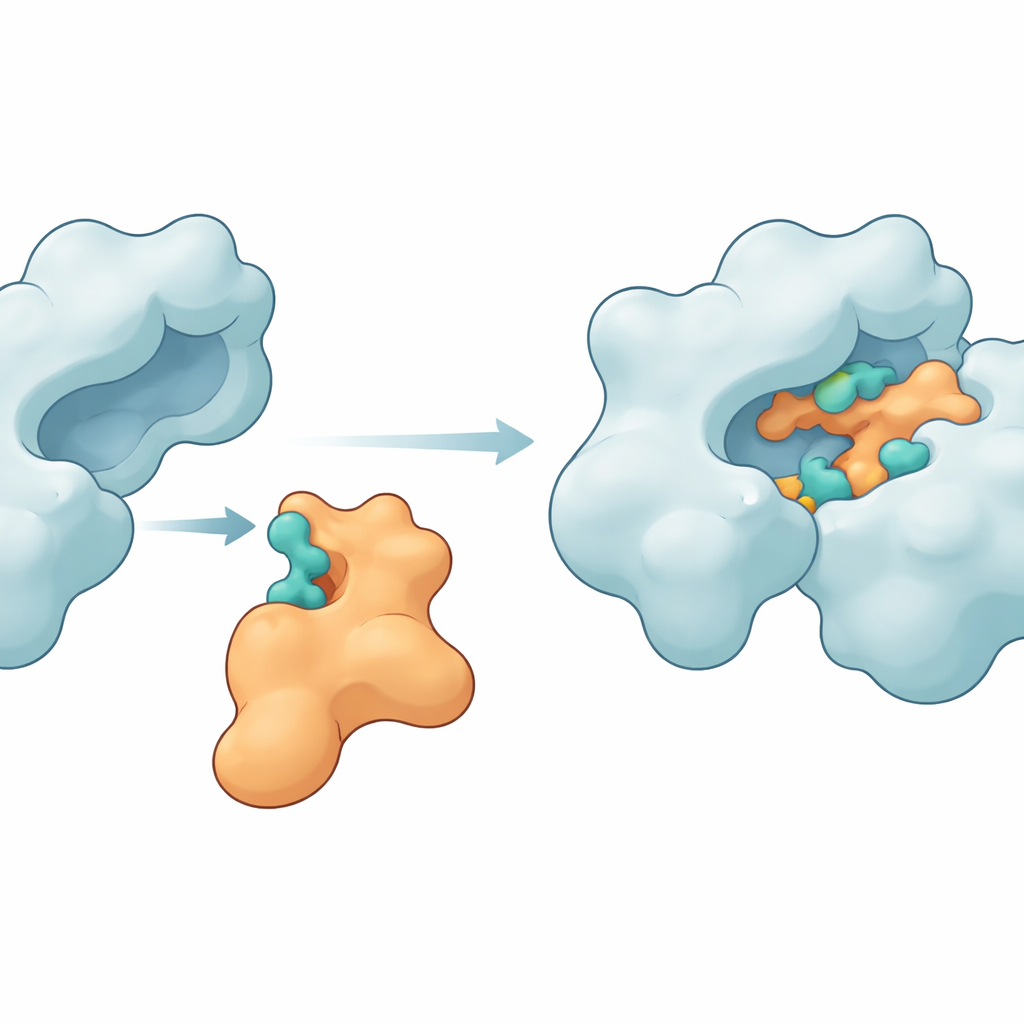
Pontos de contato chave que mantêm as proteínas unidas
As simulações revelaram que a Im9 pode, de fato, formar um complexo firme e persistente com a DNA girase. Vários aminoácidos na enzima — como MET27, ASP47, LYS105, LEU198, ASN199, ARG191 e GLU194 — formaram repetidamente ligações de hidrogênio e outras forças atrativas com sítios correspondentes na Im9. Em um modelo principal, os dois parceiros mantiveram entre seis e dez ligações de hidrogênio durante a maior parte da simulação, sinal de uma interface forte e bem organizada. Outras medidas estruturais, incluindo quão compactas permaneceram as proteínas e quanto suas formas flutuaram, mostraram que a enzima se manteve íntegra enquanto a proteína de imunidade flexionou o suficiente para moldar-se à superfície da girase. Cálculos de energia usando o método MM-GBSA apoiaram ainda a ideia de que esses contatos criam uma energia livre de ligação favorável, embora modesta, dominada por contribuições eletrostáticas e de van der Waals.
Dos modelos computacionais aos futuros antimicrobianos
Em conjunto, os resultados sugerem que a proteína de imunidade da Colicin E9 pode se ligar de forma estável à região ativa da DNA girase de Pseudomonas, formando um complexo de longa duração que poderia, em princípio, bloquear o papel normal da enzima no processamento do DNA. Embora essas descobertas se baseiem inteiramente em modelos computacionais e ainda requeiram testes experimentais, elas fornecem um roteiro detalhado de onde e como um inibidor à base de proteína poderia se fixar. Para não especialistas, a mensagem principal é que as próprias armas e escudos bacterianos da natureza podem inspirar novas estratégias contra infecções de difícil tratamento. Ao entender esse aperto microscópico em nível atômico, os cientistas avançam um passo na direção de projetar novos antimicrobianos que interrompam enzimas bacterianas cruciais sem prejudicar as células humanas.
Citação: Alfaraj, R., Alkathiri, F. & Chikhale, R. Investigating Escherichia coli Colicin E9 immunity protein interactions with DNA gyrase of Pseudomonas aeruginosa: advanced computational approach for developing novel antimicrobial strategies. Sci Rep 16, 10786 (2026). https://doi.org/10.1038/s41598-026-44427-2
Palavras-chave: resistência a antibióticos, DNA girase, interações proteína–proteína, projeto de fármacos computacional, Pseudomonas aeruginosa