Clear Sky Science · pt
Dados cristalográficos da dolicilfosfato manose sintetase de Pyrococcus furiosus sugerem que a enzima pode transpor seu produto glicolipídico
Como micróbios termófilos mantêm suas capas celulares em forma
Muitos micróbios que prosperam em ambientes extremamente quentes sobrevivem graças a uma capa protetora de açúcares na superfície celular. Construir essa capa requer moléculas especiais de gordura–açúcar que precisam ser produzidas de um lado da membrana celular e então movidas para o outro. Este estudo analisa uma enzima que sintetiza uma dessas moléculas em um microbio termófilo e sugere que, notavelmente, a mesma proteína pode também ajudar a transpor seu produto através da membrana — desempenhando duas funções ao mesmo tempo.
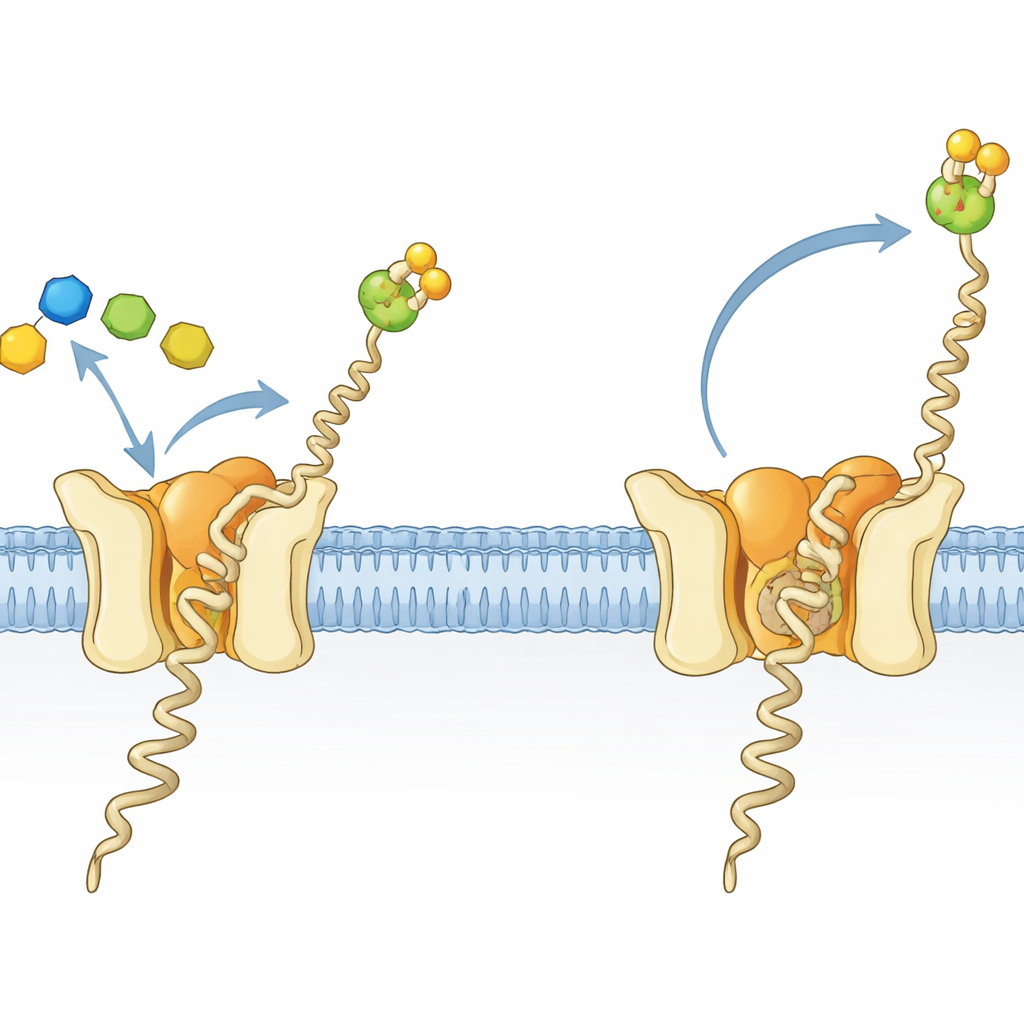
Uma fábrica minúscula para uma molécula crucial de açúcar–gordura
Células em todos os domínios da vida decoram muitas proteínas com cadeias de açúcares, um processo essencial para dobramento adequado, estabilidade e comunicação entre células. Em arqueias e eucariotos, um bloco de construção chave para essas decorações é uma molécula açúcar–gordura chamada dolicilfosfato manose (Dol-P-Man). Ela consiste em uma longa cauda oleosa ancorada na membrana e uma cabeça açúcar–fosfato que se projeta para o meio aquoso. O Dol-P-Man é sintetizado pela enzima dolicilfosfato manose sintetase (DPMS), que transfere uma manose de um doador solúvel para um lipídio ligado à membrana. No arqueão hipertermofílico Pyrococcus furiosus, a DPMS é uma proteína de cadeia única, denominada DPMS tipo III, com uma região catalítica solúvel ligada a uma seção transmembrana composta por quatro hélices cujo papel não era claro.
Capturando a enzima em ação
Os pesquisadores cristalizaram a DPMS de P. furiosus juntamente com seus substratos e acompanharam a reação por cristalografia de raios X. Sua nova estrutura, combinada com três anteriores, captura uma série de instantâneos em torno do momento em que o açúcar é transferido. Em um estado, a molécula doadora (GDP-manose) e um aceitador do tipo Dol-P estão ligados em uma geometria precisa que posiciona o carbono reativo da manose diretamente em frente ao grupo fosfato do Dol-P — um arranjo “pré-transferência” ideal. Loops na enzima atuam como portas dianteira e traseira: eles se fecham para manter o doador e o íon metálico no lugar, e então se reorganizam para abrir um caminho para o Dol-P entrar e para o GDP gasto sair depois que o açúcar foi transferido. Esses detalhes esclarecem como a enzima assegura uma transferência de açúcar eficiente e precisa na superfície da membrana.
Um produto de cabeça para baixo oculto na membrana
Mais surpreendente foi um segundo estado distinto observado nos mesmos cristais. Aqui, a molécula final Dol-P-Man não está no sítio ativo, mas alojada mais profundamente na porção transmembrana da proteína, em uma orientação “de cabeça para baixo”. Sua cabeça açúcar–fosfato repousa em um bolso polar entre dois pares de hélices (TMD1 e TMD2), enquanto a cauda oleosa percorre um sulco formado pelas hélices. Um aminoácido chave, uma fenilalanina, parece atuar como uma comporta que pode bloquear ou abrir o acesso a esse bolso. A qualidade da densidade eletrônica e a maneira como a proteína se empacota no cristal indicam que esse Dol-P-Man invertido não é um artefato de contatos cristalográficos, mas um estado genuíno e bem povoado que a enzima pode adotar.
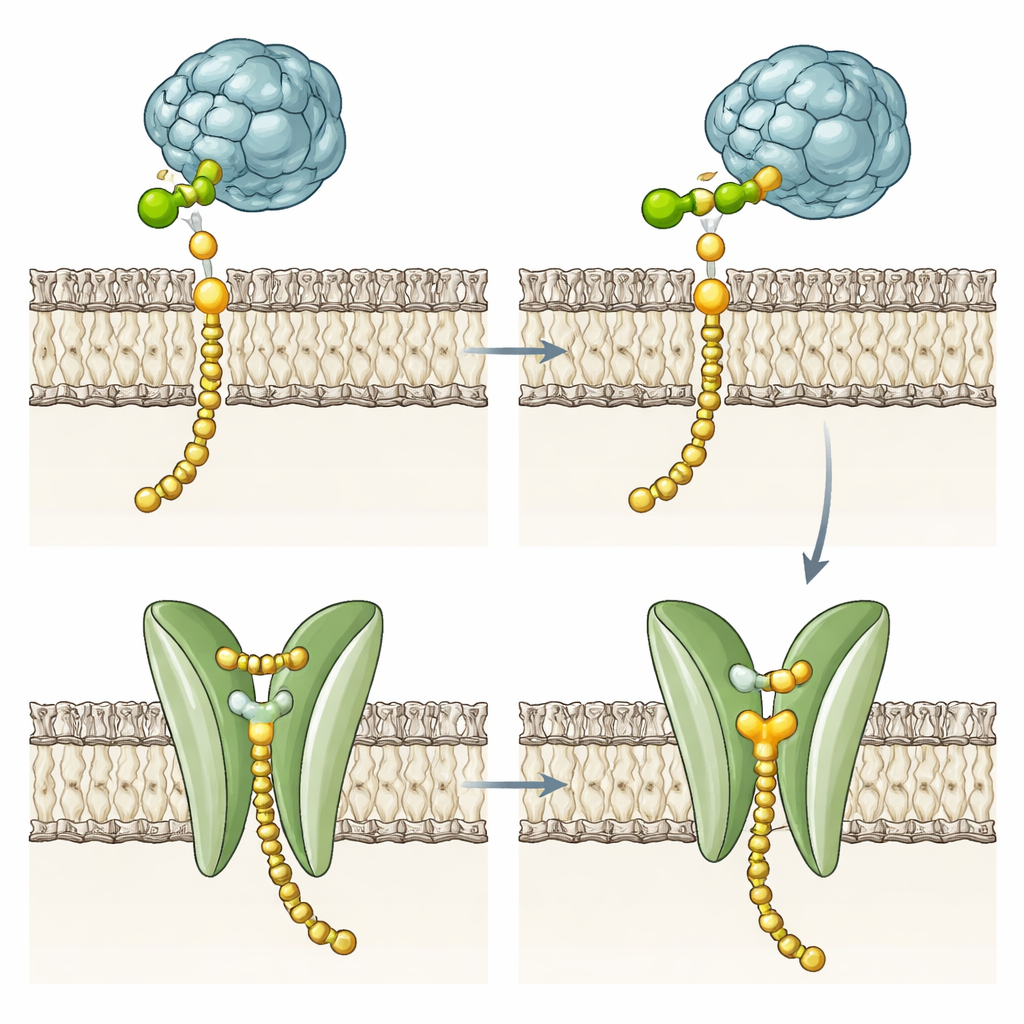
Enzimas mutantes sugerem um segundo trabalho
Para testar se o domínio transmembrana é necessário para a química da transferência de açúcar, a equipe construiu múltiplas variantes. Eles deletaram a maior parte ou todas as hélices, as trocaram por um segmento transmembrana diferente da DPMS de levedura, ou alteraram resíduos chave do bolso e a fenilalanina comporta. Notavelmente, esses mutantes ainda produziram Dol-P-Man em taxas semelhantes às da enzima intacta, embora alguns fossem ligeiramente menos estáveis na membrana. Isso mostra que a química central reside na região catalítica solúvel e que o feixe de quatro hélices não é necessário para acoplar a manose ao Dol-P. Em vez disso, seu bolso polar conservado, sulco e resíduo de comporta sugerem um papel especializado no manuseio do produto final, especialmente em arqueias hipertermofílicas cujas membranas rígidas tornam energeticamente custosa a transposição espontânea de lipídios.
Por que uma enzima com dupla função importa
Ao reunir as evidências estruturais e mutacionais, os autores propõem que a DPMS tipo III seja uma proteína “multifunção”. Primeiro sintetiza Dol-P-Man na face interna da membrana plasmática arqueal; em seguida, seu domínio transmembrana pode ajudar a transpor a molécula açúcar–gordura para que o grupo de cabeça apareça no exterior celular, pronto para ser utilizado por outras enzimas que constroem a capa de açúcares da célula. A evolução parece ter favorecido esse desenho quimérico principalmente em arqueias extremamentes termófilas, onde trazer o local de síntese próximo a um sulco dedicado à transposição poderia minimizar desperdício e danos térmicos. Embora este trabalho ainda não comprove diretamente a atividade de transposição, ele oferece um modelo estrutural concreto de como uma enzima pode tanto criar quanto reposicionar um intermediário lipídico vital através de uma barreira de membrana hostil.
Citação: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Palavras-chave: dolicilfosfato manose, flippase de lipídios, arqueias, glicosilação de proteínas, enzimas de membrana