Clear Sky Science · pt
Modelagem da patogênese das toxinas de Clostridioides difficile e proteção por antissoro em uma plataforma intestino-em-chip imunocompetente
Por que este modelo de infecção intestinal é importante
Antibióticos salvam vidas, mas também podem deixar o intestino vulnerável a infecções perigosas. Um dos piores causadores é Clostridioides difficile, uma bactéria que pode provocar diarreia grave e inflamação do cólon potencialmente fatal, especialmente em pacientes hospitalizados. Este estudo apresenta um pequeno “intestino em um chip” que recria características essenciais do intestino humano, incluindo vasos sanguíneos e células imunes, para observar em tempo real como as toxinas de C. difficile lesam o intestino e como tratamentos com anticorpos podem interromper esse dano.
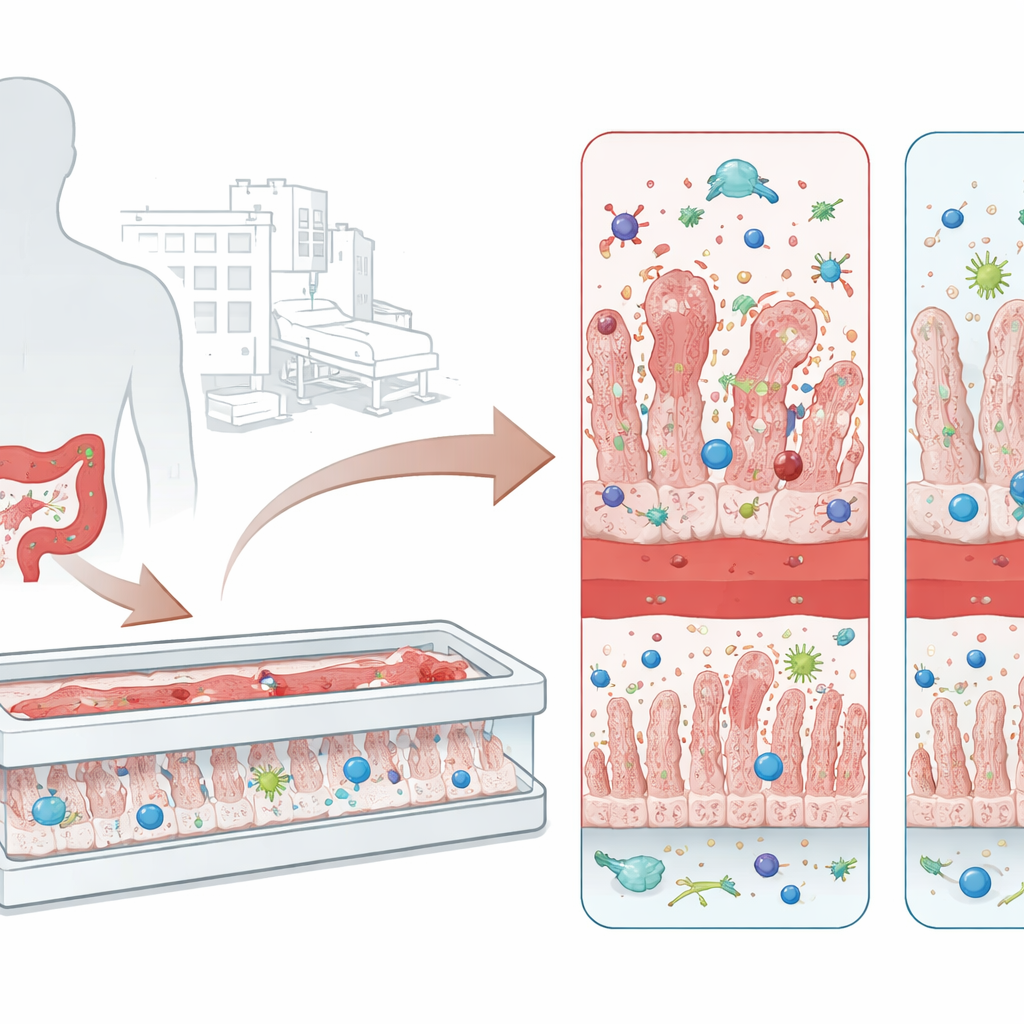
De bactéria persistente hospitalar a dano intestinal
C. difficile prospera em pessoas cuja microbiota intestinal foi perturbada, frequentemente após um ciclo de antibióticos de amplo espectro. O microrganismo sobrevive a condições adversas como esporos resistentes e, uma vez estabelecido no cólon, libera duas toxinas principais conhecidas como TcdA e TcdB. Essas toxinas atacam as células intestinais, afrouxam as junções entre elas e desencadeiam ondas de inflamação. O resultado pode variar de uma diarreia incômoda até colite pseudomembranosa, uma condição caracterizada por camadas de tecido morto e células imunes cobrindo a parede intestinal. Os tratamentos atuais dependem principalmente de mais antibióticos e, às vezes, de transplantes fecais, mas muitos pacientes experimentam reinfecções, o que ressalta a necessidade de melhores formas de estudar a doença e testar terapias que bloqueiem as toxinas.
Construindo um pequeno intestino vivo em um chip
Modelos tradicionais de laboratório cultivam uma folha plana de células intestinais em uma placa. Embora úteis, essas culturas bidimensionais carecem de vasos sanguíneos, células imunes e do fluxo gentil de fluidos que moldam um intestino real. Os pesquisadores usaram, em vez disso, um dispositivo microengenheirado “intestino-em-chip” com dois canais paralelos separados por uma membrana porosa. Um lado é revestido por células intestinais que crescem em saliências semelhantes a vilosidades e formam uma barreira rígida. O lado oposto contém células de vasos sanguíneos humanos. Nesse tecido em miniatura, a equipe adicionou macrófagos derivados de monócitos que se alojam na parede intestinal e neutrófilos circulantes que podem viajar pelo canal vascular e infiltrar o tecido, criando um intestino-em-chip imunocompetente (i‑IoC) que imita mais fielmente o intestino vivo.
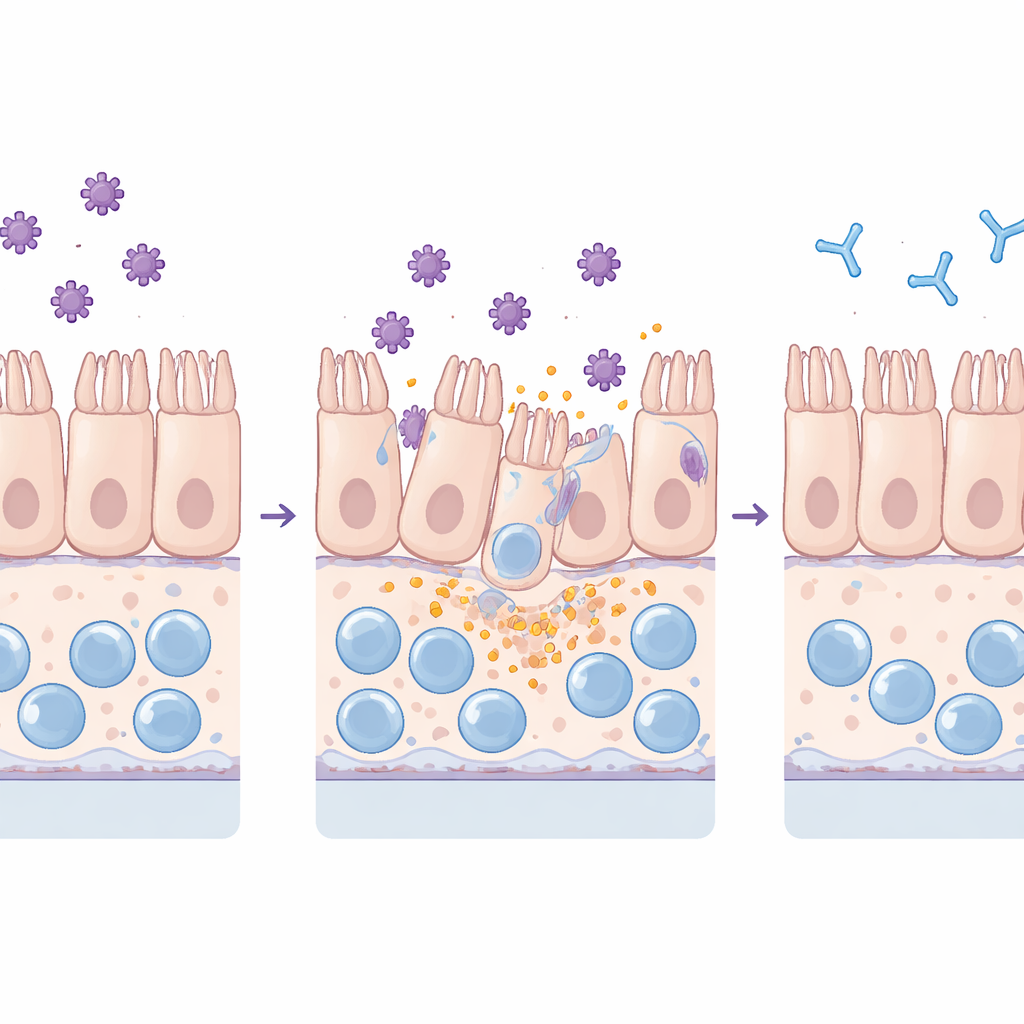
Observando as toxinas lesionarem a barreira
A equipe expôs tanto culturas planas padrão quanto o chip mais complexo às toxinas purificadas TcdA e TcdB. Monitoraram quão bem a barreira intestinal impedia a passagem de um corante fluorescente, examinaram proteínas de junção que mantêm as células vizinhas unidas e mediram moléculas inflamatórias e marcadores de lesão celular no fluido circundante. Ambas as toxinas prejudicaram o tecido, mas de maneiras distintas: a TcdA desorganizou principalmente as junções estreitas e fez as células assumirem formato arredondado, enquanto a TcdB provocou perda ampla de células da camada. Crucialmente, o chip detectou esses efeitos em níveis de toxina muito mais baixos do que as culturas planas, refletindo sua maior sensibilidade e comportamento mais semelhante ao vivo sob fluxo contínuo.
Células imunes exacerbam a resposta — e podem ser protegidas
Adicionar macrófagos e neutrófilos ao chip ampliou a resposta às toxinas. Os macrófagos aumentaram a liberação de mensageiros inflamatórios-chave, como IL‑6 e IL‑8, mas foram eles próprios depletados, compatível com uma forma inflamatória de morte celular. Neutrófilos aderiram à parede vascular e migraram para o tecido intestinal, refletindo o influxo de células imunes observado em pacientes. Exposições mais longas às toxinas danificaram não apenas o revestimento intestinal, mas também, eventualmente, a camada vascular. Quando os pesquisadores pré-misturaram as toxinas com soros contendo anticorpos neutralizantes, entretanto, o dano estrutural, o vazamento da barreira, os picos de citocinas, a perda de macrófagos e a infiltração de neutrófilos foram todos marcadamente reduzidos. Em experimentos estendidos, tecidos lesionados pela TcdB puderam se recuperar parcialmente depois que as toxinas foram removidas, enquanto a TcdA deixou danos mais persistentes, sugerindo capacidades de reparo diferentes para cada toxina.
O que isso significa para pacientes e terapias
Para um leitor leigo, a mensagem principal é que este pequeno modelo intestinal vivo pode imitar realisticamente como as toxinas de C. difficile lesam o intestino e ativam o sistema imune, além de revelar quão eficazes os anticorpos antitoxina podem ser em proteger o tecido. Em comparação com camadas celulares simples, o intestino-em-chip é mais sensível, inclui vasos sanguíneos e células imunes e pode operar por dias para captar tanto danos iniciais quanto tentativas de recuperação. Isso o torna uma plataforma promissora para testar tratamentos e vacinas de próxima geração que neutralizem toxinas sem perturbar ainda mais a microbiota intestinal, e potencialmente uma ferramenta para personalizar terapias usando células derivadas de pacientes no futuro.
Citação: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Palavras-chave: Clostridioides difficile, intestino-em-chip, infecção intestinal, anticorpos neutralizantes, modelos órgão-em-chip