Clear Sky Science · pt
Elucidando a relação entre afinidade e potência no desempenho de IgE terapêutica
Transformando anticorpos de alergia contra o câncer
Pessoas com alergia conhecem o poder dos anticorpos IgE — as moléculas que ajudam a desencadear olhos lacrimejantes e espirros súbitos. Este estudo levanta uma pergunta surpreendente: será que essa mesma biologia poderosa pode ser redirecionada para combater o câncer e, em caso afirmativo, com que precisão esses anticorpos devem ser ajustados para funcionar melhor? Os pesquisadores se concentraram em cânceres de mama que expressam uma proteína chamada HER2, inclusive casos em que o HER2 está presente em níveis muito baixos e em que as drogas atuais frequentemente falham.
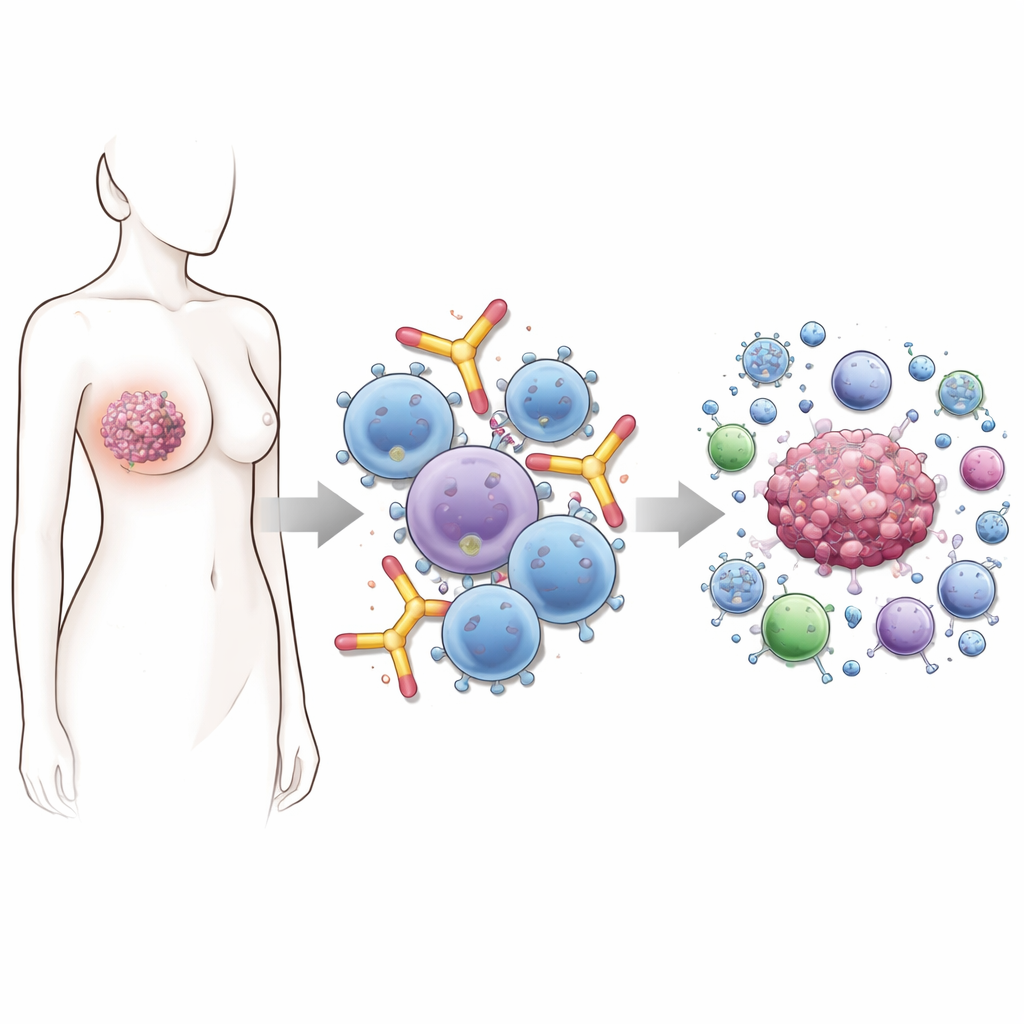
Por que essa classe de anticorpo é tão especial
A maioria dos fármacos anticorpo no mercado hoje pertence à classe IgG. Eles são os pilares da terapia moderna contra o câncer, mas têm limites — especialmente quando os tumores evitam o ataque reduzindo a quantidade da proteína-alvo na superfície. Os anticorpos IgE são diferentes. Naturalmente, eles se ligam com muita força a células imunes como mastócitos, basófilos, monócitos e macrófagos, preparando-as para respostas rápidas. Na alergia, isso significa reações explosivas a pólen ou alimentos. No câncer, a mesma arquitetura pode significar ataques rápidos e focados às células tumorais assim que a IgE encontra seu alvo na superfície do tumor.
Projetando uma IgE mais afiada em busca do câncer
A equipe já havia criado um anticorpo IgE, chamado EPS 226, que reconhece HER2 em células de câncer de mama e pode retardar o crescimento tumoral em modelos experimentais. Neste novo trabalho, eles procuraram responder a uma questão sutil mas crucial de projeto: aumentar a força com que o anticorpo agarre o HER2 melhora de fato sua capacidade de mobilizar o sistema imune, ou a ligação “de muitas mãos” típica da IgE (chamada avidez) já cumpre a maior parte do papel? Para explorar isso, usaram uma abordagem de mutagênese direcionada e seleção em bactérias para gerar milhões de pequenas variações da região de ligação ao HER2 e então selecionaram 12 novas variantes de IgE que se ligavam ao HER2 mais fortemente do que o anticorpo original.
Testando a potência em células e em animais
Esses anticorpos aprimorados foram então submetidos a testes rigorosos em uma série de experimentos celulares. Quando carregados em mastócitos e expostos a células cancerosas HER2-positivas, a maioria das IgEs de ligação mais forte desencadeou maior desgranulação — uma resposta de ativação que libera potentes mediadores imunes. Uma variante, renomeada EPS 232, destacou-se por sua capacidade de ativar células mantendo ainda ligação eficaz ao HER2 em células tumorais humanas e de rato. Testes adicionais mostraram que EPS 232 melhorou a capacidade das células imunes de matar o câncer: aumentou a citotoxicidade por basófilos e promoveu maior fagocitose de células tumorais HER2-positivas por células imunes geneticamente modificadas e por macrófagos humanos primários. Curiosamente, aumentar a força de ligação ajudou apenas até certo ponto; variantes com afinidade extremamente alta não superaram EPS 232, sugerindo que existe um “ponto ideal” em que a aderência é forte o bastante para ser eficaz, mas não tão forte que dificulte quantos anticorpos e células imunes podem se engajar em cada célula tumoral.
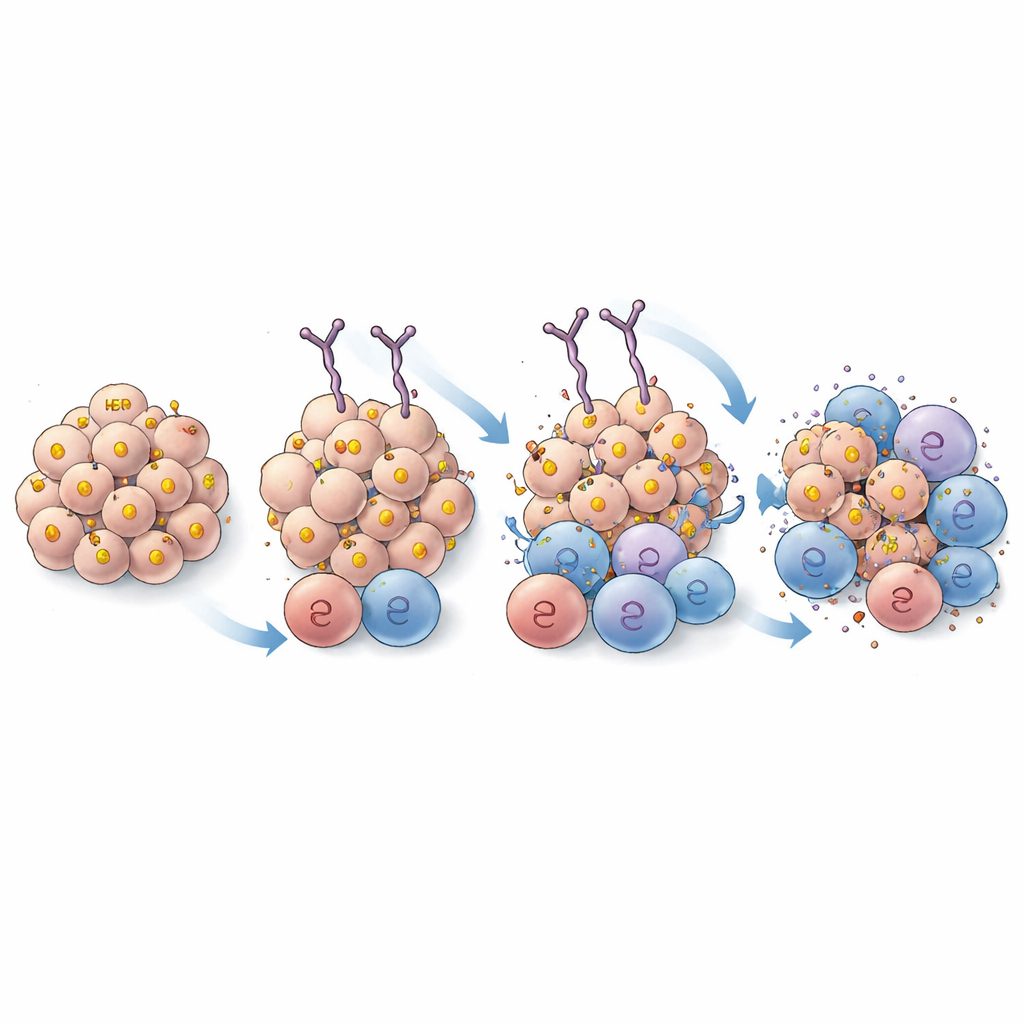
Aproximando-se de como o anticorpo se liga
Para garantir que os ganhos viessem de uma aderência mais forte e não do reconhecimento de uma nova região do HER2, os cientistas usaram criomicroscopia eletrônica de alta resolução para visualizar como EPS 232 e o EPS 226 original se acomodam na proteína HER2. As estruturas mostraram que ambos os anticorpos se acoplam à mesma região do HER2 e usam pontos de contato muito semelhantes, com apenas diferenças sutis que não deveriam alterar o sítio de ligação geral. Isso apoia a ideia de que o melhor desempenho do EPS 232 decorre de afinidade aprimorada e não de mudança de alvo.
Da bancada ao controle tumoral
O teste real veio em modelos animais. Em camundongos com tumores humanos de mama e fornecidos com células imunes humanas, EPS 232 freou o crescimento tumoral de forma mais eficaz e em doses menores do que EPS 226. Em ratos com um modelo agressivo de câncer de mama que apresenta níveis ultra-baixos de HER2 — semelhante a alguns cânceres de mama triplo-negativos — uma versão adaptada para rato do EPS 232 não só retardou o crescimento tumoral mais que sua predecessora, como também prolongou a sobrevida. Tumores de animais tratados mostraram maior infiltração de células T e macrófagos, indicando que o anticorpo melhorado remodelou o microambiente tumoral para torná-lo mais favorável ao ataque imune.
O que isso significa para futuras terapias contra o câncer
Para o leitor geral, a mensagem principal é que ajustar finamente com que força uma IgE agarra seu alvo tumoral pode fazer diferença real em sua eficácia, mesmo que a IgE já forme muitos contatos simultâneos com células. O estudo identifica EPS 232 como candidato principal de IgE contra cânceres de mama HER2-positivos e HER2-baixos, incluindo formas que atualmente carecem de boas opções de tratamento. Mais amplamente, mostra que anticorpos “no estilo alergia” podem ser projetados com o equilíbrio certo de força de ligação para transformar um sistema sensível que normalmente causa espirros em um que ajuda o sistema imune a localizar e eliminar tumores.
Citação: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
Palavras-chave: IgE terapêutica, câncer de mama HER2, afinidade de anticorpo, imunoterapia contra o câncer, câncer de mama triplo negativo