Clear Sky Science · pt
Explorando o papel duplo de vesículas extracelulares na coagulação e modulação imune no glioblastoma
Por que os coágulos importam no câncer cerebral
Pessoas diagnosticadas com glioblastoma, a forma mais agressiva de câncer cerebral, frequentemente enfrentam um perigo inesperado: coágulos perigosos nas pernas ou no cérebro. Esses coágulos podem reduzir a sobrevida e complicar tratamentos já exigentes. Este estudo faz uma pergunta simples, porém crucial: o que há nas células de glioblastoma que torna o sangue ao redor tão propenso a coagular, e como partículas minúsculas que elas liberam no sangue também remodelam as defesas imunes do corpo?
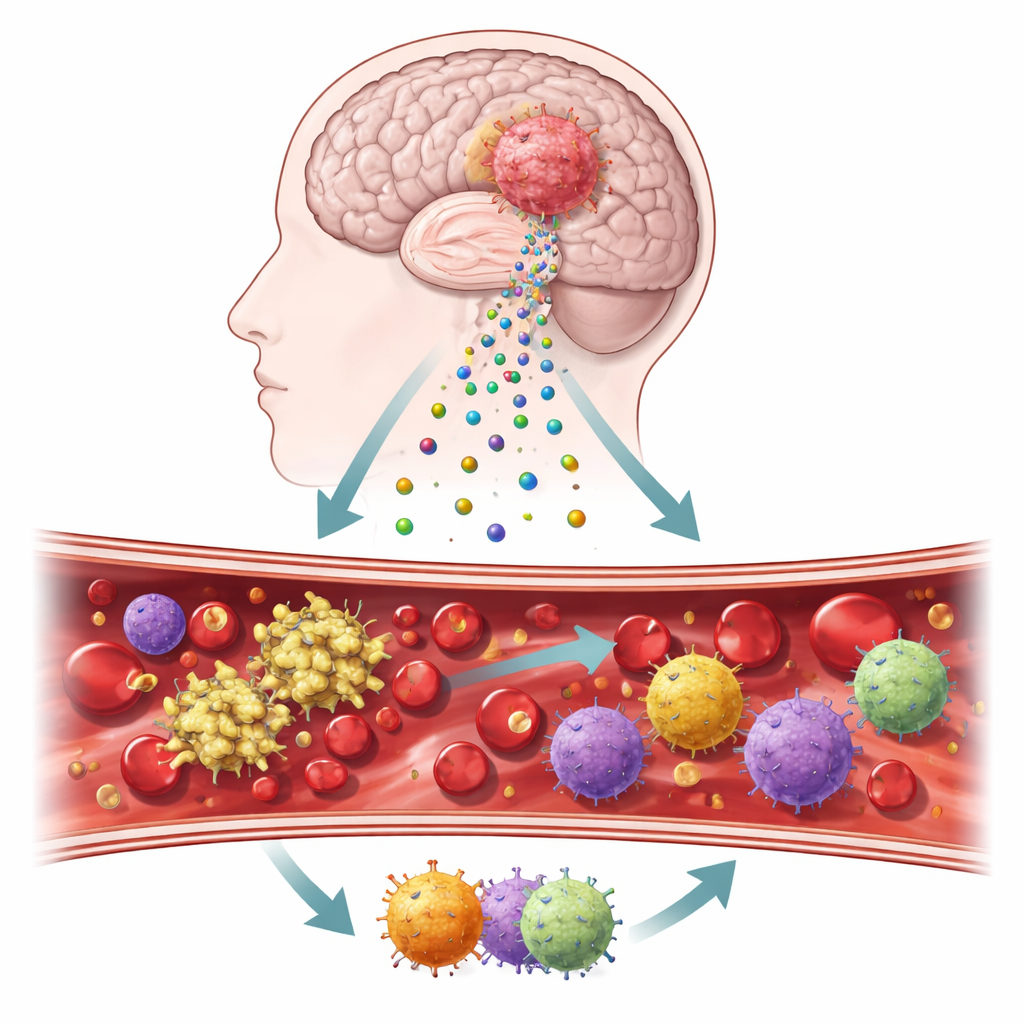
Mensageiros minúsculos saindo de um tumor cerebral
Os pesquisadores focaram em bolhas microscópicas chamadas vesículas extracelulares, que se desprendem das células tumorais e circulam pelo sangue e tecido cerebral. Essas vesículas carregam em sua superfície duas proteínas-chave, fator tecidual e podoplanina, que são conhecidas por desencadear a formação de coágulos e influenciar a inflamação. Usando amostras tumorais, sangue coletado durante a cirurgia e culturas de células derivadas dos tumores de pacientes, a equipe construiu um fluxo de trabalho em etapas para rastrear como essas moléculas se comportam em pacientes reais e em testes de laboratório controlados. Eles também compararam tecido tumoral com cérebro normal para avaliar o quão ativados estavam esses sinais ligados à coagulação.
Um fluxo sanguíneo aparentemente calmo, mas uma zona tumoral preparada
Testes hospitalares padrão sugeriram que, antes da cirurgia, o sangue de muitos pacientes parecia surpreendentemente normal: tempos de coagulação comuns e valores de firmeza do coágulo estavam em grande parte dentro das faixas de referência. Ainda assim, quando os cientistas examinaram os próprios tumores, surgiu um quadro diferente. O tecido de glioblastoma mostrou níveis consistentemente altos de fator tecidual e podoplanina e níveis muito baixos de um freio natural chamado inibidor da via do fator tecidual. Linhagens celulares derivadas dos tumores dos pacientes mantiveram em grande parte esse padrão em cultura, confirmando que a assinatura “favorável à coagulação” é uma característica intrínseca das células cancerosas. Quando essas células, ou as vesículas que elas liberavam, foram misturadas com plasma no laboratório, os coágulos se formaram mais rápido, especialmente pela chamada via extrínseca que depende do fator tecidual.
Diferentes células tumorais, diferentes estratégias de coagulação
Nem todos os glioblastomas se comportaram da mesma forma. Algumas linhagens celulares derivadas de pacientes tinham fator tecidual muito alto, outras tinham mais podoplanina e algumas tinham pouco de ambos. Células ricas em fator tecidual foram as mais potentes em reduzir o tempo de coagulação, enquanto células ricas em podoplanina contribuíram de forma modesta por efeitos sobre as plaquetas. Quando uma dessas linhagens foi separada em subgrupos que expressavam apenas fator tecidual, apenas podoplanina, ambos ou nenhum, as células não permaneceram assim por muito tempo. Ao longo de três semanas, elas retornaram para perfis mistos, revelando alto grau de plasticidade. Essa remodelação dinâmica foi acompanhada por alterações no estresse oxidativo dentro das células, sugerindo que o estresse químico no tumor pode empurrar as células para estados mais pró-coagulação.
Vesículas como moduladoras da imunidade cerebral e sanguínea
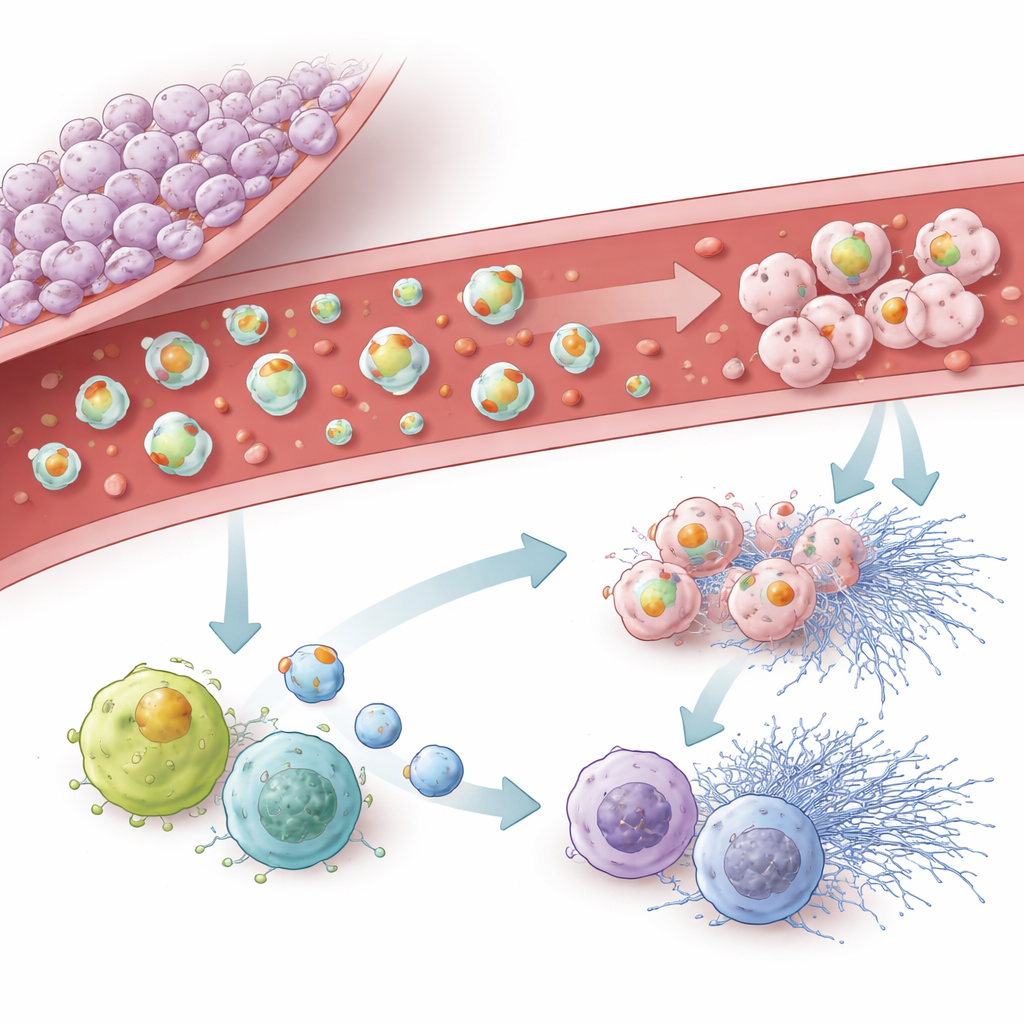
A equipe então concentrou-se em como as vesículas derivadas do tumor influenciam as próprias células imunes do cérebro, chamadas microglia, e células brancas circulantes e neutrófilos. Vesículas de linhas tumorais altamente pró-coagulação foram prontamente internalizadas pelas microglias e retardaram sua migração, ao mesmo tempo em que as deslocavam para um estado mais inflamatório, “semelhante a M1”, e sinais de envelhecimento celular. Na corrente sanguínea, vesículas ricas em fator tecidual ativaram leucócitos, aumentaram a produção de espécies reativas de oxigênio e promoveram a liberação de estruturas pegajosas em forma de teia pelos neutrófilos, conhecidas como armadilhas extracelulares. Vesículas carregando podoplanina foram menos potentes ao induzir essas reações imunes explosivas, mas estimularam fortemente um programa tipo senescência, no qual células imunes param de se dividir e mudam seu comportamento. Mesmo vesículas que não continham nenhuma das duas proteínas-chave ainda podiam provocar alguma senescência, implicando que outras cargas também importam.
O que isso significa para pacientes e cuidados futuros
Em conjunto, os achados mostram que o glioblastoma não simplesmente torna o sangue mais espesso por todo o corpo. Em vez disso, o tumor e as vesículas que ele libera criam uma zona localizada e altamente complexa onde coagulação e inflamação se alimentam mutuamente. O fator tecidual surge como o principal motor da formação de coágulos e da ativação inflamatória, enquanto a podoplanina acrescenta sua própria influência sobre plaquetas, envelhecimento imune e comportamento das microglias. Como essas vesículas circulam e espelham o estado do tumor, elas podem servir como futuros marcadores sanguíneos para identificar pacientes em risco especialmente alto de coágulos. Também podem apontar para estratégias de prevenção mais personalizadas que atinjam a maquinaria pró-coagulação do tumor sem afinar o sangue de forma ampla.
Citação: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Palavras-chave: glioblastoma, coágulos sanguíneos, vesículas extracelulares, microambiente tumoral, resposta imune