Clear Sky Science · pt
Avaliação do arcabouço de dodecina de Mycobacterium tuberculosis como plataforma de multimerização na imunogenicidade de antígenos L2 do HPV
Por que esta pesquisa importa para vacinas futuras
Os papilomavírus humanos (HPVs) causam quase todos os cânceres cervicais e uma parcela crescente de outros cânceres, contudo as vacinas atuais são complexas de fabricar e não cobrem completamente todos os tipos virais perigosos. Este estudo investiga uma nova maneira de construir uma vacina contra o HPV mais simples e de proteção mais ampla, que pode ser mais barata, mais estável e mais fácil de usar globalmente, especialmente em países de baixa e média renda. Ao reorganizar como fragmentos-chave da proteína viral são exibidos ao sistema imunológico, os pesquisadores buscam induzir o organismo a produzir anticorpos potentes contra muitos tipos de HPV ao mesmo tempo.
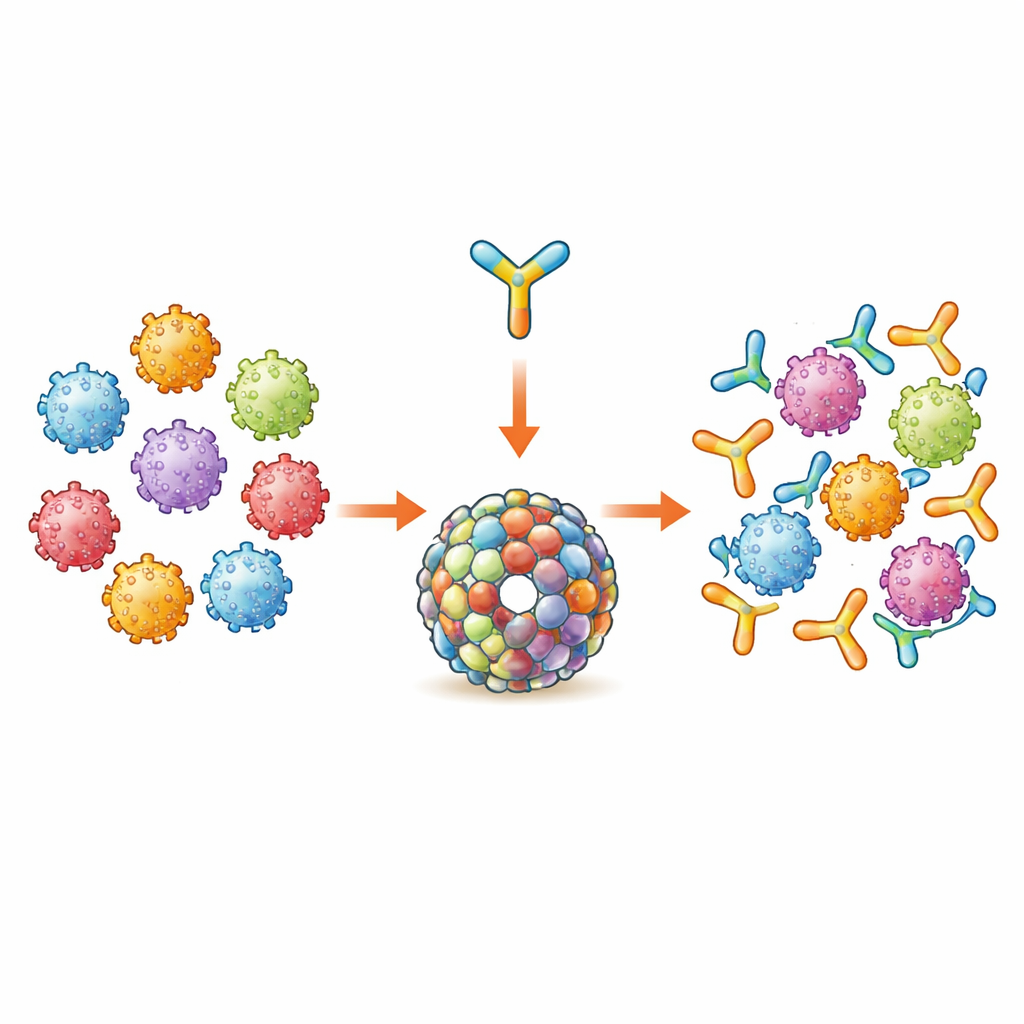
Um novo bloco de construção para proteção contra o HPV
As vacinas atuais contra o HPV dependem de uma proteína de casca viral chamada L1, montada em partículas semelhantes a vírus que estimulam fortemente a produção de anticorpos, mas principalmente contra os poucos tipos de HPV incluídos em cada vacina. A equipe concentrou-se, em vez disso, em uma segunda proteína viral, L2, que contém pequenas regiões conservadas entre muitos tipos de HPV e, portanto, pode desencadear proteção mais ampla. Eles usaram um antígeno previamente desenhado chamado Trx-8mer, no qual pequenos trechos conservados de L2 de oito tipos de HPV são costurados juntos e exibidos em um transportador proteico estável. Trabalhos anteriores já mostraram que agrupar sete dessas unidades Trx-8mer em um complexo em forma de anel (uma vacina chamada PANHPVAX) produz fortes respostas de anticorpos com proteção cruzada e atualmente está em testes humanos em estágio inicial.
Transformando uma proteína bacteriana em plataforma vacinal
Neste estudo, os pesquisadores tentaram ir além de sete cópias e acomodar ainda mais antígenos L2 em cada partícula, com a hipótese de que padrões altamente repetitivos são particularmente eficazes em ativar células B, as células produtoras de anticorpos do sistema imunológico. Eles escolheram uma pequena proteína termorresistente do microrganismo da tuberculose, chamada dodecina, que se monta naturalmente em estruturas ocas formadas por doze subunidades idênticas. Ao fundir geneticamente Trx-8mer à dodecina, criaram vários novos candidatos vacinais projetados para auto-montar nanopartículas multiméricas exibindo muitas cópias de L2. Essas partículas puderam ser produzidas em bactérias, purificadas em alta temperatura graças à sua robustez, e verificadas por múltiplos métodos biofísicos para confirmar a formação das estruturas em nanoescala pretendidas.
Quando a fusão direta não basta
Surpreendentemente, simplesmente anexar a carga L2 diretamente ao arcabouço de dodecina não superou a vacina de referência heptamérica PANHPVAX em camundongos. Embora as partículas multiméricas tenham se formado conforme o planejado e induzido anticorpos neutralizantes contra tipos de HPV vacinais e não vacinais, os títulos foram geralmente mais baixos do que os observados com PANHPVAX. Adicionar um epítopo assistente de células T embutido, que às vezes aumenta respostas de anticorpos, também não melhorou o desempenho. Modelagem estrutural e dados funcionais sugeriram que unidades volumosas de Trx-8mer fundidas diretamente podem se aglomerar e ocultar regiões críticas de L2 dos receptores das células B, atenuando a resposta imune mesmo que, em teoria, houvesse mais cópias de antígeno presentes.
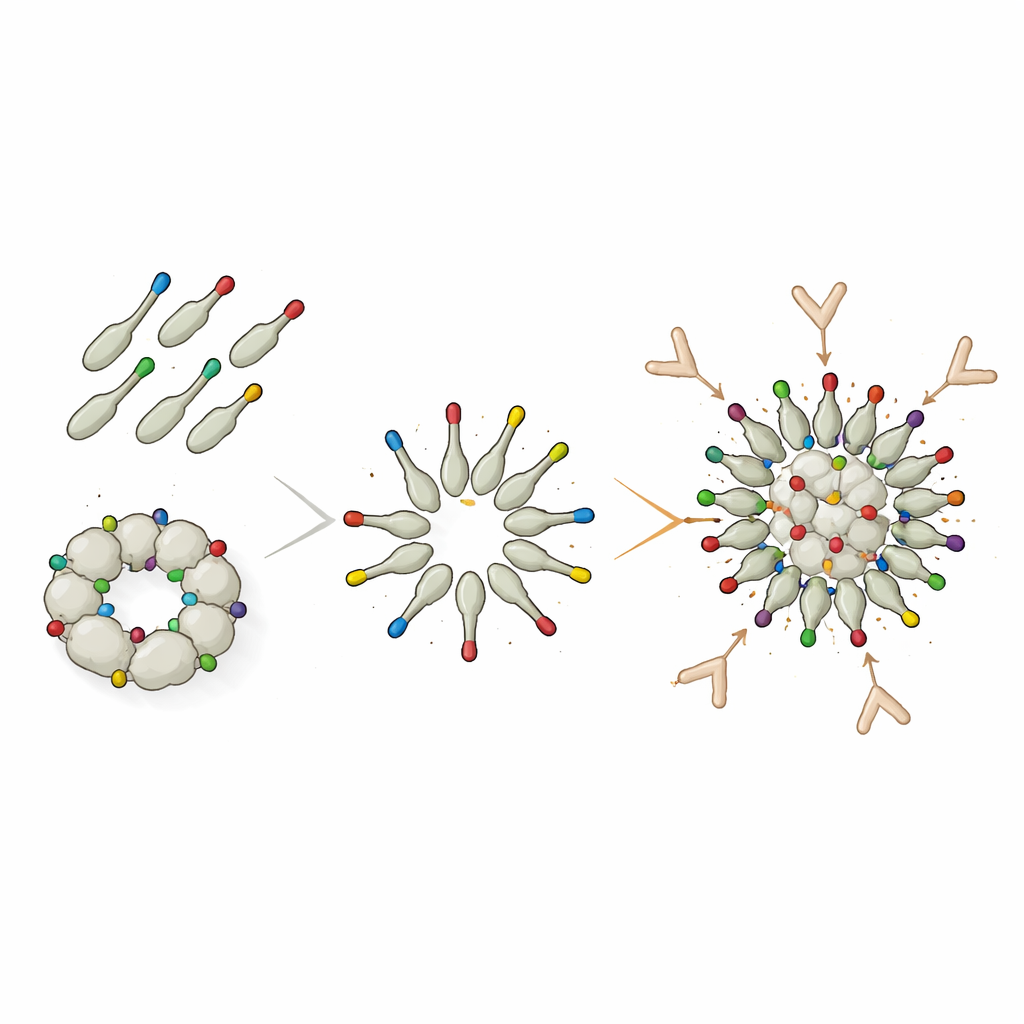
Decoração por “clique” aumenta as respostas dramaticamente
Para superar essas limitações estruturais, a equipe recorreu a um sistema modular de “cola proteica” chamado DogTag/DogCatcher. Nesse desenho, a dodecina foi produzida primeiro contendo apenas um pequeno peptídeo DogTag em sua superfície, permitindo que se montasse livremente em nanopartículas limpas. Separadamente, o antígeno Trx-8mer foi fundido ao parceiro correspondente DogCatcher. Quando misturados, Tag e Catcher se ligam por uma ligação covalente espontânea, encaixando as unidades Trx-8mer portadoras de L2 nas partículas de dodecina pré-formadas. Embora apenas cerca de metade do Trx-8mer tenha ficado presa às nanopartículas e o restante permanecesse livre em solução, camundongos imunizados com esse construto decorado produziram títulos de anticorpos neutralizantes muito mais altos contra vários tipos de alto risco do HPV do que com as partículas de fusão direta. Para alguns tipos, como HPV16, as partículas decoradas até superaram o PANHPVAX.
Implicações para vacinas contra HPV acessíveis e de ampla cobertura
Globalmente, o estudo mostra que a maneira como os antígenos são organizados no espaço pode importar mais do que o número de cópias presente no papel. Pré-montar um arcabouço nanoparticulado robusto e depois encaixar os antígenos nele proporcionou aos fragmentos L2 um espaçamento e orientação mais favoráveis, levando a respostas de anticorpos mais fortes e amplas em camundongos. Como as partículas baseadas em dodecina são pequenas, altamente termostáveis e produzidas em bactérias, elas são candidatas promissoras para vacinas contra o HPV de próxima geração que poderiam ser mais baratas de fabricar e menos dependentes da refrigeração. Com refinamento e testes adicionais, essa plataforma modular poderia suportar vacinas que protejam contra muitos tipos de HPV em uma única dose acessível, e talvez até ser adaptada para combinar componentes preventivos e terapêuticos na mesma nanopartícula.
Citação: Kaplan, E., Mariz, F.C., Zhao, X. et al. Assessment of Mycobacterium tuberculosis dodecin scaffold as a multimerization platform on the immunogenicity of HPV L2 antigens. Sci Rep 16, 9086 (2026). https://doi.org/10.1038/s41598-026-42678-7
Palavras-chave: vacina contra HPV, imunógeno nanoparticulado, antígeno L2, arcabouço de dodecina, conjugação de proteínas