Clear Sky Science · pt
Análise genética de atores-chave na cascata de sinalização PI3K do carcinoma colorretal
Por que seus genes importam para a saúde do cólon
O câncer colorretal é um dos tumores mais comuns e letais no mundo, e seus números estão aumentando em muitos países que passam por rápidas mudanças no estilo de vida. Ainda assim, nem todos com dietas ou hábitos semelhantes enfrentam o mesmo risco. Este estudo faz uma pergunta simples, porém poderosa: diferenças hereditárias em genes-chave que controlam o crescimento ajudam a explicar quem desenvolve câncer colorretal, quão agressivo ele se torna e quão eficazes são as drogas padrão — especialmente em um grande grupo de pacientes paquistaneses, uma população pouco estudada até agora?
Uma linha de controle movimentada dentro de nossas células
As células do intestino recebem constantemente sinais que lhes dizem quando crescer, dividir-se ou se autodestruir. Uma das rotas de comunicação mais ativas é a via PI3K–AKT–mTOR — uma cascata de interruptores moleculares que promove crescimento celular, sobrevivência, formação de vasos sanguíneos e resistência à morte celular. Quando essa via está hiperativa, as células podem começar a multiplicar-se descontroladamente e formar tumores. Os genes PIK3CA, AKT1 e mTOR ocupam pontos de verificação cruciais nessa via. Alterações hereditárias sutis nesses genes, chamadas polimorfismos de nucleotídeo único (SNPs), e alterações mais fortes conhecidas como mutações “hotspot” podem desequilibrar a balança em favor do câncer ou alterar como os tumores respondem ao tratamento.
Escaneando o DNA de pacientes e voluntários saudáveis
Para investigar isso, os pesquisadores conduziram um estudo caso-controle que incluiu 495 pessoas com câncer colorretal e 495 voluntários sem câncer pareados por idade e sexo. Amostras de sangue forneceram DNA, que foi examinado em relação a sete SNPs nos genes PIK3CA, AKT1 e mTOR, juntamente com duas mutações hotspot bem conhecidas chamadas E542K (em PIK3CA) e E17K (em AKT1). Usando métodos de PCR direcionada e sequenciamento de DNA, a equipe comparou com que frequência cada variante genética aparecia em pacientes versus controles e, em seguida, vinculou esses padrões a características clínicas como idade, histórico familiar, doença intestinal, estadiamento do tumor e esquemas de medicamentos recebidos pelos pacientes. 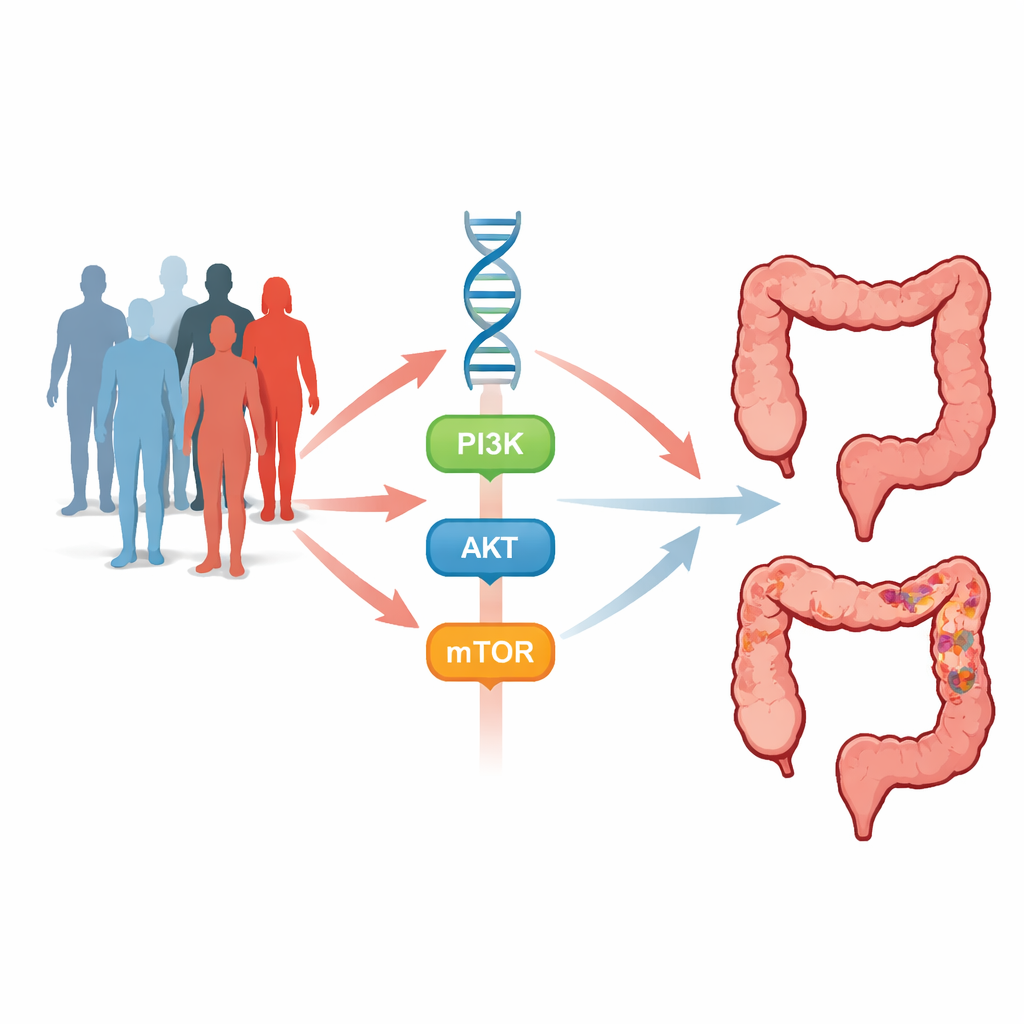
Variantes de risco e mutações potentes
A análise revelou que a maioria das variantes testadas era muito mais comum em pessoas com câncer colorretal do que em controles saudáveis, sugerindo fortemente que contribuem para o risco da doença. Várias variantes de AKT1 e mTOR, em particular, mostraram frequências marcadamente maiores em pacientes, enquanto certas versões “normais” desses genes eram mais comuns nos controles, sugerindo um papel protetor. As mutações hotspot contaram uma história ainda mais clara: a alteração E542K em PIK3CA apareceu em cerca de 15% dos pacientes, e a E17K em AKT1 em cerca de 29%, ambas muito mais frequentes do que nos controles. Modelagem por computador indicou que essas mutações não distorcem dramaticamente a forma geral da proteína, mas parecem travar a via em um estado mais “ligado”, impulsionando sinais contínuos de crescimento que favorecem o desenvolvimento tumoral.
Dos genes ao tratamento e à sobrevida
A genética isoladamente não age sozinha, por isso os pesquisadores investigaram como essas variantes interagem com fatores de risco do mundo real e com as terapias. Muitos dos SNPs foram associados ao tabagismo, doença inflamatória intestinal, histórico familiar, tipo e estadiamento do câncer e ao fato de os pacientes terem recebido quimioterapia ou radioterapia. Quando a equipe acompanhou os pacientes ao longo do tempo, descobriu que certas versões genéticas estavam ligadas a sobrevida geral melhor ou pior. Por exemplo, pessoas portadoras de versões “normais” de várias variantes de AKT1 e mTOR tendiam a viver mais do que aquelas com as versões de alto risco. O estudo também comparou a sobrevida entre pacientes que receberam combinações de drogas comuns. A capecitabina, um comprimido quimioterápico amplamente usado, associou-se às melhores estimativas de sobrevida, e várias das variantes da via pareceram influenciar quão bem diferentes regimes funcionavam, sugerindo que a genética herdada poderia orientar escolhas de tratamento mais personalizadas. 
Como as alterações viajam juntas
Além de variantes individuais, os autores examinaram como grupos de alterações tendem a ser herdados conjuntamente — um padrão conhecido como desequilíbrio de ligação. Eles descobriram um bloco de variantes vizinhas abrangendo PIK3CA e AKT1 que eram transmitidas juntas com mais frequência em pacientes do que em controles. Isso sugere que combinações de pequenas diferenças de DNA ao longo da via PI3K podem, em conjunto, moldar o risco basal de uma pessoa e o comportamento de um tumor, em vez de qualquer alteração única agir isoladamente.
O que isso significa para pacientes e medicina de precisão
Para um leitor leigo, a conclusão é que este trabalho reforça a ideia de que “um tamanho serve para todos” é um modelo inadequado para o cuidado do câncer colorretal. Nesta coorte paquistanesa, variantes hereditárias específicas e mutações hotspot em genes de controle do crescimento claramente se relacionaram com risco de câncer, características tumorais e sobrevida, e até pareceram modular como os pacientes responderam à quimioterapia padrão. Embora essas descobertas precisem ser confirmadas em grupos maiores e mais diversos, elas apontam para um futuro em que um simples exame de sangue para variantes da via PI3K–AKT–mTOR poderia ajudar a identificar quem tem maior risco, sinalizar quais pacientes podem se beneficiar de determinados medicamentos e poupar outros de tratamentos ineficazes ou desnecessariamente tóxicos.
Citação: Pervaiz, H., Masood, N., Malik, P.A. et al. Genetic analysis of key players in PI3K signaling cascade of colorectal carcinoma. Sci Rep 16, 11317 (2026). https://doi.org/10.1038/s41598-026-42006-z
Palavras-chave: genética do câncer colorretal, via PI3K AKT mTOR, polimorfismos de nucleotídeo único, oncologia de precisão, resposta à quimioterapia